
【题目】有关氨的实验室制取和性质实验如下:

(1)实验室制取氨气的化学方程式为____。
(2)如图是实验室进行氨气溶于水的喷泉实验装置,下列叙述错误的是____。
A.该实验说明氨气是一种极易溶于水的气体
B.进入烧瓶中的液体颜色由无色变为红色,说明氨水呈碱性
C.形成喷泉的原因是氨气溶于水后,烧瓶内的气压小于大气压
D.用氯气代替氨气,利用此装置也可进行喷泉实验
(3)干燥的氨气在高温下能被氧化铜氧化,生成两种单质和一种化合物。反应的化学方程式是____。
【答案】(1)2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;(2)D;(3)2NH3+3CuO
CaCl2+2NH3↑+2H2O;(2)D;(3)2NH3+3CuO![]() N2+3Cu+3H2O。
N2+3Cu+3H2O。
【解析】
试题分析:(1)实验室制取氨气用氯化铵固体和氢氧化钙的反应,其反应方程式为:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;(2)形成喷泉,利用的压强差,A、氨气溶于水形成喷泉,说明氨气极易溶于水,故错误;B、酚酞遇碱变红,说明氨水显碱性,故错误;C、喷泉利用压强差,氨气溶于水,造成瓶内压强降低,外界压强不变,把水压入烧瓶中从而形成喷泉,故错误;D、氯气在水中的溶解度较小,不能形成喷泉,故正确;(3)根据信息,得到化合物为N2、Cu、H2O,因此反应方程式为:2NH3+3CuO
CaCl2+2NH3↑+2H2O;(2)形成喷泉,利用的压强差,A、氨气溶于水形成喷泉,说明氨气极易溶于水,故错误;B、酚酞遇碱变红,说明氨水显碱性,故错误;C、喷泉利用压强差,氨气溶于水,造成瓶内压强降低,外界压强不变,把水压入烧瓶中从而形成喷泉,故错误;D、氯气在水中的溶解度较小,不能形成喷泉,故正确;(3)根据信息,得到化合物为N2、Cu、H2O,因此反应方程式为:2NH3+3CuO![]() N2+3Cu+3H2O。
N2+3Cu+3H2O。


科目:高中化学 来源: 题型:
【题目】下列实验现象描述错误的是( )
A.往稀硫酸中滴加酚酞试液,溶液变红色
B.往淀粉溶液中滴加碘水,溶液显蓝色
C.H2在C12中燃烧发出苍白色火焰
D.将SO2 通入品红溶液,溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数的值。下列说法正确的是
A.2.4g镁在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.8NA
B.标准状况下,5.6L二氧化碳气体中含有的氧原子数为0.5NA
C.8.7gMnO2与40mL 10mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA
D.0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2010年春至2013年连续四年发生在云南省的严重旱情牵动了全国人民的心,引起人们对水资源的再次重视。水是组成生命体的重要化学物质,有关水的反应有很多。
(1)在pH=1的水溶液中,一定大量共存的是_____(填序号)
①NH4+、Al3+、Br-、SO42-
② Na+、Fe2+、Cl-、NO3-
③K+、Ba2+、Cl-、NO3-
④K+、Na+、HCO3-、SO42-
(2)在下列反应中,水仅做氧化剂的是______(填字母,下同),水既不做氧化剂又不做还原剂的是________.
A.2F2+2H2O=4HF+O2
B.2Na2O2+2H2O=4NaOH+O2↑
C.CaH2+2H2O=Ca(OH)2+2H2↑
D.3Fe+4H2O![]() Fe3O4+4H2
Fe3O4+4H2
(3)“神舟七号”飞船上的能量主要来自于太阳能和燃料电池,H2、O2和KOH的水溶液可形成氢氧燃料电池,反应产生的水经冷凝后可作为航天员的饮用水,当得到1.8L饮用水时,电池内转移的电子数为___________.(NA表示阿伏加德罗常数的数值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于节能与可再生能源表述不正确的是
A.“低碳”意指更低的二氧化碳气体的排放
B.太阳能、水能、风能都属于可再生能源
C.太阳能电池的工作原理是光能与化学能的转换
D.利用燃气轮机进行天然气发电不属于可再生能源利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对乙酰氨基苯酚M(![]() )是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等。M的一种合成路线如下:
)是最常见的消炎解热镇痛药,用于治疗感冒发烧和关节痛等。M的一种合成路线如下:
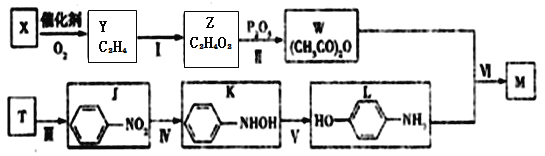
已知:①X、Y、T分子的核碰共振氢谱只显示1组峰,且X能使溴水褪色;
②![]() 。
。
(1)X、Y的结构简式为 、 ;
(2)Ⅲ的反应类型为 ,Ⅵ的反应方程式为 ;
(3)M与足量氢氧化钠溶液反应的化学方程式为 ;
(4)M有多种同分异构体,其中一类与J互为同系物且氮原子与苯环直接相连,此类同分异构体共有 种;另一类同分异构体同时满足下列条件①属于对位二取代苯且苯环上连有—NH2;②能发生水解反应;③核碰共振氢谱有4组峰。写出其中一种同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA 表示阿伏加德罗常数的值,下列叙述中正确的是
A.3g甲醛所含碳原子数为0.2NA
B.1mol CH3OH分子含有的电子总数为18NA
C.44gC3H8中含有共价键的数目为11NA
D.17g羟基中含有的电子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)NaCN为剧毒无机物。某化学兴趣小组查阅资料得知,实验室里的氰化钠溶液可使用硫代硫酸钠溶液进行统一解毒销毁,他们开展了以下三个实验,根据要求回答问题:

实验Ⅰ.硫代硫酸钠晶体(Na2S2O35H2O)的制备
已知Na2S2O3·5H2O对热不稳定,超过48℃即开始丢失结晶水。现以亚硫酸钠、硫化钠和碳酸钠等为原料、采用下述装置制备硫代硫酸钠,反应原理为:
①Na2CO3+SO2=Na2SO3+CO2
②Na2S+SO2+H2O=Na2SO3+H2S
③2H2S+SO2=3S↓+2H2O
④Na2SO3+S![]() Na2S2O3
Na2S2O3
(1)将硫化钠和碳酸钠按反应要求的比例一并放入三颈烧瓶中,注入150mL蒸馏水使其溶解,在蒸馏烧瓶中加入亚硫酸钠固体,在分液漏斗中注入_____________(填以下选择项的字母),并按上图安装好装置,进行反应。
A.稀盐酸 B.浓盐酸 C.70%的硫酸 D.稀硝酸
从以上反应可知Na2S 与Na2CO3的最佳物质的量比是___________________。
(2)pH小于7即会引起Na2S2O3溶液的变质反应,会出现淡黄色混浊。反应约半小时,当溶液中pH接近或不小于7时,即可停止通气和加热。如果SO2通过量,发生的化学反应方程式为____________________.
(3)从上述生成物混合液中获得较高产率Na2S2O35H2O的歩骤为

为减少产品的损失,操作①为趁热过滤, 操作②是________;操作③是抽滤、洗涤、干燥。
Ⅱ.产品纯度的检测
已知:Na2S2O35H2O的摩尔质量为248g/mol;2Na2S2O3+I2=2NaI+Na2S4O6。取晶体样品ag,加水溶解后,滴入几滴淀粉溶液,用0.010mol/L碘水滴定到终点时,消耗碘水溶液vmL,则该样品纯度是______________
Ⅲ.有毒废水的处理化学兴趣小组的同学在配备防毒口罩,橡胶手套和连衣式胶布防毒衣等防护用具以及老师的指导下进行以下实验:
向装有2ml0.1mol/L 的NaCN溶液的试管中滴加2ml0.1mol/L 的Na2S2O3溶液,两反应物恰好完全反应,但没有明显实验现象,取反应后的溶液少许滴入盛有10ml0.1mol/L FeCl3溶液的小烧杯,溶液呈现血红色,请写出Na2S2O3解毒的离子反应方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ如图A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
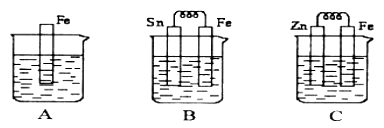
(1)B中Sn极上出现的现象________________;
(2)C中Zn片上的电极反应式为____________________;
(3)A、B、C中铁溶解的速率由快到慢的顺序是_______________。
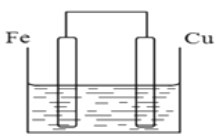
Ⅱ(4)若将质量相等的铁片和铜片用导线相连浸入硫酸铜溶液中构成原电池,如图,一段时间后,两电极质量相差1.2g,则导线中通过的电子的物质的量为_______________。
Ⅲ下图是一个化学过程的示意图,回答下列问题:
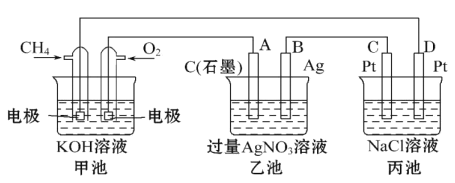
(5)甲装置中通入CH4的电极反应式为_____________________,
(6)从能量转化的角度分析,乙池是_____转化为_________的装置。
(7 )一段时间,当丙池中产生112 mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的物质的量浓度为________________。(己知:NaCl溶液足量,电解后溶液体积为500 mL)。
(8)若要使丙池恢复电解前的状态,应向丙池中通入_______(写化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com