
【题目】A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,而辛是由C元素形成的单质.已知:甲+乙=丁+辛,甲+丙=戊+辛;常温下0.1mol/L丁溶液的pH为13,则下列说法正确的是( )
A.元素C形成的单质可以在点燃条件分别与元素A、B、D形成的单质化合,所得化合物均存在共价键
B.元素B、C、D的原子半径由大到小的顺序为:r(D)>r(C)>r(B)
C.1.0 L 0.1 mol/L戊溶液中含阴离子总的物质的量小于0.1 mol
D.1 mol甲与足量的乙完全反应共转移约1.204×1024个电子
【答案】A
【解析】解:0.1mol/L 丁溶液的pH为13(25℃),丁是一元强碱,其含有的金属元素在短周期,则丁应为NaOH,发生反应:甲+乙=丁+辛,根据元素守恒可知,甲、乙两种物质至少共含有H、O、Na元素,辛是由C组成的单质,由发生反应可知,辛不能是Na,结合原子数可知,A为H、C为O、D为Na元素,故辛为氧气,可知甲是Na2O2、乙是水,再根据反应:甲+丙=戊+辛,可知丙是二氧化碳,戊是碳酸钠,则B为碳元素,
A.氧气与氢气、碳反应生成化合物只含有共价键,氧气与Na在加热条件下反应生成过氧化钠,含有离子键、共价键,故A正确;
B.同周期随原子序数增大原子半径减小,同主族自上而下原子半径增大,故原子半径大小顺序为:Na>C>O,即:D>B>C,故B错误;
C.戊是碳酸钠,在碳酸钠溶液中,CO32﹣离子水解生成HCO3﹣离子和OH﹣离子,溶液中阴离子总的物质的量大于0.1mol,故C错误;
D.甲与足量的乙完全反应的方程式为:2Na2O2+2H2O═4NaOH+O2↑,反应中过氧化钠其氧化剂、还原剂作用,各占一半,故1molNa2O2反应转移的电子为1mol× ![]() ×2=1mol,约6.02×1O23个电子,故D错误,
×2=1mol,约6.02×1O23个电子,故D错误,
故选A.
【考点精析】利用微粒半径大小的比较对题目进行判断即可得到答案,需要熟知同周期元素的原子或最高价离子半径从左到右逐渐减小(稀有气体元素除外);电子层数相同,核电荷数越大半径越小;核电荷数相同,电子数越多半径越大;电子数和核电荷数都不同的,一般通过一种参照物进行比较;具有相同电子层结构的离子,一般是原子序数越大,离子半径越小.


科目:高中化学 来源: 题型:
【题目】将两支惰性电极插入CuSO4溶液中,通电电解,当有 1 mol 的 OH-放电时,溶液显浅蓝 色,则下列叙述正确的是
A. 阳极上析出11.2 L O2(标准状况)
B. 阴极上析出 32 g Cu
C. 阴极上析出11.2 L H2(标准状况)
D. 阳极和阴极质量都无变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察如下反应,总结规律,然后完成下列问题:①Al(OH)3+H2OAl(OH) ![]() +H+;
+H+;
②NH3+H2ONH ![]() +OH﹣
+OH﹣
(A)已知B(OH)3是一元弱酸,试写出其电离方程式________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2﹣二溴乙烷的反应原理如下: CH3CH2OH ![]() CH2═CH2
CH2═CH2
CH2═CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如图所示:
有关数据列表如下:
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | 一l30 | 9 | ﹣1l6 |
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是;(填正确选项前的字母) a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入 , 其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母) a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是;
(4)将1,2﹣二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在层(填“上”、“下”);
(5)若产物中有少量未反应的Br2 , 最好用洗涤除去;(填正确选项前的字母) a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是;但又不能过度冷却(如用冰水),其原因是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应对应的离子方程式表示正确的是( )
A.FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+
B.NH4HCO3溶于过量的NaOH溶液中:HCO ![]() +OH﹣═
+OH﹣═ ![]() +H2O
+H2O
C.少量SO2通入苯酚钠溶液中:C6H5O﹣+SO2+H2O═C6H5OH+HSO ![]()
D.FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br﹣+2Cl2═2Fe3++4Cl﹣+Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对羟基扁桃酸是农药、药物、香料合成的重要中间体,它可由苯酚和乙醛酸在一定条件下反应制得. 
下列有关说法不正确的是( )
A.上述反应的原子利用率可达到100%
B.在核磁共振氢谱中对羟基扁桃酸应该有6个吸收峰
C.对羟基扁桃酸可以发生加成反应、取代反应和缩聚反应
D.1 mol对羟基扁桃酸与足量NaOH溶液反应,消耗3 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象.可以通过下列装置所示实验进行探究.下列说法正确的是( ) 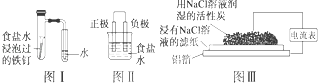
A.按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B.图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
C.铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl﹣由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl﹣﹣2e﹣═Cl2↑
D.图Ⅲ装置的总反应为4Al+3O2+6H2O═4Al(OH)3 , 生成的Al(OH)3进一步脱水形成白斑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙烯能发生以下转化: 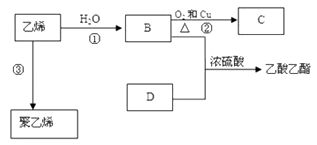
(1)乙烯的结构式为: .
(2)写出化合物官能团的化学式及名称:B中含官能团的化学式;官能团名称;
(3)写出反应的化学方程式②:反应类型:③:反应类型: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.100molL﹣1 NaOH溶液分别滴定20.00mL 0.100molL﹣1的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( ) 
A.Ⅱ表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗的V(NaOH)小于20mL
C.V(NaOH)=20.00mL时,两份溶液中c(Cl﹣)=c(CH3COO﹣)
D.V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com