
【题目】某温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g)发生反应H2(g) + CO2(g) ![]() H2O(g) + CO(g),其起始浓度如表所示,已知平衡时甲中H2的转化率为60%。下列判断正确的是
H2O(g) + CO(g),其起始浓度如表所示,已知平衡时甲中H2的转化率为60%。下列判断正确的是
起始浓度 | 甲 | 乙 | 丙 |
c(H2)[mol/L] | 0.010 | 0.020 | 0.020 |
c(CO2)[mol/L] | 0.010 | 0.010 | 0.020 |
A. 刚开始反应时,乙中的反应速率最快,甲中的反应速率最慢
B. 平衡时,乙中H2的转化率大于60%
C. 平衡时,丙中c(CO) = 0.008 mol/L
D. 该温度下,平衡常数K=9/4
【答案】D
【解析】
A.浓度越大反应速率越快,由表中数据可知,甲、乙容器内,开始CO2浓度相等,乙中H2浓度比甲中浓度大,所以速率乙>甲,乙、丙容器内,开始H2浓度相等,丙中CO2浓度比乙中浓度大,所以速率丙>乙,故速率丙>乙>甲,即丙中最快,甲中最慢,故A错误;B.乙与甲相比,相当于甲平衡后再充入氢气,则氢气的转化率小于甲,即乙中H2的转化率小于60%,故B错误;C.根据表格数据可知,甲、丙为等效平衡,平衡时,甲、丙中H2和CO2的转化率相等,甲中H2的转化率为60%,则平衡时甲容器内c(CO)=0.01mol/L×60%=0.006mol/L,丙中c(CO)是甲中的2倍,丙中c(CO) = 0.012 mol/L,故C错误;
D.对于甲容器:H2(g)+CO2(g)H2O(g)+CO(g)
开始(mol/L): 0.01 0.01 0 0
变化(mol/L): 0.006 0.006 0.006 0.006
平衡(mol/L): 0.004 0.004 0.006 0.006
所以K=![]() =
=![]() ,故D正确;故选D。
,故D正确;故选D。


科目:高中化学 来源: 题型:
【题目】某同学设计如图装置(气密性已检查)制备Fe(OH)2白色沉淀。

请回答:
(1) 仪器1的名称________。装置5的作用________。
(2) 实验开始时,关闭K2,打开K1,反应一段时间后,再打开K2,关闭K1,发现3中溶液不能进入4中。请为装置作一处改进,使溶液能进入4中________。
(3) 装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产生白色沉淀的原因________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是

A. WZ的水溶液呈碱性
B. 元素非金属性的顺序为X>Y>Z
C. Y的最高价氧化物的水化物是中强酸
D. 该新化合物中Y不满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温恒容的密闭容器中充入浓度均为1 mol/L的NH3和HCl,发生NH3(g) + HCl(g)![]() NH4Cl(?) △H = -a kJ/mol,下列说法正确的是
NH4Cl(?) △H = -a kJ/mol,下列说法正确的是
A. 现象为产生白雾
B. 反应物的活化能为a kJ/mol
C. 该条件下,混合气体的平均摩尔质量始终不变
D. 任何温度下,该反应均能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为短周期的主族元素,其原子序数依次增大,A的原子电子层数等于其核外电子数,B与C可形成离子化合物CB2,D原子的M层电子数是K层电子数的3倍。
(1)A的元素符号是____。
(2)B的氢化物与E的氢化物相比,较稳定的是___(填化学式)。
(3)C、E组成的化合物的电子式是___,其中所含化学键的类型是___。
(4)B、D、E按原子半径由大到小的顺序排列为___(填元素符号)。
(5)C的最高价氧化物对应的水化物是___,它与D的最高价氧化物对应的水化物的稀溶液发生反应的离子方程式是____。
(6)欲证明E2的氧化性强于I2,可进行的实验操作是___,观察到的现象是___,有关反应的离子方程式是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关含碳微粒的说法,按要求填空:
(1)同温度,同浓度的Na2CO3溶液的碱性_________ NaHCO3溶液的碱性(填“大于”、“小于”或“等于”),请设计一个较简便的实验证明___________。
(2)在25 ℃时,在10 mL 0.1 mol/L Na2CO3溶液中逐滴加入0.1 mol/L HCl溶液20 mL,溶液中含碳微粒的物质的量随溶液pH的变化如图所示。
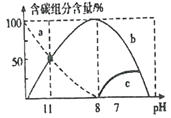
①HC1溶液滴加到一半时,溶液呈___________(填“酸性”、“碱性”或“中性”),理由是____________________(用主要的离子方程式表示)。
②关于图像下列说法正确的是_________________。
A、0.1 mol/L Na2CO3溶液中:c(Na+) + c(H+) = c(OH-) + 2c(CO32-) + c(HCO3-)
B、b曲线代表CO32-
C、pH=11时,c(HCO3-) > c(Cl-)
D、pH=11 时,c(Na+) + c(H+) = 3c(CO32-) + c(OH-)
E、在同一溶液中,H2CO3、HCO3-、CO32-能大量共存
(3)草酸(H2C2O4)溶液具有还原性,将酸性KMnO4溶液滴入草酸溶液中,会产生气泡,且紫红色褪去,写出该反应的离子方程式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究小组用碘量法来测定样品中N2H4·H2O的含量。取样品5.000 g,加水配成250 mL无色溶液,已知溶液呈碱性,取25.00 mL溶液,用滴定管盛装0.2000 mol/L的I2标准液进行滴定。滴定反应中氧化产物和还原产物分别为N2和I-。
(1)用_____________填“酸式”或“碱式”)滴定管盛装I2标准液,在取液、盛装、滴定过程中还需要的玻璃仪器有_____________________________________。
(2)滴定过程中,需要加入_____作为指示剂,滴定终点的判断方法___________。
(3)滴定前后液面如图所示,所用I2标准液的体积为________________mL。

(4)样品中水合肼(N2H4·H2O)的质量分数为_____________________,若滴定过程中,盛放I2标准液的滴定管刚开始有气泡,滴定后无气泡,则测得样品中水合肼(N2H4·H2O)的质量分数____________填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)
A | B | C | D |
NaCl溶于水 |
电解CuCl2溶液 |
CH3COOH在水中电离 |
H2与Cl2反应能量变化 |
NaCl | CuCl2 | CH3COOH | H2(g)+Cl2(g) ΔH=183kJ·mol1 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是

A. 反应2NO(g)+O2(g)![]() 2NO2(g)的ΔH>0
2NO2(g)的ΔH>0
B. 图中X点所示条件下,延长反应时间能提高NO转化率
C. 图中Y点所示条件下,增加O2的浓度不能提高NO转化率
D. 380℃下,c起始(O2)=5.0×104 mol·L1,NO平衡转化率为50%,则平衡常数K>2000
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com