
【题目】短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是
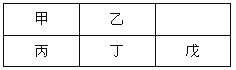
A. 原子半径:丙<丁<戊B. 金属性:甲>丙
C. 氢氧化物碱性:丙>丁>戊D. 最外层电子数:甲>乙
 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】分类是学习和研究化学的一种重要方法,下列分类合理的是
A.K2CO3和K2O都属于盐B.KOH和Na2CO3都属于碱
C.H2SO4和HNO3都属于酸D.Na2O和Na2SO3都属于氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子一定能够大量共存的是
A.Na+、OH-、SO42-、Fe3+B.K+、SO42-、CO32-、H+
C.Na+、Ca2+、Cl-、CO32-D.Ba2+、Na+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3 为中学化学中经常使用的物质,长郡化学实验小组为探究 FeCl3 的性质,进行了如下实验。
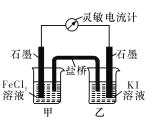
(1)学习小组 A 为探究 FeCl3与 KI 溶液的反应,特设计如右图所示的原电池实 验装置。在实验过程中,学习小组 A 发现,灵敏电流计的指针先偏转,最后 示数为零。若此时向甲中加入适量 FeCl2 固体,灵敏电流计的指针又发生偏转 此时________(填“甲”或“乙”)中石墨电极为负极,对应的电极反应方程式为_________
(2)学习小组 B 把 FeCl3 溶液分别加入Na2CO3 溶液和Na2SO3溶液中,发现有如下实验现象:
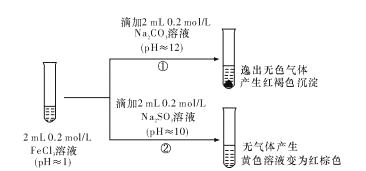
对于②中的实验现象,学习小组 B 的同学们有诸多猜测,继续进行实验: I.小明取②中的红棕色溶液少许,滴入盐酸酸化的 BaCl2溶液,产生白色沉淀。小明得出结论:FeCl3 与 Na2SO3 发生了氧化还原反应,离子方程式是_____。
Ⅱ,小红认为小明的实验不严谨,重新设计实验方案并进行实验,证实了小明的结论是正确的。其实验方 案是______________________________。
(3)学习小组 C 进一步探究 FeCl3 溶液与足量锌粉的反应。实验操作及实验现象如下表所示:

已知:Zn 的化学性质与 Al 相似,能发生反应![]()
①结合实验现象和平衡移动原理解释出现红褐色沉淀的原因:______
②分离出黑色固体,经下列实验证实了其中含有的主要物质。
i.黑色固体可以被磁铁吸引
ii.向黑色固体中加入足量的 NaOH 溶液,产生气泡;
iii.将 ii 中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡; iv.向 iii 反应后的溶液中滴加 KSCN 溶液,无变化。 a.黑色固体中一定含有的物质是_____。
b.学习小组 C 认为上述实验无法确定黑色固体中是否含有 Fe3O4,理由是__________________
(4)为进一步探究 1.0 mol/L FeCl3 溶液中 Fe3+和 H+氧化性的相对强弱,学习小组 C 补充实验并观察到反应开始时的实验现象如下表所示:
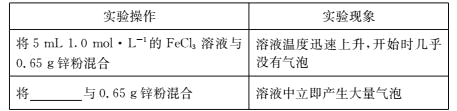
学习小组 C 得出结论:在 1.0 mol/L FeCl3 溶液中,Fe3+的氧化性比 H+强。则表格中横杠处应填____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢气体在资源利用和环境保护等方面均有重要应用。
(1)工业采用高温分解H2S制取氢气,2H2S(g) ![]() 2H2(g) + S2(g),在膜反应器中分离出H2。在容积为 2L 的恒容密闭容器中,控制不同温度进行此反应。H2S的起始物质的量均为 1mol,实验过程中测得H2S的转化率如图所示。曲线 a 表示H2S的平衡转化率与温度的关系,曲线 b 表示不同温度下反应经过相同时间时H2S的转化率。
2H2(g) + S2(g),在膜反应器中分离出H2。在容积为 2L 的恒容密闭容器中,控制不同温度进行此反应。H2S的起始物质的量均为 1mol,实验过程中测得H2S的转化率如图所示。曲线 a 表示H2S的平衡转化率与温度的关系,曲线 b 表示不同温度下反应经过相同时间时H2S的转化率。
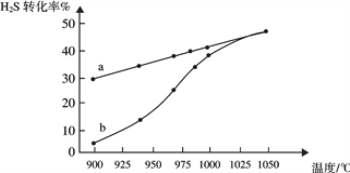
①反应2H2S(g) ![]() 2H2(g) + S2(g)的ΔH_________(填“>”“<”或“=”)0。
2H2(g) + S2(g)的ΔH_________(填“>”“<”或“=”)0。
②985℃时,反应经过5 s达到平衡状态,此时H2S的转化率为40%,则用H2表示的反应速率为v(H2) =___________。
③随着H2S分解温度的升高,曲线b向曲线a逐渐靠近,其原因是___________。
(2)将H2S和空气的混合气体通入FeCl3 、FeCl2 、CuCl2的混合溶液中反应回收S,其物质转化如下图所示。
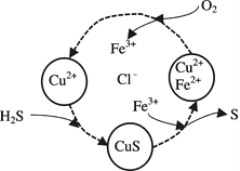
①在图示的转化中,化合价不变的元素是____________。
②在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含CuS,可采取的措施有____________。
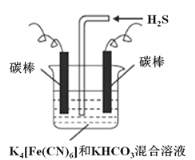
(3)工业上常采用上图电解装置电解K4[Fe(CN)6]和KHCO3混合溶液,电解一段时间后,通入H2S 加以处理。利用生成的铁的化合物K3[Fe(CN)6]将气态废弃物中的H2S 转化为可利用的S,自身转化为K4[Fe(CN)6]。
①电解时,阳极的电极反应式为___________。
②当有16 g S析出时,阴极产生的气体在标准状况下的体积为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com