
【题目】非金属及其化合物在生产、生活中应用广泛。
Ⅰ.CO2的有效利用可以缓解温室效应和能源短缺问题,CO2的分子结构决定了其性质和用途。
(1)CO2的电子式是______,包含的化学键类型为______共价键(填“非极性”或“极性”)。
(2)在温度高于31.26 oC、压强高于7.29×106 Pa时,CO2处于超临界状态,称为超临界CO2流体,可用作萃取剂提取草药中的有效成分。与用有机溶剂萃取相比,超临界CO2萃取的优点有______(答出一点即可)。
Ⅱ.氯水以及氯的化合物经常用于饮用水的消毒。
(3)将铁片插入盛有少量新制氯水的试管中,无气泡产生,用长滴管吸取KSCN溶液滴入铁片附近,溶液变红色,然后红色消失。显红色的离子方程式为______。
(4)净水丸能对饮用水进行快速的杀菌消毒,药丸通常分内外两层。外层的优氯净Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去。
①优氯净中氯元素的化合价为___________。
②亚硫酸钠将水中多余次氯酸除去的反应的化学方程式为_______________。
【答案】![]() 极性 萃取剂与溶质更易分离或萃取剂更环保等 Fe3++3SCN-Fe(SCN)3 +1 Na2SO3+HClO=Na2SO4+HCl
极性 萃取剂与溶质更易分离或萃取剂更环保等 Fe3++3SCN-Fe(SCN)3 +1 Na2SO3+HClO=Na2SO4+HCl
【解析】
(1)CO2为共价化合物,C与每个O原子间都以双键相连。
(2)超临界CO2萃取的优点,可从成本、分离、环保等方面考虑。
(3)用长滴管吸取KSCN溶液滴入铁片附近,溶液变红色,表明溶液中含有Fe3+,显红色是Fe3+与SCN-反应生成Fe(SCN)3。
(4)优氯净Cl2Na(NCO)3先与水反应生成次氯酸,则表明Cl元素显+1价;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去,则HClO与SO32-发生氧化还原反应生成SO42-、Cl-等。
(1)CO2为共价化合物,C与每个O原子间都以双键相连,电子式为![]() ;包含的化学键类型为极性共价键。答案为:
;包含的化学键类型为极性共价键。答案为:![]() ;极性;
;极性;
(2)从成本、分离、环保等方面考虑,超临界CO2萃取的优点为萃取剂与溶质更易分离或萃取剂更环保等。答案为:萃取剂与溶质更易分离或萃取剂更环保等;
(3)用长滴管吸取KSCN溶液滴入铁片附近,溶液变红色,表明溶液中含有Fe3+,显红色是Fe3+与SCN-反应生成Fe(SCN)3,离子方程式为Fe3++3SCN-Fe(SCN)3。答案为:Fe3++3SCN-Fe(SCN)3;
(4)优氯净Cl2Na(NCO)3先与水反应生成次氯酸,则表明Cl元素显+1价;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去,则HClO与SO32-发生氧化还原反应生成SO42-、Cl-等,化学方程式为Na2SO3+HClO=Na2SO4+HCl。答案为:+1;Na2SO3+HClO=Na2SO4+HCl。


科目:高中化学 来源: 题型:
【题目】下列推理正确的是
A. 铝粉在氧气中燃烧生成Al2O3,铁丝在氧气中燃烧也生成Fe2O3
B. 铁能从硫酸铜溶液中置换出铜,钠也能从硫酸铜溶液中快速置换出铜
C. 铝片表面易形成致密的氧化膜,钠块表面也易形成致密的氧化膜
D. 钠与氧气、水等反应时钠均作还原剂,金属单质参与氧化还原反应时金属均作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用于汽车刹车片的聚合物 Y 是一种聚酰胺纤维,合成路线如图:
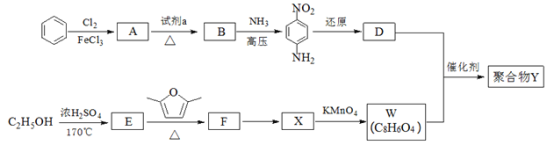
已知:![]()
(1)生成 A 的反应类型是_____。
(2)试剂 a 是_____。
(3)B 中所含的官能团的名称是_____。
(4)W、D 均为芳香化合物,分子中均只含两种不同化学环境的氢原子。
①F 的结构简式是_____。
②生成聚合物 Y 的化学方程式是_____。
(5)Q 是 W 的同系物且相对分子质量比 W 大 14,则 Q 有______种,其中核磁共振氢谱有4 组峰,且峰面积比为 1∶2∶2∶3 的为___________(写一种结构简式即可)。
(6)试写出由 1,3﹣丁二烯和乙炔为原料(无机试剂及催化剂任用)合成![]() 的合成路线__________________。(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
的合成路线__________________。(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关反应14CuSO4+5FeS2+12H2O===7Cu2S+5FeSO4+12H2SO4的下列说法中错误的是
A. CuSO4在反应中被还原
B. FeS2既是氧化剂也是还原剂
C. 14 mol CuSO4氧化了1 mol FeS2
D. 被还原的S和被氧化的S的质量之比为3∶7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
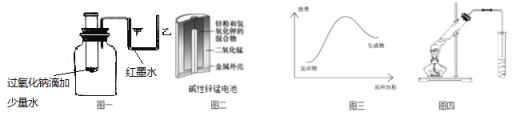
A.图一可表示模拟反应的能量变化,反应后左侧液面上升,右侧液面下降
B.图二所示电池中,MnO2的作用是催化剂
C.图三可表示需加热的放热反应
D.图四可用于乙酸和乙醇的酯化反应,小试管中是饱和碳酸钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的NaCl溶液时,下列操作不正确的是( )
A. 接近称量质量时,轻振手腕,加够药品
B. 溶解时,用量筒控制所加蒸馏水的量
C. 移液时,玻璃棒插在刻度线上,防止液体洒出![]()
D. 接近刻度线1~2cm时,用胶头滴管滴加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用活性铁可以很好地消除酸性水体中NO3-造成的污染,除去原理如图所示。下列说法中正确的是
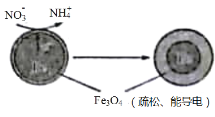
A.铁电极的电极反应式:3Fe-8e-+4H2O=Fe3O4+8H+
B.NO3-在负极上发生还原反应
C.除NO3-的过程中水体pH减小
D.当电路中有4 mol电子转移时,溶液中会有1 mol NH4+生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物A经李比希法测得其中含碳为70.59%、含氢为 5.88%,其余含有氧。现用下列方法测定该有机化合物的相对分子质量和分子结构。
方法一:用质谱法分析得知A的质谱如图:
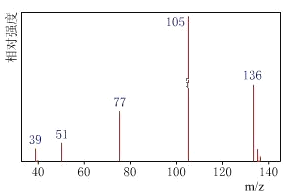
方法二:核磁共振仪测出A的核磁共振氢谱有4个峰,其面积之比为1∶2∶2∶3。
方法三:利用红外光谱仪测得A分子的红外光谱,如图:
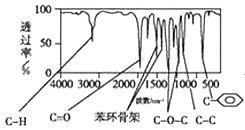
(1)分子中共有____种化学环境不同的氢原子。
(2)A的分子式为____。
(3)该物质属于哪一类有机物____。
(4)A的分子中只含一个甲基的依据是____(填序号)。
a A的相对分子质量 b A的分子式
c A的核磁共振氢谱图 d A分子的红外光谱图
(5)A的结构简式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。

下列说法不正确的是
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效提高反应物的平衡转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com