

���� ��1��Ԫ�صķǽ�����Խǿ����縺��Խǿ��
��2�����⻯ﮣ�LiBH4��������ڹ��ۼ������Ӽ���
��3���ٸ���Bԭ���γɵļ۲���Ӷ����жϣ�
����ͼ��֪Bԭ���γ���4�����ۼ������Bԭ�ӵļ۵�����������
��4��һ��H3BO3�к���3��O-H�������γ�3��H-O��H��
��� �⣺��1��Ԫ�صķǽ�����Խǿ����縺��Խǿ���ǽ����ԣ�F��B��Na����縺�ԣ�F��B��Na��
�ʴ�Ϊ��F��B��Na��
��2�����⻯ﮣ�LiBH4���������H-B���ۼ������Ӽ��������ڽ���������������»�����
�ʴ�Ϊ��ade��
��3������Ļ�����F3B-N��CH3��3���ɽṹͼ��֪��Bԭ���γ�4�����ۼ�������۲���Ӷ���Ϊ4����Ϊsp3�ӻ���
�ʴ�Ϊ��sp3��
����ͼ��֪�û�������һ��Bԭ����3��Fԭ�ӽ���γ�3��B-F���ۼ���ͬʱ����һ��Nԭ�ӽ���γ�N-B������Bԭ��ֻ��3���۵��ӣ������ṩһ���չ���γ���λ�������Ըû������д�����λ����
�ʴ�Ϊ���У��û�������һ��Bԭ����3��Fԭ�ӽ�ϵ�ͬʱ����һ��Nԭ�ӽ�ϣ���Bԭ��ֻ��3���۵��ӣ������ṩһ���չ���γ���λ����
��4��һ��H3BO3�к���3��O-H�������γ�3��H-O��H����1mol H3BO3�����к���3mol�����
�ʴ�Ϊ��3��
���� ���⿼���˻�ѧ�����縺�ԵıȽϡ��ӻ����͵��жϡ���λ��������ȣ���Ŀ�Ѷ��еȣ�ע����������������ʵĽṹͼ�������ڿ���ѧ���ķ��������ͶԻ���֪ʶ��Ӧ��������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ȼ�����Һ�еμ�HI��Һ��2Fe3++2HI�T2Fe2++2H++I2 | |
| B�� | ��NH4Al��SO4��2��Һ�е���Ba��0H��2ǡ��ʹ��Ӧ��ȫ��2Ba2++4OH-+Al3++2SO42-�T2BaSO4+AlO2-+2H2O | |
| C�� | 1mol/L��NaAlO2��Һ��2.5 mol/L��HCl��������Ȼ��2AlO2-+5H+�TAl��OH��3+Al3++H2O | |
| D�� | �ù���������ữ�ĺ����ҽ���Һ����ȡ�⣺2I-+H2O2�TI2+2OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��SO2ͨ��Ʒ����Һ������ˮ����ʹ������ɫ����˵��SO2����Ư���� | |
| B�� | պ��Ũ��ˮ��պ��ŨHNO3�IJ���������ʱ�а��̲���������Ϊ�����л�ԭ�� | |
| C�� | ij��Һ�еμ�ϡNaOH��Һ����ʪ���ɫʯ����ֽ�����Թܿڣ���ֽ��������˵����Һ��һ��û��NH4+ | |
| D�� | NH3•H2O���Ȳ��ȶ��Կ��Խ���ʵ�������ü��Ȱ�ˮ�İ취��ȡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
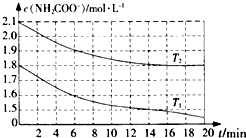 ��ѧ�о�С���������泥�NH2COONH4���ķֽ��ˮ�ⷴӦ����̽����
��ѧ�о�С���������泥�NH2COONH4���ķֽ��ˮ�ⷴӦ����̽�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��NaCl��������Na+�����Cl-��6�� | |
| B�� | ��NaCl�����У�ÿ������ʵ��ӵ��4��Na+��4��Cl- | |
| C�� | �ڽ��ʯ�����У�̼ԭ����̼̼������Ŀ��Ϊ1��4 | |
| D�� | �ڽ��ʯ�����У���С������6��̼ԭ�ӹ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ���������������ԭ��Ӧ����ѧ��ת���ɵ��ܵ�װ�� | |
| B�� | ����A��B�õ������Ӻ����ϡ���������ԭ���ʱ��A����������B�Ľ�����ǿ��A | |
| C�� | ��ѧ��Ӧ�ﵽƽ��״̬ʱ��ֻҪ�������ı䣬�����ʵ�Ũ�ȾͲ��ٸı� | |
| D�� | ���ڷ�ӦN2��g��+3H2��g��?2NH3��g������λʱ����ÿ����1molN2��ͬʱ����3molH2��˵����Ӧ����ѧƽ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
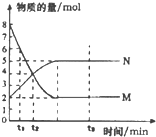
| A�� | ��Ӧʽ��a��b=2��5 | |
| B�� | 0-t1����M��Ũ��c��M��������1mol•L-1 | |
| C�� | t2ʱ��c��M��=c��N��=4mol•L-1����Ӧһ���ﵽƽ��״̬ | |
| D�� | t3ʱ��c��M�����ٱ仯������Ӧ����С���淴Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧʽ | ��ɫ | Ksp |
| AgCl | ��ɫ | 2.0��10-10 |
| AgBr | dz��ɫ | 5.4��10-13 |
| AgI | ��ɫ | 8.3��10-17 |
| Ag2S | ��ɫ | 2.0��10-48 |
| Ag2CrO4 | ��ɫ | 2.0��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
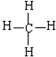 ��
�� ���γɵľ��������Ӿ��壮
���γɵľ��������Ӿ��壮�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com