
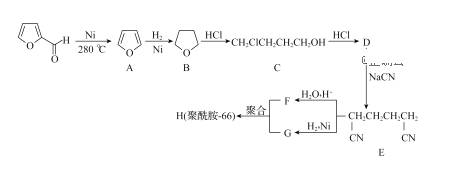
【题目】糠醛(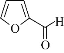 ),又称a一呋喃甲醛,是一种制备多种药物和化工产品的原料。一种由它制备锦纶-66的合成路线如图:
),又称a一呋喃甲醛,是一种制备多种药物和化工产品的原料。一种由它制备锦纶-66的合成路线如图:
已知:(1)R-CN![]() R-COOH R-CN
R-COOH R-CN![]() R-CH2NH2
R-CH2NH2
(2)RCHO+CH3CHO![]() RCH=CHCHO+H2O
RCH=CHCHO+H2O
回答下列问题:
(1)C中含有的官能团名称为______。
(2)有机物D的化学名称为________。
(3)由D生成E的反应类型为_______。
(4)写出F和G反应生成H的化学方程式:______。
(5)糠醛催化加氢后的产物为C5H10O2,与其互为同分异构体且属于酯的有机物共有_____种。
(6)以糠醛和乙醇为原料(其他试剂任选),设计制备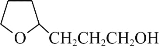 的合成路线。______
的合成路线。______
【答案】羟基和氯原子 1,4-二氯丁烷 取代反应 nHOOC(CH2)4COOH+n H2N(CH2)6NH2![]() +(2n+1)H2O 9
+(2n+1)H2O 9 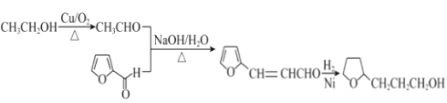
【解析】
(1)根据流程图中C的结构简式,C中含有的官能团名称为羟基和氯原子;
答案为:羟基和氯原子
(2)有机物C在HCl作用下发生取代反应,将C中的羟基取代转化为D,故有机物D的结构式为CH2ClCH2CH2CH2Cl,D的化学名称为1,4-二氯丁烷;
答案为:1,4-二氯丁烷
(3)由D生成E过程中,D中的氯原子被-CN原子团取代得到E,因此由D生成E反应类型为取代反应。
答案为:取代反应;
(4)根据已知条件(1)E在酸性条件下与水反应,-CN原子团转化为-COOH生成F,F的结构式为HOOCCH2CH2CH2CH2COOH;E在Ni做催化剂条件下与氢气发生加成反应,-CN转化为-CH2NH2生成G,G的结构式为H2NCH2CH2CH2CH2CH2CH2NH2,F和G反应生成H的化学方程式:nHOOC(CH2)4COOH+n H2N(CH2)6NH2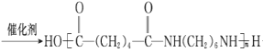 +(2n+1)H2O;
+(2n+1)H2O;
答案为:nHOOC(CH2)4COOH+n H2N(CH2)6NH2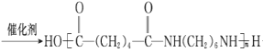 +(2n+1)H2O。
+(2n+1)H2O。
(5)糠醛催化加氢后的产物为C5H10O2,与其互为同分异构体且属于酯的有机物,除糠醛加氢后的环状结构外,其余分别HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3、CH3COOCH2CH2CH3、CH3COOCH(CH3)2、CH3CH2COOCH2CH3、CH3CH2CH2COOCH3、(CH3)2CHCOOCH3;共有9种。
答案为:9
(6)以糠醛和乙醇为原料(其他试剂任选),制备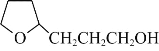 的合成路线
的合成路线
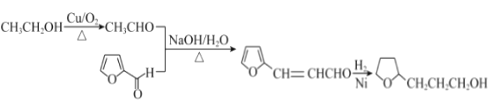
答案为: 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】由两种有机物组成的混合物,在一定的温度和压强下完全气化为气体.在相同的温度和压强下,只要混合气体体积一定,那么无论两物质以何种比例混合,其完全燃烧时所消耗的氧气体积就是一定的,符合这种情况的可能组合是:
A. 乙醇(![]() )和乙酸(
)和乙酸(![]() ) B. 乙醛(
) B. 乙醛(![]() )和甲醇(
)和甲醇(![]() )
)
C. 丙醛(![]() )和甘油(
)和甘油(![]() ) D. 丙酮(
) D. 丙酮(![]() )和丙二醇(
)和丙二醇(![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知溴乙烷(C2H5Br)是无色液体,沸点38.4℃,密度比水大,难溶于水,可溶于多种有机溶剂。在溴乙烷与NaOH乙醇溶液的消去反应中可以观察到有气体生成。有人设计了如图所示的装置,用KMnO4酸性溶液是否褪色来检验生成的气体是否是乙烯。

请回答下列问题:
(1)仪器a的名称为__________。
(2)实验前应检测装置A的气密性。方法如下:关闭止水夹c,由仪器a向仪器b中加水,若______________________________,则证明装置A不漏气。
(3)仪器b中发生反应的化学方程式为______________________________。
(4)反应开始一段时间后,在装置B底部析出了较多的油状液体,若想减少油状液体的析出,可对装置A作何改进?__________________________________________________
(5)装置A中产生的气体通入装置C之前要先通过装置B,装置B的作用为__________________。
(6)检验乙烯除用KMnO4酸性溶液外还可选用的试剂有__________,此时,是否还有必要将气体先通过装置B?__________(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一块金属钠露置于空气中,观察到下列现象:
![]()
请回答下列问题:
(1)白色粉末的化学式是__________,过程②的化学方程式是_________。
(2)下列说法正确的是________。
A. 过程③为物理变化
B. 过程④是碳酸钠吸收空气中的CO2、水蒸气形成了碳酸氢钠
C. 过程⑤发生了分解反应
D. 整个变化过程中只有一个氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组利用如图所示装置制备少量NCl3。已知:NCl3可由Cl2与NH4Cl溶液在适宜温度下反应生成。常温下,NCl3为黄色油状液体,熔点为-40℃,沸点为71℃;极易爆炸,自然爆炸点为95℃。
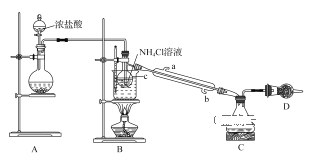
回答下列问题:
(1)装置A中圆底烧瓶内所盛放的固体是___(填化学式)。
(2)装置B中仪器C的名称是___,实验过程中该仪器内发生反应的化学方程式为___。
(3)装置B的烧杯中应控制水浴加热的温度范围为____。
(4)装置D中所盛放的试剂不能为下列选项中的___(填字母)。
a.生石灰 b.NaOH固体 C.碱石灰 d.无水CaCl2
(5)查阅资料可知,电解pH<5的NH4Cl溶液也可制得NCl3,则电解池中产生NCl3的电极为___(填“阴极’’或“阳极’’),该电极的电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,可用离子方程式![]() +
+![]() =
=![]() 表示的是
表示的是
A.NH4Cl+NaOH![]() NaCl+NH3↑+H2O
NaCl+NH3↑+H2O
B.Mg(OH)2+2HCl=MgCl2+2H2O
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)现有浓度均为![]() 的盐酸、硫酸、醋酸三种溶液,回答下列问题:
的盐酸、硫酸、醋酸三种溶液,回答下列问题:
(1)若三种溶液中![]() 分别为
分别为![]() ,则它们的大小关系为_________________________________________。
,则它们的大小关系为_________________________________________。
(2)等体积的以上三种酸分别与过量的![]() 溶液反应,若生成的盐的物质的量依次为
溶液反应,若生成的盐的物质的量依次为![]() ,则它们的大小关系为__________________________。
,则它们的大小关系为__________________________。
(3)分别用以上三种酸中和一定量的![]() 溶液生成正盐,若需要酸的体积分别为
溶液生成正盐,若需要酸的体积分别为![]() ,其大小关系为__________________________________。
,其大小关系为__________________________________。
(4)分别与锌反应,开始时生成氢气的速率为![]() ,其大小关系为______________________。
,其大小关系为______________________。
(二)有![]() 四种强电解质,它们在水中电离产生下列离子(每种物质只含一种阴离子且互不重复)。
四种强电解质,它们在水中电离产生下列离子(每种物质只含一种阴离子且互不重复)。
阳离子 |
|
阴离子 |
|
已知:①![]() 溶液的
溶液的![]() 均大于7,
均大于7, ![]() 的溶液中水的电离程度相同;②
的溶液中水的电离程度相同;②![]() 溶液和
溶液和![]() 溶液相遇时只生成白色沉淀,
溶液相遇时只生成白色沉淀, ![]() 溶液和
溶液和![]() 溶液相遇时只生成刺激性气味的气体,
溶液相遇时只生成刺激性气味的气体, ![]() 溶液和
溶液和![]() 溶液混合时无现象。
溶液混合时无现象。
(1) ![]() 是_________________________,
是_________________________,![]() 是_______________________(填化学式)。
是_______________________(填化学式)。
(2)写出![]() 和
和![]() 反应的离子方程式_________________________________。
反应的离子方程式_________________________________。
(3) ![]() 时,
时, ![]() 溶液的
溶液的![]() ,则
,则![]() 溶液中
溶液中![]() _________________________________________(用含有
_________________________________________(用含有![]() 的关系式表示)。
的关系式表示)。
(4)将等体积、等物质的量浓度的![]() 溶液和
溶液和![]() 溶液混合,反应后溶液中各种离子浓度由大到小的顺序是_________________________。
溶液混合,反应后溶液中各种离子浓度由大到小的顺序是_________________________。
(5)在一定体积的![]() 的
的![]() 溶液中,加入一定体积的
溶液中,加入一定体积的![]() 的盐酸,混合溶液的
的盐酸,混合溶液的![]() ,若反应后溶液的体积等于
,若反应后溶液的体积等于![]() 溶液与盐酸的体积之和,则
溶液与盐酸的体积之和,则![]() 溶液与盐酸的体积比是_______________。
溶液与盐酸的体积比是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知浓硫酸的密度是1.84g/mL,物质的量浓度为18.4mol/L,质量分数为98%。取10mL浓硫酸和a mL水混合得到溶液的物质的量浓度为c mol/L,质量分数为b%。下列组合正确的是( )
(1)若c=9.2,则a<18.4,b>49 (2)若c=9.2,则a<18.4,b<49
(3)若b=49,则a=18.4,c<9.2 (4)若b=49,则a=18.4,c>9.2。
A.(1)(3)B.(1)(4)C.(2)(3)D.(2)(4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W为短周期主族元素,在元素周期表中的相对位置如下图所示,其中Z元素原子之间通常形成Z2分子。下列说法不正确的是( )
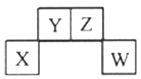
A. X元素的单质既能与强酸反应也能与强碱反应
B. Y元素形成的氢化物在常温下不一定为气体
C. W元素的最高价氧化物对应水化物一定为强酸
D. 由Y、Z、W三种元素形成的二元化合物中只含共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com