
ЁОЬтФПЁПЯТСаИїЛЏКЯЮяжаЃЌОљЮЊШѕЕчНтжЪЕФвЛзщЪЧ
A. H2CO3 Ba(OH)2 K2S H3PO4 B. FeCl3 HCl C2H5OH NH4Cl
C. CH3COOH H2CO3 Cu(OH)2 H2O D. HCl KNO3 H2CO3 H2SO4
 аЁбЇПЮЪБзївЕШЋЭЈСЗАИЯЕСаД№АИ
аЁбЇПЮЪБзївЕШЋЭЈСЗАИЯЕСаД№АИ Н№АцПЮЬУПЮЪБбЕСЗЯЕСаД№АИ
Н№АцПЮЬУПЮЪБбЕСЗЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙЄвЕШМЩеУКЁЂЪЏгЭЕШЛЏЪЏШМСЯЪЭЗХГіДѓСПNOxЁЂCOЁЂCO2ЕШЦјЬхЃЌбЯжиЮлШОПеЦјЃЌЖдЗЯЦјНјааЭбЯѕЃЌЭбЬМЕШДІРэПЩЪЕЯжТЬЩЋЛЗБЃЁЂЗЯЮяРћгУЁЃ
ЂёЁЂЭбЯѕЃК
вбжЊЃКЂйH2ЕФШШжЕЮЊ142.9kJ/gЃЈШШжЕЪЧБэЪОЕЅЮЛжЪСПЕФШМСЯЭъШЋШМЩеЩњГЩЮШЖЈЕФЛЏКЯЮяЪБЫљЗХГіЕФШШСПЃЉЃЛ
ЂкN2(g)+2O2(g)=2NO2(g) ІЄH=+133kJ/mol
ЂлH2O(g)=H2O(l) ІЄH=-44kJ/mol
ДпЛЏМСДцдкЯТЃЌH2ЛЙдNO2ЩњГЩЫЎеєЦјКЭЦфЫћЮоЖОЮяжЪЕФШШЛЏбЇЗНГЬЪНЮЊЃК_______
ЂђЁЂЭбЬМ
ЃЈ1ЃЉCOгыПеЦјПЩЩшМЦГЩШМСЯЕчГиЃЈвдШлШкЕФЬМЫсбЮЮЊЕчНтжЪЃЉЁЃаДГіИУЕчГиЕФИКМЋЗДгІЪНЃК_______ЁЃ
ЃЈ2ЃЉМзДМЪЧвЛжжПЩдйЩњФмдДЃЌЙЄвЕЩЯПЩгУКЯГЩЦјжЦБИМзДМЃЌЗДгІЮЊCO(g)+2H2(g) ![]() CH3OH(g)ЁЃФГЮТЖШЯТдкШнЛ§ЮЊVLЕФУмБеШнЦїжаНјааЗДгІЃЌЦфЯрЙиЪ§ОнтгвЭМЃЛЗДгІПЊЪМжСЦНКтЪБЃЌгУH2БэЪОЛЏбЇЗДгІЫйТЪЮЊ________ЁЃИУЮТЖШЯТCOЕФЦНКтзЊЛЏТЪЮЊ_________ЁЃ
CH3OH(g)ЁЃФГЮТЖШЯТдкШнЛ§ЮЊVLЕФУмБеШнЦїжаНјааЗДгІЃЌЦфЯрЙиЪ§ОнтгвЭМЃЛЗДгІПЊЪМжСЦНКтЪБЃЌгУH2БэЪОЛЏбЇЗДгІЫйТЪЮЊ________ЁЃИУЮТЖШЯТCOЕФЦНКтзЊЛЏТЪЮЊ_________ЁЃ
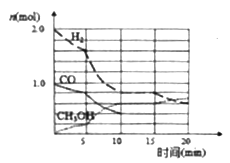
ЃЈ3ЃЉЯђ1LУмБеШнЦїжаМгШы1molCO2ЁЂ3molH2ЃЌдкЪЪЕБЕФЬѕМўЯТЃЌЗЂЩњЗДгІCO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g).
CH3OH(g)+H2O(g).
ЂйЯТСаа№ЪіФмЫЕУїДЫЗДгІДяЕНЦНКтзДЬЌЕФЪЧ___________ЁЃ
a.ЛьКЯЦјЬхЕФЦНОљЯрЖдЗжзгжЪСПБЃГжВЛБф
b.CO2КЭH2ЕФЬхЛ§ЗжЪ§БЃГжВЛБф
c.CO2КЭH2ЕФзЊЛЏТЪЯрЕШ
d.ЛьКЯЦјЬхЕФУмЖШБЃГжВЛБф
e.1molCO2ЩњГЩЕФЭЌЪБгж3molH-HМќЖЯСб
ЂкЯрЭЌЬѕМўЯТЃЌдкШнЛ§ЖМЮЊ1LЧвЙЬЖЈЕФСНИіУмБеШнЦїжаЃЌАДШчЯТЗНЪНМгШыЗДгІЮяЃЌвЛЖЮЪБМфКѓЗДгІДяЕНЦНКтЁЃ
ШнЦї | Мз | вв |
ЗДгІЮяЭЖШыСП | 1mol CO2ЁЂ3molH2 | amol CO2ЁЂ3amolH2 bmolCH3OH(g)ЁЂbmolH2O(g) |
ШєМзжаЦНКтКѓЦјЬхЕФбЙЧПЮЊПЊЪМЕФ0.6БЖЃЌвЊЪЙЦНКтКѓввгыМзжаЯрЭЌзщЗжЕФЬхЛ§ЗжЪ§ЯрЕШЃЌЧвЦ№ЪМЪБЮЌГжЛЏбЇЗДгІЯђФцЯђЗДгІЗНЯђНјааЃЌдђbЕФШЁжЕПЩФмЮЊ_________ЃЈЬюађКХЃЉ
a.0.7 b.0.9 c.1.2
ШєБЃГжЮТЖШВЛБфЃЌЦ№ЪММгШы0.5molCO2ЁЂ0.5molH2ЁЂ0.5molCH3OH(g)ЁЂ0.5molH2O(g) дђДЫЗДгІЫйТЪЕФЙиЯЕЃКvе§__________vФцЁЃЃЈЬюЁА>ЁБЁЂЁА<ЁБЛђЁА=ЁБЃЉ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙЄвЕЩЯвдТШЦјКЭЪЏЛвШщЮЊдСЯжЦдьЦЏАзЗлЃЎЦЏАзЗлЕФгааЇГЩЗжЪЧЃЈ ЃЉ
A.Cl2
B.CaCl2
C.CaЃЈOHЃЉ2
D.CaЃЈClOЃЉ2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЛЏКЯЮягЩСНжжЕЅжЪжБНгЗДгІЩњГЩЃЌНЋЦфМгШыBa(HCO3)2ШмвКжаЭЌЪБгаЦјЬхКЭГСЕэВњЩњЁЃЯТСаЛЏКЯЮяжаЗћКЯЩЯЪіЬѕМўЕФЪЧ
A. AlCl3 B. Na2O C. FeCl2 D. SiO2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪГДзЕФзмЫсСПМДвЛЖЈЬхЛ§ЕФЪГДздвКЫљКЌДзЫсЕФжЪСПЃЌЕЅЮЛЪЧgЁЄ L-1ЛђИіg/100mLЁЃЙњМвБъзМЙцЖЈФ№дьЪГДззмЫсКЌСПВЛЕУЕЭгк3.5g/100mLЁЃ
ЃЈ1ЃЉгУЫсМюЕЮЖЈЗЈВтЖЈФГЪГДзбљЦЗжаЕФзмЫсСПЪБЃЌЯТСаЫЕЗЈжае§ШЗЕФЪЧ ЁЃ
AЃЎгУNaOHШмвКЕЮЖЈЪБЗДгІЕФРызгЗНГЬЪНЮЊH++OH-=H2O
BЃЎЪГДзбљЦЗВЛашвЊдЄЯШЯЁЪЭвЛЖЈБЖЪ§КѓПЩвджБНгНјааЕЮЖЈ
CЃЎгУNaOHШмвКЕЮЖЈЪБЃЌПЩЪЙгУЗгЬЊЛђМзЛљГШзїжИЪОМС
DЃЎШєВтЕУбљЦЗЕФЮяжЪЕФСПХЈЖШЮЊ0.75molЁЄL-1ЃЌдђЦфзмЫсСПЮЊ45gЁЄL-1
ЃЈ2ЃЉФГЭЌбЇзаЯИЙлВьИУЪГДзбљЦЗЕФБъЧЉЃЌЗЂЯжЦфжаЛЙКЌгазїЮЊЪГЦЗЬэМгМСЕФБНМзЫсФЦЃЈC6H5COONaЃЉЃЌЫћЯыгУРэТлбщжЄДзЫсгыБНМзЫсФЦВЛЛсЗЂЩњРызгЛЅЛЛЗДгІЃЌашВщевдквЛЖЈЮТЖШЯТДзЫсгыБНМзЫсЕФ ЁЃ
AЃЎpH BЃЎЕчРыЖШ CЃЎЕчРыГЃЪ§ DЃЎШмНтЖШ
ЃЈ3ЃЉГЃЮТЯТЃЌгУ0.1000molЁЄ L-1 NaOHШмвКЗжБ№ЕЮЖЈ20.00mL 0.1000molЁЄ L-1 HClШмвККЭ20.00mL 0.1000molЁЄ L-1 CH3COOHШмвКЃЌЕУЕНСНЬѕЕЮЖЈЧњЯпЃЌШчЭМЫљЪОЁЃ
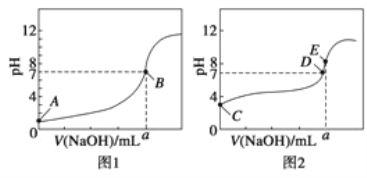
ЂйЕЮЖЈДзЫсШмвКЕФЧњЯпЪЧ ЃЈЬюЁАЭМ1ЁБЛђЁАЭМ2ЁБЃЉЃЛЕЮЖЈЧњЯпжаa= mLЃЛ
ЂкEЕуpHЃО8ЕФдвђЪЧЃЈгУРызгЗНГЬЪНБэЪОЃЉЃК ЁЃ
ЃЈ4ЃЉВтЖЈЪГДзЕФзмЫсСПЪЕбщжаЃЌХфжЦNaOHШмвККЭЯЁЪЭЪГДзЫљгУЕФеєСѓЫЎБиаыжѓЗаЃЌФПЕФЪЧ ЁЃ
ЃЈ5ЃЉЪЕбщЪБЃЌЮќШЁЪГДзбљЦЗ10mLгк100mLШнСПЦПжаЖЈШнЁЃвЦШЁЖЈШнКѓЕФШмвК20mLгкзЖаЮЦПжаЃЌМгШы1ЁЋ2ЕЮжИЪОМСЃЌгУХЈЖШЮЊc molЁЄL-1ЕФNaOHБъзМШмвКЕЮЖЈЃЌЦНааВтЖЈШ§ДЮЃЌЯћКФNaOHШмвКЕФЦНОљЬхЛ§ЮЊV mLЁЃдђдЪГДзбљЦЗЕФзмЫсСП=____________g/100mLЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФПЧАЙЄвЕКЯГЩАБЕФдРэЪЧN2(g)+3H2(g)=2NH3(g) ЁїH=-93.0kJ/mol
ЃЈ1ЃЉвбжЊвЛЖЈЬѕМўЯТЃК2N2(g)+6H2O(l)=4NH3(g)+3O2(g) ЁїH=-+1530.0kJ/molЁЃдђЧтЦјШМЩеШШЕФШШЛЏбЇЗНГЬЪНЮЊ_________________ЁЃ
ЃЈ2ЃЉШчЯТЭМЃЌдкКуЮТКуШнзАжУжаНјааКЯГЩАБЗДгІЁЃ

ЂйБэЪОN2ХЈЖШБфЛЏЕФЧњЯпЪЧ_________ЁЃ
ЂкЧА25minФкЃЌгУH2ХЈЖШБфЛЏБэЪОЕФЛЏбЇЗДгІЫйТЪЪЧ_____________ЁЃ
Ђлдк25minФЉИеКУЦНКтЃЌдђЦНКтГЃЪ§K=___________ЁЃ
ЃЈ3ЃЉдкКуЮТКубЙзАжУжаНјааЙЄвЕКЯГЩАБЗДгІЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ_______________ЁЃ
AЃЎЦјЬхЬхЛ§ВЛдйБфЛЏЃЌдђвбЦНКт
BЃЎЦјЬхУмЖШВЛдйБфЛЏЃЌЩаЮДЦНКт
CЃЎЦНКтКѓЃЌЭљзАжУжаЭЈШывЛЖЈСПArЃЌбЙЧПВЛБфЃЌЦНКтВЛвЦЖЏ
DЃЎЦНКтКѓЃЌбЙЫѕШнЦїЃЌЩњГЩИќЖрNH3
ЃЈ4ЃЉЕчГЇбЬЦјЭбЕЊЕФжїЗДгІЮЊЃК4NH3(g)+6NO(g)=5N2(g)+6H2O(g) ЁїH<0
ИБЗДгІЮЊЃК2NH3(g)+8NO(g)=5N2O(g)+3H2O(g) ЁїH>0
ЦНКтЛьКЯЦјжаN2гыN2OКЌСПгыЮТЖШЕФЙиЯЕШчЯТЭМЫљЪОЁЃ

ЧыЛиД№ЃКдк400ЁЋ600KЪБЃЌЦНКтЛьКЯЦјжаN2КЌСПЫцЮТЖШЕФБфЛЏЙцТЩЪЧ______ЃЌЕМжТетжжЙцТЩЕФдвђЪЧ_________ЃЈШЮД№КЯРэЕФвЛЬѕдвђЃЉЁЃ
ЃЈ5ЃЉжБНгЙЉАБЪНШМСЯЕчГиЪЧвдNaOHШмвКЮЊЕчНтжЪШмвКЃЌЕчГиЗДгІЮЊ4NH3ЃЋ3O2=2N2+6H2OЁЃдђИКМЋЕчМЋЗДгІЪНЮЊ_______________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЗДгІдквЛЖЈЬѕМўЯТПЩвдЪЕЯжЕФЪЧЃЈ ЃЉ
ЂйЫсадбѕЛЏЮягыМюЗДгІ ЂкгаЕЅжЪВЮМгЕФЗЧбѕЛЏЛЙдЗДгІ
ЂлУЛгаЫЎЩњГЩЃЌвВУЛгаГСЕэКЭЦјЬхЩњГЩЕФИДЗжНтЗДгІ
ЂмСНжжЫсШмвКГфЗжЗДгІКѓЕФШмвКГЪжаад
A. 1Иі B. 2Иі C. 3Иі D. 4Иі
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЮяжЪжаЃЌЪєгкЗЧЕчНтжЪЕФЪЧ
A. ОЦОЋ B. Cl2 C. NaOH D. H2SO4
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГбаОПадбЇЯАаЁзщЮЊЬНОПФГвНвЉЙЋЫОГіЦЗЕФвКЬхВЙбЊМСжаЕФЬњдЊЫиЃЌНјааСЫШчЯТЪЕбщЁЃ
Ђё. дњЮїЯђЪдЙмжаМгШывКЬхВЙЬњМС2mLЃЌМгШыеєСѓЫЎЃЌеёЕДКѓЗЂЯжШмвКБфГЮЧхЭИУїЃЛЕЮМгKSCNШмвКЃЌШмвКЯдЪОЕКьЩЋЁЃдњЮїОнДЫШЯЮЊДЫВЙбЊМСКЌЬњСПКмЕЭЃЌЪєВЛКЯИёВњЦЗЁЃ
Ђђ. зПТъШЯЮЊНіЦОдњЮїЕФжЄОнЛЙВЛФмЫЕУїДЫВЙбЊМСВЛКЯИёЃЌгкЪЧЫ§НЋдњЮїЪЕбщЫљЕУШмвКЗжГЩСНЗнЃЌЗжБ№МгШыСЫТШЫЎЁЂфхЫЎЁЃЗЂЯжМгШыТШЫЎЁЂфхЫЎКѓШмвКГЪбЊКьЩЋЃЌбеЩЋУїЯдМгЩюЁЃзПТъОнДЫШЯЮЊДЫВЙбЊМСЪЧЗёКЯИёЛЙашвЊдйМјЖЈЁЃ
Ђѓ. ЛЦФнЖддњЮїзіЕФЪЕбщКмИааЫШЄЃЌЫ§ЯђдњЮїЪЕбщЫљЕУЕФЕКьЩЋШмвКжаМгШыЙ§СПЬњЗлЃЌЗЂЯжДЫШмвКЕФЧГКьЩЋКмПьЭЪШЅЁЃ
ЧыИљОнвдЩЯМЧТМЛиД№ЯТСаЮЪЬтЃК
(1)ФуШЯЮЊдњЮїКЭзПТъЕФЙлЕуЫе§ШЗЃП__________ЁЃ
(2)ИљОнзПТъКЭЛЦФнЕФЩЯЪіЪЕбщЫЕУїВЙбЊМСжаЕФЬњгІИУЮЊ____________МлЁЃ
(3)ЕЋдњЮїжБНгЯђВЙбЊМСШмвКжаЕЮМгKSCNШмвКЃЌНсЙћЯдЪОСЫЕКьЩЋЕФдвђПЩФмЪЧ____________________ЁЃ
(4)ЧыаДГізПТъЯђШмвКжаМгШыТШЫЎКѓЫљЗЂЩњЕФЗДгІЕФРызгЗДгІЗНГЬЪН
______________ЁЃ
(5)ИљОнзПТъЕФЪЕбщЯжЯѓПЩвдЭЦЖЯЃЌТШЁЂфхЕФЕЅжЪПЩНЋЬњЕЅжЪбѕЛЏГЩ____________МлЬњЃЌЧыаДГіфхЕЅжЪгыFeЕЅжЪдкЕуШМЕФЬѕМўЯТЗДгІЕФЛЏбЇЗНГЬЪН_____________________ЁЃ
(6)ЧыаДГіЛЦФнЕФЪЕбщжаЪЙЕКьЩЋЭЪШЅЕФРызгЗНГЬЪН_________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com