
【题目】炼铁的反应原理为:Fe2O3+3CO![]() 3CO2+2Fe,当有2molFe生成时。下列说法中,错误的是( )
3CO2+2Fe,当有2molFe生成时。下列说法中,错误的是( )
A.参加反应的Fe2O3和CO物质的量分别为1mol、3mol
B.将生成67.2L标准状况下的CO2气体
C.参加反应的Fe2O3的质量为160g
D.参加反应的Fe2O3、CO与生成CO2的体积比为1:3:3
科目:高中化学 来源: 题型:
【题目】用如图中装置进行实验,实验一段时间后,现象与预测不一致的是
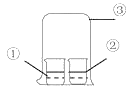
①中物质 | ②中物质 | 实验预测 | |
A | 浓氨水 | 酚酞试液 | ②中溶液变为红色 |
B | 浓硝酸 | 淀粉KI溶液 | ②中溶液变为蓝色 |
C | 浓盐酸 | 浓氨水 | 大烧杯中有白烟 |
D | 饱和的亚硫酸溶液 | 稀溴水 | ②中无明显变化 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热 42g NaHCO3 和 Na2CO3 固体混合物,至没有气体放出时,剩余的固体质量是 35.8 g。那么原固体混合物中Na 2CO3 的质量是
A. 25.2g B. 16.8 g C. 10.6 g D. 24.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果不正确的是
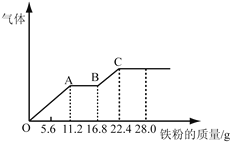
A. 混合酸中HNO3物质的量浓度为2mol/L
B. OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C. 原混合酸中H2SO4物质的量为0.4 mol
D. 第二份溶液中最终溶质为FeSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种有机物,它们的转化关系如图所示(图中部分反应条件及生成物没有全部写出).已知:液体B能发生银镜反应,气体D的相对分子质量为28.
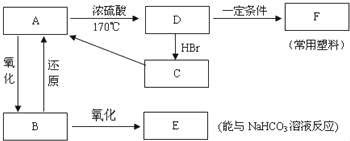
(1)A、B、C的结构简式分是 、 、 .
(2)B、C中所含官能团的名称分别是 、 .
(3)A到D的反应类型为 .
(4)C→A的反应条件是 .
(5)D→F反应的化学方程式是 .
(6)在一定的条件下,A与E反应可生成一种具有香味的物质.该反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是某化学课外活动小组配制500mL3.5mol·L-1NaOH溶液的操作。
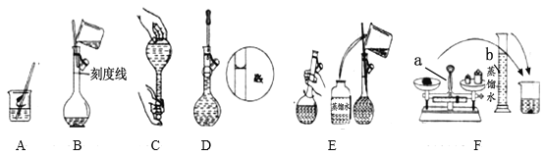
(1)请写出下列仪器的名称:仪器a___,仪器b ___。
(2)配制溶液时,所用容量瓶上标有的数据为___。
(3)在配制过程中,玻璃棒所起的作用有___。
(4)容量瓶使用前,要检验是否漏水,检验是否漏水的实验操作为___。
(5)请你按照配制一定物质的量浓度溶液的具体操作排出操作的顺序:
以上步骤中,正确的操作步骤顺序为F→ → → → → (填序号)。___。
(6)上述操作的图示中存在错误的是___(填序号,用大写字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的含氧衍生物的球棍模型如图所示(图中球与球之间连线代表化学键单键或双键)。下列关于该有机物的说法正确的是( )
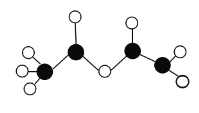
A.该有机物的名称是乙酸乙酯
B.该有机物能使Br2的CCl4或酸性高锰酸钾褪色,原理相同
C.该有机物能发生取代反应、氧化反应和消去反应
D.该有机物的同分异构体中能与NaHCO3反应产生气体的链状结构只有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。下列说法不正确的是

A. 电流由O2所在的铂电极经外电路流向另一电极
B. O2所在的铂电极处发生还原反应
C. 该电池的负极反应式为:CH3CH2OH+3H2O-12e-="=" 2CO2↑+12H+
D. 微处理器通过检测电流大小而计算出被测气体中酒精的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)黑火药爆炸时发生反应:2KNO3+S+3C=K2S+N2↑+3CO2↑,其中被还原的元素是___,被氧化的元素是___。
(2)在反应MnO2+4HCl(浓)![]() MnCl2+C12↑+2H2O中,当有0.2mol电子转移时,产生氯气的体积(标准状况)是___;被氧化的HCl的物质的量为___。
MnCl2+C12↑+2H2O中,当有0.2mol电子转移时,产生氯气的体积(标准状况)是___;被氧化的HCl的物质的量为___。
(3)在一定条件下,RO3n-和I-发生反应的离子方程式如下:RO3n-+6I-+6H+=R-+3I2+3H2O。该反应中还原剂为___,RO3n-中R元素的化合价是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com