
【题目】(1)黑火药爆炸时发生反应:2KNO3+S+3C=K2S+N2↑+3CO2↑,其中被还原的元素是___,被氧化的元素是___。
(2)在反应MnO2+4HCl(浓)![]() MnCl2+C12↑+2H2O中,当有0.2mol电子转移时,产生氯气的体积(标准状况)是___;被氧化的HCl的物质的量为___。
MnCl2+C12↑+2H2O中,当有0.2mol电子转移时,产生氯气的体积(标准状况)是___;被氧化的HCl的物质的量为___。
(3)在一定条件下,RO3n-和I-发生反应的离子方程式如下:RO3n-+6I-+6H+=R-+3I2+3H2O。该反应中还原剂为___,RO3n-中R元素的化合价是___。
【答案】N、S C 2.24L 0.2mol I- +5
【解析】
(1)由化学方程式可知,反应中C元素化合价升高被氧化, N、S元素的化合价降低被还原;
(2)由化学方程式可知,反应中转移电子2mol时,生成的氯气物质的量为1mol;
(3)由方程式可知,反应中碘元素化合价升高被氧化,依据电荷守恒和化合价代数和为零计算可得。
(1)由化学方程式可知,反应中C元素化合价升高被氧化,C是还原剂,N、S元素的化合价降低被还原,KNO3和S是氧化剂,故答案为:N、S;C;
(2)由化学方程式可知,反应中转移电子2mol时,生成的氯气物质的量为1mol,当有0.2mol电子转移时,生成的氯气物质的量为0.1mol,体积为0.1mol×22.4L/mol=2.24L,故答案为:2.24;
(3)由方程式可知,反应中碘元素化合价升高被氧化,I-为还原剂;根据离子方程式遵循电荷守恒可知:(-n)+(-6)+6=-1,可知n=1,根据RO3n-离子化合价代数和关系:(x-2×3)=-1(设R的化合价为x),可知x=+5,故答案为:I-;+5。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】炼铁的反应原理为:Fe2O3+3CO![]() 3CO2+2Fe,当有2molFe生成时。下列说法中,错误的是( )
3CO2+2Fe,当有2molFe生成时。下列说法中,错误的是( )
A.参加反应的Fe2O3和CO物质的量分别为1mol、3mol
B.将生成67.2L标准状况下的CO2气体
C.参加反应的Fe2O3的质量为160g
D.参加反应的Fe2O3、CO与生成CO2的体积比为1:3:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将3molA气体和1molB气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g),请填写下列空白:
xC(g),请填写下列空白:
(1)反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为_______;x为______。
(2)若反应经2min达到平衡,平衡时C的浓度______0.8mol/(填大于,小于或等于”)
(3)若已知达平衡时,该容器内混合气体总压强为P,混合气体起始压强为P0.请用P0、P来表示达平衡时反应物A的转化率a(A)为______%
(4)能够说明该反应达到平衡的标志是__________。
A .容器内混合气体的密度保持不变
B. v(A)=3v(B)
C .A、B的浓度之比为3:1
D .单位时间内消耗3n molA的同时生成n molB
E.体系的温度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,所选装置不合理的是( )

A.粗盐提纯,选①和②
B.用CCl4提取碘水中的碘,选③
C.用FeCl2溶液吸收Cl2,选⑤
D.分离饱和Na2CO3溶液和CH3COOC2H5(难溶于水),选④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某气态氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL则该R摩尔质量为___。
(2)已知CO、SO2的混合气体质量共18.4g,标准状况下体积为8.96L,则可推知该混合气体中CO的物质的量分数为____,混合气体的平均相对分子质量为____。
(3)同温同压下,SO2与氢气的密度之比为____;若体积相同时,两种气体的质量比为____。
(4)质量比为51∶28的NH3、CO所含质子数之比为____。
(5)标准状况下,aL气体X2和bL气体Y2恰好完全反应生成cL气体Z,若2a=6b=3c,则Z的化学式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,利用培养皿进行实验。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。
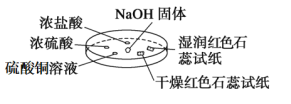
下表中对实验现象所做的解释不正确的是( )
选项 | A | B | C | D |
实验 现象 | 浓盐酸附近产生白烟 | 浓硫酸附近无明显现象 | 干燥红色石蕊试纸不变色,湿润红色石蕊试纸变蓝 | 硫酸铜溶液变浑浊 |
解释 | NH3与HCl反应产生了NH4Cl固体 | NH3与浓硫酸不发生反应 | NH3与水反应生成了NH3·H2O,电离出OH-使红色石蕊试纸变蓝 | 生成Cu(OH)2沉淀 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列说法正确的是
A.将pH均为a的氢氧化钠溶液和氨水分别加水稀释100倍,pH变为b和c,则a、b、c的大小关系是:a>b>c
B.KNO3溶液和CH3OOONH4溶液pH均为7,但两溶液中水的电离程度不相同
C.5.0×10-3 mol·L-1KHA溶液的pH=3.75,该溶液中c(A2-)<c(H2A)
D.己知某分散系中存在:M(OH)2(s)![]() M2+(aq)+2OH-(aq),K=a,c(M2+)=b mol·L-1时,溶液的pH等于
M2+(aq)+2OH-(aq),K=a,c(M2+)=b mol·L-1时,溶液的pH等于![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关于溶液和胶体的说法正确的是 ( )
A.常温下,向FeCl3溶液滴加NaOH溶液至有红褐色小颗粒生成即可制得![]() 胶体
胶体
B.溶液是均一稳定的,胶体是介稳体系,所以人的肉眼就可以区分开来
C.在![]() 胶体中,逐滴加入稀硫酸至过量,先产生红褐色沉淀后又消失
胶体中,逐滴加入稀硫酸至过量,先产生红褐色沉淀后又消失
D.明矾水解时产生具有吸附性的胶体粒子,可作漂白剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com