
【题目】一定温度下,将3molA气体和1molB气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g),请填写下列空白:
xC(g),请填写下列空白:
(1)反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为_______;x为______。
(2)若反应经2min达到平衡,平衡时C的浓度______0.8mol/(填大于,小于或等于”)
(3)若已知达平衡时,该容器内混合气体总压强为P,混合气体起始压强为P0.请用P0、P来表示达平衡时反应物A的转化率a(A)为______%
(4)能够说明该反应达到平衡的标志是__________。
A .容器内混合气体的密度保持不变
B. v(A)=3v(B)
C .A、B的浓度之比为3:1
D .单位时间内消耗3n molA的同时生成n molB
E.体系的温度不再变化
【答案】0.2mol·L-1·min-1 2 小于 ![]() D
D
【解析】
(1)直接利用浓度来列三段式,将x当已知来用;
(2)因从反应开始投料,所以正向反应速率越来越小;
(3)利用在相同的温度和体积下,气体的压强之比等于物质的量之比列式计算;
(4)利用“正、逆反应速率相等”和“变量不变”进行分析判断;
(1)利用三段式法进行计算:
3A(g) + B(g) ![]() xC(g)
xC(g)
起始c(mol/L) 1.5 0.5 0
转化(mol/L) 0.6 0.2 0.2x
1min后(mol/L) 0.9 0.3 0.2x
1min内,B的平均反应速率为:![]() ,且据题给数据可知:0.2x=0.4mol/L,解得x=2;
,且据题给数据可知:0.2x=0.4mol/L,解得x=2;
(2) 因为从反应物开始投料,所以随着反应的进行,正反应速率不断减慢,同样是历时1min生成的C的量要比前1min少。由题给数据知,反应进行1min时,C的浓度为0.4mol/L,若反应继续进行至达到平衡再需1分钟,则平衡时C的浓度必小于0.8mol/L;
(3)设达到平衡时。转化的B为nmol,则
3A(g)+B(g) ![]() 2C(g)
2C(g)
起始(mol) 3 1 0
转化(mol) 3n n 2n
1min后(mol) 3-3n 1-n 2n
根据相同条件下,气体的压强之比等于其物质的量之比,即:![]() ,所以
,所以![]() ,则A的转化率为:
,则A的转化率为:![]() ;
;
(4)A.因反应物和生成物均为气体,且容器的体积不变,所以气体的密度始终不变,所以气体密度不变不能作为平衡建立的判据,A项错误;
B.没有标示出用A、B表达的是正反应速率还是逆反应速率,所以无法依此比例判断是否达到平衡,B项错误;
C.平衡时是浓度不变,不是相等,也不是成比例,C项错误;
D.将生成的nmolB换算成生成3nmolA可以明显发现,单位时间内消耗3nmolA同时生成3nmolA,生成速率等于消耗速率,显然已达平衡,D项正确;
E.因为恒温,所以温度始终不变,温度不变就不能作为该反应达平衡的判断依据,E项错误。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】加热 42g NaHCO3 和 Na2CO3 固体混合物,至没有气体放出时,剩余的固体质量是 35.8 g。那么原固体混合物中Na 2CO3 的质量是
A. 25.2g B. 16.8 g C. 10.6 g D. 24.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的含氧衍生物的球棍模型如图所示(图中球与球之间连线代表化学键单键或双键)。下列关于该有机物的说法正确的是( )
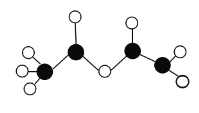
A.该有机物的名称是乙酸乙酯
B.该有机物能使Br2的CCl4或酸性高锰酸钾褪色,原理相同
C.该有机物能发生取代反应、氧化反应和消去反应
D.该有机物的同分异构体中能与NaHCO3反应产生气体的链状结构只有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。下列说法不正确的是

A. 电流由O2所在的铂电极经外电路流向另一电极
B. O2所在的铂电极处发生还原反应
C. 该电池的负极反应式为:CH3CH2OH+3H2O-12e-="=" 2CO2↑+12H+
D. 微处理器通过检测电流大小而计算出被测气体中酒精的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3为黑棕色固体,无水氯化铁在300℃以上升华,遇潮湿空气极易潮解。
(1)甲组同学拟用下列装置制取纯净干燥的氯气。
①装置B的作用是_________
②装置A中发生反应时消耗的氧化剂和还原剂的物质的量之比为__________
(2)乙组同学选用甲组实验中的装置ABC和下列装置制取FeCl3
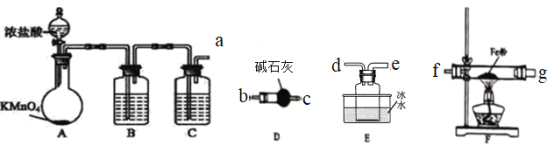
①乙组同学的实验装置中,依次连接的合理顺序为:a→_____→_____→_____→_____→_____→_____
②连好装置,检查装置的气密性,先打开装置A中___________(填仪器的名称)的活塞,直到______再点燃装置F处的酒精灯,目的是_______
③装置D的作用有_______
(3)实验结束后,取少量F中的固体加水溶解,欲对所得产物FeCl3中是否含有FeCl2进行检测,所需试剂是_______
a.KSCN b.H2O2 c.K3[Fe(CN)6] d. .K4[Fe(CN)6]
经检测发现溶液中含有Fe2+,丙同学认为所得产物FeCl3中一定含有FeCl2,丁同学认为不一定,理由是_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用。右图表示一个电解池, 装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
⑴(8分)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
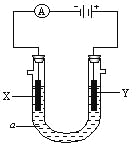
①电解池中X极上的电极反应式是 。
在X极附近观察到的现象是 。
②Y电极上的电极反应式是 ,
检验该电极反应产物的方法是 。
⑵(6分)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式是
②Y电极的材料是 ,电极反应式是
(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铁泥(主要成分为Fe2O3、FeO和少量Fe)制备纳米Fe3O4,的流程示意图如下:

下列叙述错误的是
A. 为提高步骤①的反应速率,可采取搅拌、升温等措施
B. 步骤②中,主要反应的离子方程式是2Fe3++Fe=3Fe2+
C. 步骤④中,反应完成后剩余的H2O2无需除去
D. 步骤⑤中,“分离”包含的操作有过滤、洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)黑火药爆炸时发生反应:2KNO3+S+3C=K2S+N2↑+3CO2↑,其中被还原的元素是___,被氧化的元素是___。
(2)在反应MnO2+4HCl(浓)![]() MnCl2+C12↑+2H2O中,当有0.2mol电子转移时,产生氯气的体积(标准状况)是___;被氧化的HCl的物质的量为___。
MnCl2+C12↑+2H2O中,当有0.2mol电子转移时,产生氯气的体积(标准状况)是___;被氧化的HCl的物质的量为___。
(3)在一定条件下,RO3n-和I-发生反应的离子方程式如下:RO3n-+6I-+6H+=R-+3I2+3H2O。该反应中还原剂为___,RO3n-中R元素的化合价是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把5.1 g铝镁合金的粉末放入100 mL某盐酸中,恰好完全反应,标准状况下收集到5.6 L H2。试计算(注意:无计算过程不给分):
(1)该盐酸的物质的量浓度是多少?_____________
(2)该合金中铝的质量为多少克?_____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com