
 2NH3��g������H=-92.4kJ?mol-1����ͼ1�������ֲ�ͬʵ��������ģ�⻯����������ʵ�������N2��ʱ��仯ʾ��ͼ��
2NH3��g������H=-92.4kJ?mol-1����ͼ1�������ֲ�ͬʵ��������ģ�⻯����������ʵ�������N2��ʱ��仯ʾ��ͼ��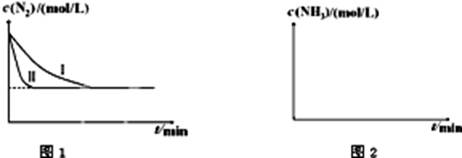
 ����4��C(Na+)>C(HCO3-)>C(CO32-)>C(OH-)>C(H+) ��
����4��C(Na+)>C(HCO3-)>C(CO32-)>C(OH-)>C(H+) �� ��
��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��v��A��=0.5mol/��L?min�� | B��v��B��=0.05mol/��L?min�� |
| C��v��C��=0.9mol/��L?min�� | D��v��D��=1.0mol/��L?min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢ڢ� | B���٢ۢ� | C���٢ڢۢ� | D���٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢ޢ� | B���ۢݢ� | C���ۢߢ� | D���ۢܢޢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��20 mL,2 mol/L | B��20 mL,3 mol/L | C��10 mL,5 mol/L | D��10 mL,3 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������¡�����ͭ����ͭƬ�Ļ�ԭ��ǿ����Ӧʱ��Ӧ���ʿ� |
| B��������ͭ��������ϸС����ѧ��Ӧʱ�Ӵ�������Է�Ӧ���ʿ� |
| C��������ͭ����ͭ��ͬ�������� |
| D�������¡�����ͭ����ͭƬ���õ��ӣ���Ӧʱ��Ӧ���ʿ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
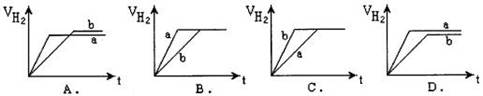
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢ۢ� | B���٢ڢ� | C���٢ڢۢ� | D���٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ������������ʵ�� �����Һ���������� | A | B | C | D | E | F |
| 4 mol��L-1 H2SO4��Һ/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| ����CuSO4��Һ/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com