
| A.吸热反应 | B.放热反应 | C.放出832 kJ热量 | D.吸收183 kJ热量 |
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源:不详 题型:计算题


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
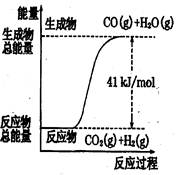
| A.CO+H2O=CO2+H2;△H="+41" kJ/mol |
| B.CO(g)+H2O(g)=CO2(g)+H2(g);;△H= ?41 kJ/mol |
| C.CO2(g)+H2(g)=CO(g)+H2O(g);△H="+41" kJ/mol |
| D.CO2(g)+H2(g) =CO(g)+H2O(g);△H=?41 kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.+184.6kJ·mol-1 | B.―92.3kJ·mol-1 |
| C.+92.3kJ | D.+92.3kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH1=-99 kJ·mol-1
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH1=-99 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NO(g) DH=a kJ·mol-1的平衡常数K如下表:
2NO(g) DH=a kJ·mol-1的平衡常数K如下表:| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
 2NO(g)达到平衡时N2的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
2NO(g)达到平衡时N2的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.4Q1+0.5Q2 | B.4Q1+Q2+10Q3 | C.4Q1+2Q2 | D.4Q1+0.5Q2+9Q3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com