
【题目】常温常压下,22.4氢气的物质的量是
A. 6.02×1023 B. 1mol C. 大于1mol D. 小于1mol
科目:高中化学 来源: 题型:
【题目】
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ/mol
N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
写出氨气催化氧化生成一氧化氮气体和水蒸气的热化学反应方程式。
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g) ![]() 2NH3(g)反应的影响,实验结果如图所示:(图中T表示温度,n表示物质的量)
2NH3(g)反应的影响,实验结果如图所示:(图中T表示温度,n表示物质的量)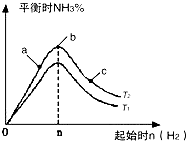
①图象中T2和T1的关系是:T2T1(填“高于”、“低于”、“等于”、“无法确定”).
②若比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是(填字母).
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g) ![]() 4NO2(g) + O2(g).△H﹥0,下表为反应在T1温度下的部分实验数据:
4NO2(g) + O2(g).△H﹥0,下表为反应在T1温度下的部分实验数据:
| 0 | 500 | 1000 |
| 5.00 | 3.52 | 2.48 |
①500s内NO2的平均生成速率为。
②该反应的化学平衡常数表达式为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化还原反应的叙述中正确的是
A. 一种元素被氧化,肯定另一种元素被还原
B. 反应中不一定所有元素的化合价都发生变化
C. 某元素由化合物变为单质,则该元素一定被还原
D. 氧化还原反应中一定有得氧或失氧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学家屠呦呦因创制新型抗疟药﹣﹣青蒿素和双氢青蒿素获得2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素的结构式如图.从青蒿中提取青蒿素主要采用有机溶剂提取的方法.下列有关说法不正确的是( ) 
A.青蒿素的分子式为C15H22O5
B.青蒿素通过还原反应可制得双氢青蒿素
C.青蒿素有青蒿的芳香气味,是芳香族化合物
D.用有机溶剂乙醚从青蒿中提取青蒿素,主要采用萃取的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.摩尔既是物质的量的单位,又是粒子的数量单位
B.2 mol O2的摩尔质量是64 g/mol
C.摩尔质量在数值上与1mol该物质的质量相等
D.1 mol SO2中含有2 mol O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为元素周期表的一部分,其中X、Y、Z、W为四种短周期元素。Z元素原子核外K层与M层上的电子数相等。下列说法中正确的是( )
![]()
A. Y元素的最高价氧化物对应的水化物的化学式为H3YO4
B. Y的最简单气态氢化物的水溶液显弱碱性
C. 原子半径由小到大的顺序为X<Z<Y<W
D. X、Z两种元素的氧化物中所含化学键的类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列我国科学家中,为化学理论做出重大贡献的是
A. 徐光宪(创立稀土萃取理论) B. 屠呦呦(创制新的抗疟疾药)
C. 袁隆平(培育杂交水稻) D. 钱学森
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com