
| A、无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其c(H+)?c(OH-)=1×10-14 |
| B、c(H+)等于1×10-7mol?L-1的溶液一定是中性溶液 |
| C、0.2 mol?L-1CH3COOH溶液中的c(H+)是0.1 mol?L-1CH3COOH溶液中的c(H+)的2倍 |
| D、任何浓度的溶液都可以用pH来表示其酸性的强弱 |


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
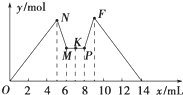 如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图.根据图示判断,下列结论中不正确的是( )
如图所示是向MgCl2和AlCl3的混合溶液中加入一定量NaOH溶液,紧接着再加入一定量稀盐酸,生成沉淀的物质的量y与加入溶液的体积x的关系图.根据图示判断,下列结论中不正确的是( )| A、N点时溶液中的溶质只有NaCl |
| B、M点之前加入的是NaOH溶液,M点之后加入的是盐酸 |
| C、c(NaOH)=c(HCl) |
| D、原混合溶液中c(MgCl2):c(AlCl3)=1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②④ | C、③⑤ | D、②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol H2SO4与1 mol Ba(OH)2完全中和所放出的热量为中和热 |
| B、由C(石墨)→C(金刚石)△H=+119 kJ?mol-1可知,石墨比金刚石稳定 |
| C、在101 kPa时,2gH2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ?mol-1 |
| D、在101 kPa,298 K条件下,1 mol S和2 mol S的燃烧产生的热量不相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定条件下,水由气态变为液态 |
| B、2H2(g)+O2(g)═2H2O(g) |
| C、HCl(g)+NH3(g)═NH4Cl(s) |
| D、NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向沸水中滴加饱和氯化铁溶液可制得氢氧化铁胶体 |
| B、利用滤纸可以分离胶体与溶液 |
| C、胶体与溶液的本质区别在于能否发生丁达尔效应 |
| D、蔗糖、淀粉、蛋白质的水溶液均能产生丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2 | B、2:1 |
| C、3:2 | D、2:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com