
| A、①③ | B、②④ | C、③⑤ | D、②⑤ |
科目:高中化学 来源: 题型:
| A、①② | B、①⑤ | C、②③④ | D、④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无色溶液:Ca2+、H+、Cl-、HSO3 - | ||
| B、能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3 - | ||
| C、Na2CO3溶液:K+、Fe3+、SO42-、NO3 - | ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
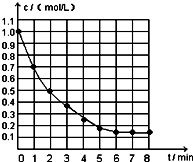 如图表示反应X(g)═4Y(g)+Z(g)△H<0,在某温度时X的浓度
如图表示反应X(g)═4Y(g)+Z(g)△H<0,在某温度时X的浓度| A、该反应的过程是熵减小的过程 |
| B、若降低温度,v正减小,v逆增大 |
| C、第6min后,反应就停止了 |
| D、X在第一分钟和第二分钟内的平均反应速率之比是3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、此反应物的总能量低于生成物的总能量 |
| B、反应达到平衡后,3ν正(NH3)=2ν逆(H2O) |
| C、其它条件不变,温度越高,氨的转化率越高 |
| D、寻找合适的催化剂是加快反应速率的有效措施 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、推进小火力发电站的兴建,缓解地方用电困难,促进地方经济的发展 |
| B、推广“低碳经济”,减少温室气体的排放 |
| C、推广“绿色自由”计划,吸收空气中的CO2并利用廉价能源合成汽油 |
| D、利用晶体硅制作的太阳能电池可将太阳能直接转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴入甲基橙显红色的溶液中:K+、Al3+、I-、ClO-、NO3- |
| B、常温下,某溶液pH=1的溶液中含有:NO3-、NH4+、Fe2+、SO42- |
| C、常温下,c(H+)/c(OH-)=1×10-12的溶液:K+、AlO2-、CO32-、Na+ |
| D、0.1mol/LFeCl3溶液中:Fe2+、NH4+、SCN-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其c(H+)?c(OH-)=1×10-14 |
| B、c(H+)等于1×10-7mol?L-1的溶液一定是中性溶液 |
| C、0.2 mol?L-1CH3COOH溶液中的c(H+)是0.1 mol?L-1CH3COOH溶液中的c(H+)的2倍 |
| D、任何浓度的溶液都可以用pH来表示其酸性的强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属阳离子被还原不一定得到金属单质 |
| B、失电子难的原子获得电子的能力一定强 |
| C、得到电子越多的氧化剂,其氧化性就越强 |
| D、阳离子只有氧化性,阴离子只有还原性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com