
【题目】某金属加工厂排放的污水中含有CuSO4、ZnSO4、FeSO4,某研究小组利用该污水回收工业重要原料硫酸锌和有关金属,其流程如下:
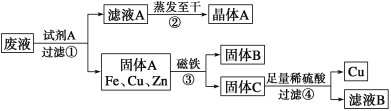
请回答下列问题:
(1)下列说法正确的是________。
A.该工艺流程中发生了3个置换反应
B.CuSO4与Mg(OH)2发生复分解反应可得Cu(OH)2
C.步骤①②③④都包含化学变化
(2)写出步骤①发生反应的离子方程式:__________________、_________________
(3)步骤④中加入足量稀硫酸的目的是________________
(4)滤液B含有的分散质为____________、___________ .
【答案】A Zn+Cu2+===Cu+Zn2+ Zn+Fe2+===Fe+Zn2+ 使Zn完全溶解 ZnSO4 H2SO4
【解析】
因金属的活泼性Zn>Fe>Cu,由废水中含有CuSO4,ZnSO4、FeSO4,则加入锌粉能发生锌与硫酸亚铁、锌与硫酸铜的反应,其反应分别为Zn+FeSO4═ZnSO4+Fe、Zn+CuSO4═ZnSO4+Cu,滤液A为ZnSO4溶液,蒸发得到硫酸锌晶体,固体A经磁铁将铁分离开,固体C中含有锌与铜,加足量稀硫酸时,铜并不反应经过滤可得到,而锌与稀硫酸发生化学反应,其反应为Zn+H2SO4═ZnSO4+H2↑,加入适量稀硫酸的目的是使锌完全转化为ZnSO4,以此解答该题。
(1)A.由以上分析可知发生的置换反应有Zn+FeSO4═ZnSO4+Fe、Zn+CuSO4═ZnSO4+Cu、Zn+H2SO4═ZnSO4+H2↑,正确;B.CuSO4与MgCl2不能发生复分解反应,错误;C.步骤②为物理过程,不涉及化学变化,错误;选A;
(2)步骤①发生反应为Zn+FeSO4═ZnSO4+Fe、Zn+CuSO4═ZnSO4+Cu,离子方程式为Zn+Cu2+=Cu+Zn2+、Zn+Fe2+=Zn2++Fe;
(3)加足量稀硫酸时,铜并不反应经过滤可得到,而锌与稀硫酸发生化学反应,其反应为Zn+H2SO4═ZnSO4+H2↑,加入适量稀硫酸的目的是使锌完全转化为ZnSO4,使Zn完全溶解;
(4) 固体C中含有锌与铜,加足量稀硫酸时,铜并不反应经过滤可得到,而锌与稀硫酸发生化学反应,其反应为Zn+H2SO4═ZnSO4+H2↑,加入适量稀硫酸的目的是使锌完全转化为ZnSO4,滤液B含有的分散质为ZnSO4和过量的H2SO4。


科目:高中化学 来源: 题型:
【题目】已知反应A2(g)+2B2(g)![]() 2AB2(g) ΔH<0,下列说法正确的是
2AB2(g) ΔH<0,下列说法正确的是
A. 达平衡后降低温度,混合气体平均相对分子质量减小
B. 使用催化剂能加快反应速率,缩短达平衡所需的时间且提高A2的转化率
C. 达平衡后升高温度并增大压强,有可能每一组分的百分含量都不改变,但平衡常数一定发生改变
D. 达平衡后,降低温度或减小压强都有利于该平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应)。请回答下列问题:
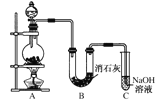
(1)A为实验室制氯气的发生装置,反应化学方程式为_________________________;某学生用12 mol·L-1的浓盐酸100 mL和足量的MnO2反应制Cl2,实际得到的Cl2________6.72 L(填“<”、“>”或“=”)。
(2)漂白粉将在U形管中产生,其化学方程式是_________________________________。
(3)此实验所得漂白粉的有效成分偏低。该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应:
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是________________。
②Cl2中含HCl,会发生反应2HCl+Ca(OH)2===CaCl2+2H2O,为避免此副反应的发生,可将装置作何改进______________________________。
(4) C装置的作用是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为探究AgNO3溶液和不同类型盐溶液反应的多样性,设计如图实验:已知:AgSCN为白色难溶物。下列说法不正确的是( )

A.①中的白色沉淀是![]()
B.向①的试管中滴加![]() KI溶液,有黄色沉淀生成证明存在
KI溶液,有黄色沉淀生成证明存在![]()
![]()
![]()
C.②中发生了氧化还原反应
D.对于②中红色褪去的原因可能与平衡移动原理有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X为中学化学中一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的氧化物可作耐火材料,可用它来制造耐火坩埚和耐高温试验仪器;H为气体单质,D为无色气体,D在空气中会出现红棕色,各物质的转化关系如下图,(部分反应产物已略去).
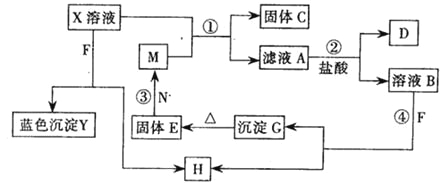
请回答下列问题;
(1)E的化学式为_____________________
(2)将M丝插入盛有X溶液的试管中,反应一段时间后的现象是:_______________________
(3)在反应①②③④中属于置换反应的是_________________(填序号).
(4)反应②的离子方程式为___________________________________
(5)用石墨作电极电解500mL X溶液,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;电解一段时间后,取出A电极,洗涤、干燥、称量,电极增重1. 6g.请回答下列问题:
①写出电解时的阳极反应式_______________________
②电解后溶液的pH为________________________假设电解前后溶液体积不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】基本知识填空
(1)在一定条件下,当一个可逆反应的_____与____相等时,反应物的浓度与生成物的浓度不再改变,即达到化学平衡状态。
(2)化学平衡状态的特征:_____、____、_____、_____、_____。
(3)对于可逆化学反应mA+nBpC+qD在一定温度下达到化学平衡时,其平衡常数表达式为:______。
(4)强电解质包括的范围:____、____、____。弱电解质包括的范围:____、_____、____、_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素C是一种水溶性维生素(其水溶液呈酸性),它的化学式是C6H8O6,人体缺乏这样的维生素能得坏血症,所以维生素C又称抗坏血酸。在新鲜的水果、蔬菜、乳制品中都富含维生素C,例如新鲜橙汁中维生素C的含量在500mg/L左右。某校课外活动小组测定了某牌子的软包装橙汁中维生素C的含量,下面是测定实验分析报告。(请填写有关空白)
(一)测定目的:测定××牌软包装橙汁中维生素C的含量。
(二)测定原理:C6H8O6+I2 →C6H6O6+2H++2I―
(三)实验用品及试剂
(1)仪器和用品(自选,略)
(2)试剂:指示剂___(填名称),浓度为7.50×10-3mol·L-1的I2标准溶液、蒸馏水等。
(四)实验过程
(1)洗涤仪器,检查滴定管是否漏液,润洗后装好标准碘溶液待用。
(2)用___(填仪器名称)向锥形瓶中移入20.00mL待测橙汁,滴入2滴指示剂。
(3)用左手控制滴定管的___(填部位),右手摇动锥形瓶,眼睛注视___,直到滴定终点。滴定至终点时的现象是___。
(五)数据记录与处理(请在下面设计并画出数据记录和数据处理的表格,不必填数据)。__

若经数据处理,滴定中消耗标准碘溶液的体积是15.00mL,则此橙汁中维生素C的含量是___mg/L。
(六)问题讨论:
(1)滴定时能否剧烈摇动锥形瓶?为什么?_____
(2)从分析数据看,此软包装橙汁是否是纯天然橙汁?___(填“是”或“不是”或“可能是”)。制造商最可能采取的做法是____(填编号):
A.加水稀释天然橙汁 B.橙汁已被浓缩 C.将维生素C作为添加剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨的催化氧化是工业制硝酸的重要反应:4NH3+5O2![]() 4NO+6H2O,对于该反应判断正确的是
4NO+6H2O,对于该反应判断正确的是
A. 氧气被还原B. 该反应是置换反应
C. 氨气是氧化剂D. 若有17 g氨参加反应,反应中转移10 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知Ca2+、OH-、![]() 的摩尔电导率分别为0.60、1.98、0.45据此可判断,向饱和的澄清石灰水中通入过量的二氧化碳,溶液导电能力随二氧化碳通入量的变化趋势正确的是( )
的摩尔电导率分别为0.60、1.98、0.45据此可判断,向饱和的澄清石灰水中通入过量的二氧化碳,溶液导电能力随二氧化碳通入量的变化趋势正确的是( )
A. B.
B. C.
C. D.
D.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com