
【题目】某化学实验小组欲选用下列装置和药品制取纯净乙炔并进行乙炔性质的探究,试回答下列问题:
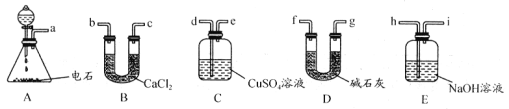
(1)A中制取乙炔的化学反应方程式为_________
(2)制乙炔时,旋开分液漏斗的活塞,使饱和食盐水缓慢滴下的原因是_______
(3)用电石制的乙炔中常含有 H2S、PH3 等杂质,除去杂质应选用____ (填序号,下同) 装置,气体应从____进;C 中通入含杂质的乙炔后有 Cu3P 沉淀、H3PO4 等生成,该反应化学方程式为_____________
(4)一种有机物 Y,与乙炔具有相同的最简式,其相对分子质量是 104。
①若该化合物 Y 分子的一氯代物只有一种且不能使溴水褪色,则 Y 的结构简式为________(用 “键线式”表示)。它的二氯代物有_____种同分异构体。
②前些年,化学家合作合成了一种新型炸药,该炸药分子可以看成是 Y 分子的四硝基(-NO2)取代物,分子结构非常对称,在核磁共振氢谱上观察到氢原子给出的峰只有一个,试画出其结构简式____.
【答案】CaC2+2H2O→C2H2↑+Ca(OH)2 控制反应速率,使产生的气流稳定,避免产生的泡沫进入导管 C d 24CuSO4+11PH3+12H2O=8Cu3P↓+3H3PO4+24H2SO4 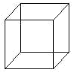 3
3 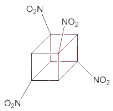
【解析】
(1)A中用电石与饱和食盐水制取乙炔,化学反应方程式为CaC2+2H2O→C2H2↑+Ca(OH)2 ;
(2)制乙炔时,由于电石与水反应很剧烈,所以必须控制反应速率,使饱和食盐水缓慢滴下,所以答案为控制反应速率,使产生的气流稳定,避免产生的泡沫进入导管;
(3) H2S、PH3等具有还原性可以利用CuSO4除去,除杂时应是长口进,短口出。根据题干信息知,C中是杂质PH3与CuSO4发生的氧化还原反应,根据得失电子守恒配平得:24CuSO4+11PH3+12H2O=8Cu3P↓+3H3PO4+24H2SO4,故答案为:C;d;24CuSO4+11PH3+12H2O=8Cu3P↓+3H3PO4+24H2SO4;
(4)有机物Y与乙炔最简式相同,则Y分子式为CnHn,相对分子质量是104,则n=8,Y为C8H8;
①若该化合物Y分子的一氯代物只有一种且不能使溴水褪色,则Y中不含碳碳双键,则Y的结构简式为: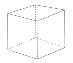 ;两个氯原子可以在相邻碳原子上,也可以在同一个面的对角线位置,还有一种是经过体心的对角线位置,所以它的二氯代物有3种同分异构体;
;两个氯原子可以在相邻碳原子上,也可以在同一个面的对角线位置,还有一种是经过体心的对角线位置,所以它的二氯代物有3种同分异构体;
②根据题干信息,分子结构非常对称,则硝基立方体的不相邻的4个顶点,核磁共振氢谱上观察到氢原子给出的峰只有一个,则其结构简式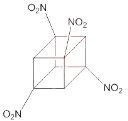 。
。


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】2009年《化学教育》期刊封面刊载如图所示的有机物M(只含C、H、O)的球棍模型图。不同大小、颜色的小球代表不同的原子,小球之间的“棍”表示共价键,既可以表示三键,也可以表示双键,还可以表示单键。下列有关M的推断正确的是( )
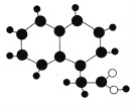
A. M的分子式为C12H12O2
B. M与足量氢气在一定条件下反应的产物的环上一氯代物有7种
C. M能发生中和反应、取代反应
D. 一个M分子最多有11个原子共面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叠氮化钠(NaN3)是一种无色晶体,常见的两种制备方法为2NaNH2+N2O==NaN3+NaOH+NH3,3NaNH2+NaNO3==NaN3+3NaOH+NH3↑。
回答下列问题:
(1)氮元素所在的周期中,电负性最大的元素是________,第一电离能最小的元素是_______。
(2)基态氮原子的L层电子排布图为_________________。
(3)与N3-互为等电子体的分子为_________(写出一种)。依据价层电子对互斥理论,NO3-的空间构型是______________,其中心原子杂化类型是__________。
(4)叠氮化钠中不含有的化学键类型有_____________。
A.离子键 B.极性共价键 C.σ键 D.π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要“打赢蓝天保卫战”,意味着对污染防治比过去要求更高。某种利用垃圾渗透液实现发电、环保二位一体相结合的装置示意图如图,当该装置工作时,下列说法正确的是( )
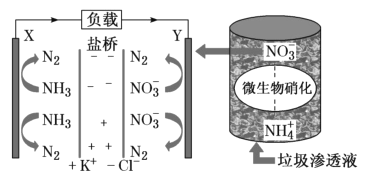
A.盐桥中K+向X极移动
B.电路中流过7.5mol电子时,共产生标准状况下N2的体积为44.8L
C.该装置实现了将电能转化为化学能
D.Y极发生的反应为2NO3--10e-+6H2O=N2↑+12OH-,周围pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是中学化学中常见的物质,且A、B、C均含有同一种元素,在一定条件下相互转化关系如下图所示(部分产物已略去)。请回答:
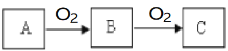
(1)若B是无色气体,C是红棕色气体。
① A、B、C所含相同元素在元素周期表中的位置是______。
② 下列说法正确的是______(填字母)。
a.常温下,A为无色气体
b.A、B、C中所含相同元素的化合价依次升高
c.C与水反应只做还原剂。
③若A是化合物,写出由A氧化生产B的化学方程式__________________。
(2)若B是一种有刺激性气味的有毒气体,C与水反应生成硫酸
① A、B、C所含相同元素的原子结构示意图是______。
② 下列说法不正确的是______(填字母)。
a.A一定是黄色晶体
b.可以用上述转化关系制备硫酸
c.B与水反应做还原剂。
③C的水溶液与氢氧化钠的反应为______________(填吸热或放热)反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na3OCl是一种良好的离子导体,具有反钙钛矿晶体结构。
回答下列问题:
(1)基态Ti原子4s轨道上的一个电子激发到4p轨道上形成激发态,写出该激发态价层电子排布式__。第三电离能:Ca__Ti(填“大于”或“小于”)。
(2)由O、Cl元素可组成不同的单质和化合物,其中Cl2O2能破坏臭氧层。
①Cl2O2的沸点比H2O2低,原因是__。
②O3分子的中心原子杂化类型为___;与O3互为等电子体的是__(任意写一种)。
(3)Na3OCl可由以下方法制得:2Na+2NaOH+2NaCl![]() 2Na3OCl+H2↑,在该反应中,形成的化学键有__(填标号)。
2Na3OCl+H2↑,在该反应中,形成的化学键有__(填标号)。
A.金属键 B.离子键 C.配位键 D.极性键 E.非极性键
(4)Na3OCl晶体属于立方晶系,其晶胞结构如图所示。已知:晶胞参数为anm,密度为dgcm3。

①Na3OCl晶胞中,O位于各顶点位置,Cl位于__位置。
②用a、d表示阿伏加德罗常数的值NA=__(列计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用无机矿物资源生产部分材料的流程示意图如图:

下列说法不正确的是( )
A.石灰石、纯碱、石英都属于盐,都能与盐酸反应
B.用铝土矿制备较高纯度Al的过程中常用到NaOH溶液、CO2、冰晶石等
C.在制粗硅时,被氧化的物质与被还原的物质的物质的量之比为2:1
D.黄铜矿(CuFeS2)与O2反应产生的Cu2S、FeO均是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了更简便地制取干燥的NH3,下列方法中适合的是
A.NH4Cl与浓H2SO4混合共热,生成的气体用碱石灰进行干燥
B.N2+3H2![]() 2NH3,用烧碱进行干燥
2NH3,用烧碱进行干燥
C.加热浓氨水,气体用碱石灰干燥
D.加热NH4HCO3,气体用P2O5干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用微生物燃料电池原理,可以处理宇航员排出的粪便,同时得到电能。美国宇航局设计的方案是:用微生物中的芽孢杆菌来处理粪便产生氨气,氨气与氧气分别通入燃料电池两极,最终生成常见的无毒物质。示意图如下所示。下列说法错误的是( )
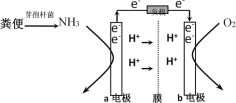
A.a电极是负极,b电极是正极
B.负极区发生的反应是2NH3 - 6e-=N2+6H+
C.正极区,每消耗标准状况下2.24 L O2,a向b电极转移0.4 mol电子
D.电池工作时电子通过由a经负载流向b电极,再穿过离子交换膜回到a电极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com