
【题目】Na3OCl是一种良好的离子导体,具有反钙钛矿晶体结构。
回答下列问题:
(1)基态Ti原子4s轨道上的一个电子激发到4p轨道上形成激发态,写出该激发态价层电子排布式__。第三电离能:Ca__Ti(填“大于”或“小于”)。
(2)由O、Cl元素可组成不同的单质和化合物,其中Cl2O2能破坏臭氧层。
①Cl2O2的沸点比H2O2低,原因是__。
②O3分子的中心原子杂化类型为___;与O3互为等电子体的是__(任意写一种)。
(3)Na3OCl可由以下方法制得:2Na+2NaOH+2NaCl![]() 2Na3OCl+H2↑,在该反应中,形成的化学键有__(填标号)。
2Na3OCl+H2↑,在该反应中,形成的化学键有__(填标号)。
A.金属键 B.离子键 C.配位键 D.极性键 E.非极性键
(4)Na3OCl晶体属于立方晶系,其晶胞结构如图所示。已知:晶胞参数为anm,密度为dgcm3。

①Na3OCl晶胞中,O位于各顶点位置,Cl位于__位置。
②用a、d表示阿伏加德罗常数的值NA=__(列计算式)。
【答案】3d24s14p1 大于 H2O2分子间存在氢键 sp2 SO2(或NO3-等) BE 体心 ![]()
【解析】
同种类型晶体的熔沸点高低取决于微粒间作用力的大小,分子间存在氢键的熔沸点高;②根据价层电子对互斥理论和杂化轨道理论分析解答;根据Na3OCl和H2存在的化学键类型判断;根据均摊法分析判断Na3OCl晶体结构中空心白球、顶点阴影球、实心黑球的数目再结合Na3OCl化学式分析判断;由密度公式ρ= 计算解答。
计算解答。
(1)基态Ti原子4s轨道上的一个电子激发到4p轨道上形成激发态,该激发态价层电子排布式3d24s14p1,Ca原子失去两个电子后恰好达到全满结构,很难失去第三个电子,第三电离能Ca较大。
(2)①同种类型晶体的熔沸点高低取决于微粒间作用力的大小,H2O2分子间存在氢键,熔沸点高;
②根据价层电子对互斥理论,O3分子的中心O原子的价层电子对为![]() ,杂化形式为sp2,O3分子为V形结构,分子中正负电荷重心不重合,为极性分子,与O3互为等电子体的是SO2(或NO3-等)。
,杂化形式为sp2,O3分子为V形结构,分子中正负电荷重心不重合,为极性分子,与O3互为等电子体的是SO2(或NO3-等)。
(3)在反应2Na+2NaOH+2NaCl![]() 2Na3OCl+H2↑中,形成的化学键有Na3OCl中Na与O、Na与Cl间的离子键,H2分子内有H与H间的非极性键,即答案为BE。
2Na3OCl+H2↑中,形成的化学键有Na3OCl中Na与O、Na与Cl间的离子键,H2分子内有H与H间的非极性键,即答案为BE。
(4)①Na3OCl晶体结构中空心白球类原子6×![]() =3、顶点阴影球类原子8×
=3、顶点阴影球类原子8×![]() =1、实心黑球类原子1×1=1,根据Na3OCl化学式,可判断钠原子应为空心白球,,氯原子应为实心黑球,处在晶体结构的体心。
=1、实心黑球类原子1×1=1,根据Na3OCl化学式,可判断钠原子应为空心白球,,氯原子应为实心黑球,处在晶体结构的体心。
②已知晶胞参数为a nm,密度为d gcm-3,则d gcm-3= =
=![]() ,解得:NA=
,解得:NA=![]() 。
。


科目:高中化学 来源: 题型:
【题目】(1)在①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,⑦(NH4)2SO4,⑧乙醇中,由极性键形成的非极性分子有_______(填序号,以下同),含有金属离子的物质是__,分子间可形成氢键的物质是________,属于离子晶体的是__,属于原子晶体的是__,①~⑤五种物质的熔点由高到低的顺序是__。
(2)A,B,C,D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500 ℃
试推断它们的晶体类型:A.__;B.__;C.__;D.__。
(3)下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:A.__;B.__;C.__D.____。
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴是一种中等活泼金属,化合价为+2 价和+3 价,其中 CoCl2易溶于水.某校同学设计实验制取(CH3COO )2Co( 乙酸钴)并验证其分解气体产物.问答下列问题:
(1)甲同学用 Co2O3 与盐酸反应制备CoCl2·4H2O其实验装置如下:
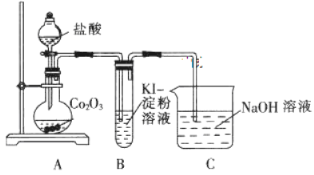
①已知 B 装置中溶液变蓝, 写出烧瓶中发生反应的离子方程式为 _____________。
②由烧瓶中的溶液制取干燥的CoCl2·4H2O,还需经过的操作有蒸发浓缩、__________、洗涤、干燥等。
(2)乙同学利用甲同学制得的CoCl2·4H2O 在醋酸氛围中制得无水(CH3COO)2Co。已知(CH3COO)2Co![]() Co3O4 +CO↑+ CO2↑+ X↑, 该同学称取一 定量的无水(CH3COO )2Co,利用下列装置检验(CH3COO )2Co分解的气体产物(实验过程中同时通入N2),并测定X 的化学式。已知PdCl2溶液可用于检验CO ,它能将CO氧化成 CO2。
Co3O4 +CO↑+ CO2↑+ X↑, 该同学称取一 定量的无水(CH3COO )2Co,利用下列装置检验(CH3COO )2Co分解的气体产物(实验过程中同时通入N2),并测定X 的化学式。已知PdCl2溶液可用于检验CO ,它能将CO氧化成 CO2。
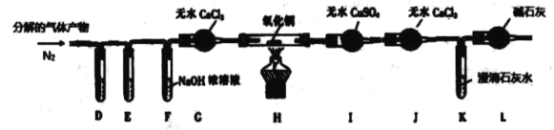
①装置D、E 是用于检验CO 和 CO2的 ,其中盛放PdCl2 溶液的是装置_____(填“D”或“E”)。
②装置F 的作用是__________; 装置L 的作用是__________。
③已知 X 为 二元化合物.假设实验中的每一步反应均完全,实验中观察到装置H 中氧化铜变红,装置I中固体变成蓝色且增重5.4g, K 中石灰水变浑浊且增重8.8g,则X的化学式为_______,写出(CH3COO )2Co 热分解的化学反应化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,体积均为25.00mL,浓度均为0.0100mo1L-1的HA、H3B溶液分别用0.0100mo1L-1NaOH溶液滴定,溶液的pH随V(NaOH)变化曲线如图所示,下列说法正确的是( )
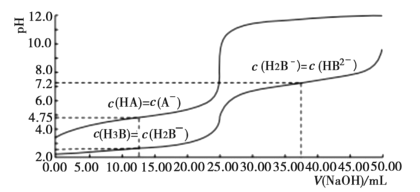
A.25℃时,0.0100mo1L-1Na2HB溶液的pH>7
B.向HA溶液中滴加NaOH溶液至中性,c(A-)<c(HA)
C.NaOH溶液滴定HA溶液应选甲基橙作指示剂
D.25℃时,H2B-离子的水解常数的数量级为10-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组欲选用下列装置和药品制取纯净乙炔并进行乙炔性质的探究,试回答下列问题:
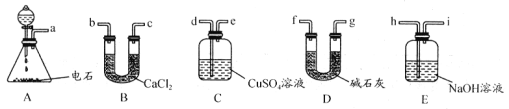
(1)A中制取乙炔的化学反应方程式为_________
(2)制乙炔时,旋开分液漏斗的活塞,使饱和食盐水缓慢滴下的原因是_______
(3)用电石制的乙炔中常含有 H2S、PH3 等杂质,除去杂质应选用____ (填序号,下同) 装置,气体应从____进;C 中通入含杂质的乙炔后有 Cu3P 沉淀、H3PO4 等生成,该反应化学方程式为_____________
(4)一种有机物 Y,与乙炔具有相同的最简式,其相对分子质量是 104。
①若该化合物 Y 分子的一氯代物只有一种且不能使溴水褪色,则 Y 的结构简式为________(用 “键线式”表示)。它的二氯代物有_____种同分异构体。
②前些年,化学家合作合成了一种新型炸药,该炸药分子可以看成是 Y 分子的四硝基(-NO2)取代物,分子结构非常对称,在核磁共振氢谱上观察到氢原子给出的峰只有一个,试画出其结构简式____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列物质:①He;②N2;③H2O2;④CaO;⑤NaHCO3;⑥NH4Cl;⑦Na2O2;⑧SiO2;⑨MgCl2;⑩KOH。请用序号填空:
(1)只含离子键的物质是______________;
(2)只含共价键的物质是______________;
(3)既含离子键又含共价键的物质是______________;
(4)只含极性键的物质是______________;
(5)既含离子键又含非极性键的物质是______________;
(6)不存在化学键的物质是______________;
(7)属于离子化合物的是______________;
(8)属于共价化合物的是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L密闭容器中,X、Y、Z 三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析
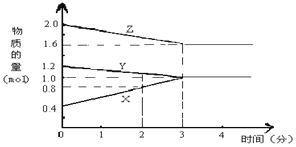
(1)该反应的化学方程式为________。
(2)反应开始至2min末,X的反应速率为_________。
(3)该反应____________。(填序号)
①是可逆反应
②不是可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4X(X为卤素原子)有关转化过程的能量关系如图所示。下列说法不正确的是

A.ΔH1>ΔH4
B.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6=0
C.因为NH4Cl固体溶于水吸热,所以ΔH6<0
D.相同条件下,NH4Br的(ΔH2+ΔH3+ΔH5)比NH4I的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是原子序数依次增大的短周期元素,且
是原子序数依次增大的短周期元素,且![]() 原子序数之和是
原子序数之和是![]() 原子序数之和的
原子序数之和的![]() 。甲、乙、丙、丁是由这些元素组成的二元化合物,
。甲、乙、丙、丁是由这些元素组成的二元化合物,![]() 是某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物
是某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物![]() 是具有漂白性的气体(常温下)。上述物质间的转化关系如图所示(部分反应物和生成物省略)。下列说法正确的是
是具有漂白性的气体(常温下)。上述物质间的转化关系如图所示(部分反应物和生成物省略)。下列说法正确的是

A. 由四种元素形成的两种盐,水溶液中反应能生成![]()
B. ![]() 与
与![]() 形成的化合物中阴、阳离子个数比可为1:1
形成的化合物中阴、阳离子个数比可为1:1
C. 化合物![]() 、乙烯使溴水褪色的原理相同
、乙烯使溴水褪色的原理相同
D. ![]() 与
与![]() 形成的化合物中,成键原子均满足8电子结构
形成的化合物中,成键原子均满足8电子结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com