
【题目】在标准状况下:
(1)0.5 mol HCl占有的体积是__________L。
(2)33.6 L H2的摩尔质量是__________。
(3)在9.5 g某二价金属的氯化物固体中含有0.2 mol Cl-,将此固体加水溶解稀释为100毫升,则此氯化物的摩尔质量为_________此氯化物溶液的物质的量浓度为___________。
科目:高中化学 来源: 题型:
【题目】实验室需要配制0.50 mol·L-1 NaCl溶液480 mL。按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、________、________以及等质量的几片滤纸。
(2)计算。配制该溶液需称取NaCl晶体的质量为________g。
(3)称量。
①称量过程中NaCl晶体应放于天平的________(填“左盘”或“右盘”)。
②称量完毕,将药品倒入烧杯中。
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是________________________。
(5)转移、洗涤。在转移时应使用____________________引流,洗涤烧杯2~3次是为了________________________________。
(6)定容,摇匀。
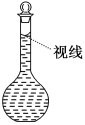
(7)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三草酸合铁酸钾K3[Fe(C2O4)3]xH2O晶体是一种亮绿色的晶体,是制备负载型活性铁催化剂的主要原料,也是一种有机反应良好的催化剂。已知M(K3[Fe(C2O4)3])=437g/mol。本实验以(NH4)2Fe(SO4)26H2O(硫酸亚铁铵晶体)为原料,加入草酸(H2C2O4)制得草酸亚铁(FeC2O4)后,在过量的草酸根(C2O42-)部分实验过程如下:
![]()
(1)在沉淀A中加入饱和K2C2O4溶液,并用40℃左右水浴加热,再向其中慢慢滴加足量的30%H2O2溶液,不断搅拌。此过程需保持温度在40℃左右,可能的原因是:______
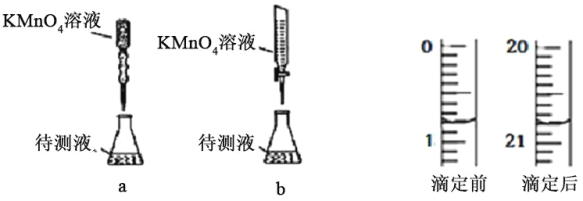
(2)某兴趣小组为知道晶体中x的数值,称取1.637g纯三草酸合铁酸钾(K3[Fe(C2O4)3]xH2O)晶体配成 100ml 溶液,取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4,用浓度为 0.05000molL-1的KMnO4标准溶液进行滴定。其中,最合理的是______(选填 a、b)。由如图KMnO4滴定前后数据,可求得x=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 AgNO3 溶液分别滴定浓度均为 0.01 mol/L 的KCl、K2C2O4 溶液,所得的沉淀溶解平衡图像如图所示(不考虑 C2O42-的水解)。已知 Ksp(AgCl) 数量级为 10-10。下列叙述正确的是
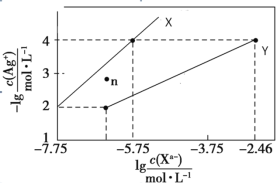
A.图中 Y 线代表的 AgCl
B.n 点表示 Ag2C2O4 的过饱和溶液
C.向 c(Cl-)=c(C2O42-)的混合液中滴入 AgNO3溶液时,先生成 AgCl 沉淀
D.Ag2C2O4+2Cl-=2AgCl+C2O42-的平衡常数为 10-0.71
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是二氧化氯(ClO2)泡腾片的主要成分。实验室以氯酸钠(NaClO3)为原料先制得ClO2,再制备NaClO2粗产品,其流程如图:
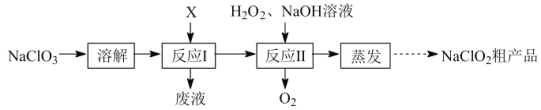
已知:①ClO2可被NaOH溶液吸收,反应为2ClO2+2NaOH=NaClO3+NaClO2+H2O。
②无水NaClO2性质稳定,有水存在时受热易分解。
(1)反应Ⅰ中若物质X为SO2,则该制备ClO2反应的离子方程式为___。
(2)实验在如图-1所示的装置中进行。
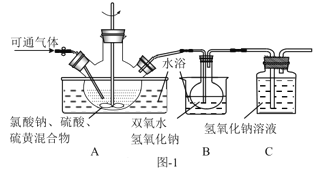
①若X为硫磺与浓硫酸,也可反应生成ClO2。该反应较剧烈。若该反应在装置A的三颈烧瓶中进行,则三种试剂(a.浓硫酸;b.硫黄;c.NaClO3溶液)添加入三颈烧瓶的顺序依次为___(填字母)。
②反应Ⅱ中双氧水的作用是___。保持反应时间、反应物和溶剂的用量不变,实验中提高ClO2吸收率的操作有:装置A中分批加入硫黄、___(写出一种即可)。
(3)将装置B中溶液蒸发可析出NaClO2,蒸发过程中宜控制的条件为___(填“减压”、“常压”或“加压”)。
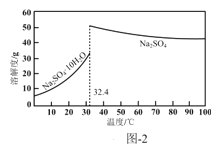
(4)反应Ⅰ所得废液中主要溶质为Na2SO4和NaHSO4,直接排放会污染环境且浪费资源。为从中获得芒硝(Na2SO4·10H2O)和石膏(水合硫酸钙),请补充完整实验方案:___,将滤液进一步处理后排放(实验中须使用的试剂和设备有:CaO固体、酚酞、冰水和冰水浴)。已知:CaSO4不溶于Na2SO4水溶液;Na2SO4的溶解度曲线如图2所示。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应与酸性氧化物的通性无关的是( )
A. 存放NaOH的试剂瓶不用磨口玻璃塞B. ![]() 与水反应制备氧气
与水反应制备氧气
C. 烧煤时加入生石灰脱硫D. ![]() 与澄清石灰水作用
与澄清石灰水作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭容器中,中间有一可自由滑动的隔板,将容器分成两部分。当左边充入1molN2,右边充入8gCO和CO2的混合气体时,隔板处于如右图所示位置(两侧温度相同)。则混合气体中CO和CO2的分子个数比为 ( )

A.1:1 B.1:3 C.2:1 D.3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝氢化钠(![]() )是有机合成的重要还原剂,其合成线路如下图所示。
)是有机合成的重要还原剂,其合成线路如下图所示。
![]()
(1)无水![]() (
(![]() 升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
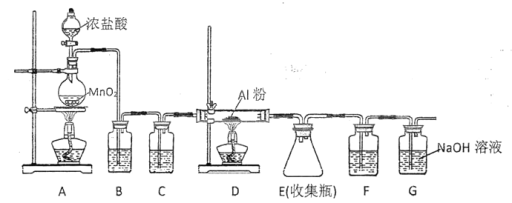
①![]() 中发生反应的化学方程式为__________________。
中发生反应的化学方程式为__________________。
②实验时应先点燃______(填“![]() ”或“
”或“![]() ”)处酒精灯,当观察到____________时,再点燃另一处酒精灯。
”)处酒精灯,当观察到____________时,再点燃另一处酒精灯。
③装置![]() 中盛放饱和NaCl溶液,该装置的主要作用是__________________,请结合方程式进行解释__________________。
中盛放饱和NaCl溶液,该装置的主要作用是__________________,请结合方程式进行解释__________________。
④![]() 中试剂的作用是__________________。用一件仪器装填适当试剂后也可起到
中试剂的作用是__________________。用一件仪器装填适当试剂后也可起到![]() 和
和![]() 的作用,所装填的试剂为__________________。
的作用,所装填的试剂为__________________。
(2)制取铝氢化钠的化学方程式是__________________。
(3)改变![]() 和
和![]() 中的试剂就可以用该装置制取NaH,NaH中氢元素化合价为______,若装置中残留有氧气,制得的NaH中可能含有的杂质为______。
中的试剂就可以用该装置制取NaH,NaH中氢元素化合价为______,若装置中残留有氧气,制得的NaH中可能含有的杂质为______。
(4)铝氢化钠遇水发生剧烈反应,其反应的化学方程式为____________。欲测定铝氢化钠粗产品(只含有NaH杂质)的纯度。称取![]() 样品与水完全反应后,测得气体在标准状况下的体积为
样品与水完全反应后,测得气体在标准状况下的体积为![]() ,样品中铝氢化钠的质量分数为______。(结果保留两位有效数字)
,样品中铝氢化钠的质量分数为______。(结果保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:

已知:RX![]() ROH;RCHO+CH3COOR’
ROH;RCHO+CH3COOR’![]() RCH=CHCOOR’
RCH=CHCOOR’
请回答:
(1)E中官能团的名称是 。
(2)B+D→F的化学方程式 。
(3)X的结构简式 。
(4)对于化合物X,下列说法正确的是 。
A.能发生水解反应 B.不与浓硝酸发生取代反应
C.能使Br2/CCl4溶液褪色 D.能发生银镜反应
(5)下列化合物中属于F的同分异构体的是 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com