
【题目】实验室需要配制0.50 mol·L-1 NaCl溶液480 mL。按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、________、________以及等质量的几片滤纸。
(2)计算。配制该溶液需称取NaCl晶体的质量为________g。
(3)称量。
①称量过程中NaCl晶体应放于天平的________(填“左盘”或“右盘”)。
②称量完毕,将药品倒入烧杯中。
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是________________________。
(5)转移、洗涤。在转移时应使用____________________引流,洗涤烧杯2~3次是为了________________________________。
(6)定容,摇匀。
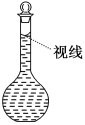
(7)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会________(填“偏高”、“偏低”或“无影响”)。
【答案】500 mL容量瓶(不答规格或答错规格不给分) 胶头滴管 14.6 左盘 搅拌,加速溶解 玻璃棒 保证溶质全部转移至容量瓶中 偏低
【解析】
(1)根据配制步骤是计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;(2)根据n=cV和m=nM来计算;(3)用托盘天平称量药品时,要注意左物右码;(4)结合玻璃棒的作用分析解答;(5)为了防止溶液溅出,要用玻璃棒引流;洗涤烧杯并将洗涤液注入容量瓶的目的是将溶质都转移至容量瓶;(7)根据c=![]() 并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析。
并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析。
(1)操作步骤有计算、称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.由于无480mL的容量瓶,故选用500mL容量瓶,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,根据提供的仪器可知,还需仪器有500mL容量瓶、胶头滴管,故答案为:500mL容量瓶;胶头滴管;
(2)由于无480mL的容量瓶,故选用500mL容量瓶,故配制出的溶液的体积为500mL,根据n=cV可知需要的NaCl的物质的量n=0.50mol/L×0.5L=0.25mol,质量m=nM=0.25mol×58.5g/mol=14.6g,故答案为:14.6;
(3)用托盘天平称量药品时,应左物右码,故答案为:左盘;
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是搅拌,加速固体溶解,故答案为:搅拌,加速溶解;
(5)为了防止溶液溅出,要用玻璃棒引流;洗涤烧杯并将洗涤液注入容量瓶的目的是将溶质都转移至容量瓶,故答案为:玻璃棒;将溶质全部转移至容量瓶;
(7)仰视刻度线,会导致溶液体积偏大,则浓度偏低,故答案为:偏低。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】CO和CO2是碳的两种氧化物,请计算:
(1)在标准状况下,5.6LCO的物质的量是__________,质量是__________。
(2)11gCO2在标准状况下的体积是__________。
(3)相同物质的量的CO和CO2所含氧原子个数之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Zewail创立的飞秒(![]() )化学研究了极短时间内的反应历程,巧妙地解决了如何确定反应起点问题。例如
)化学研究了极短时间内的反应历程,巧妙地解决了如何确定反应起点问题。例如![]() 与
与![]() 的反应过程片段为:
的反应过程片段为:![]() 。下列有关说法正确的是( )
。下列有关说法正确的是( )
A.中间产物![]() 属于有机化合物
属于有机化合物
B.反应起点为![]() 离解为H和I自由基,终点为
离解为H和I自由基,终点为![]() 自由基与I自由基结合
自由基与I自由基结合
C.![]() 经1000fs离解为
经1000fs离解为![]() 自由基和
自由基和![]() ,说明
,说明![]() 与
与![]() 的反应速率极快
的反应速率极快
D.飞秒化学展现的反应历程为“化学反应实质是旧键断裂和新键形成”提供有力证据
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年12月以来,我国武汉等地相继暴发了新冠肺炎,为此我国政府和相关部门采取了多项措施控制疫情。75%乙醇和84消毒液等均能有效灭活新冠病毒。84消毒液的主要成分是次氯酸钠。设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.74.5g次氯酸钠中含有的离子数目为2NA
B.1mol次氯酸钠与足量盐酸反应转移的电子数为2NA
C.46g75%乙醇中含有的氧原子数大于6NA
D.利用氯气和氢氧化钠溶液反应制取0.1mol次氯酸钠需要消耗2.24L氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:① Fe + H2SO4(稀) ![]() FeSO4 + H2↑
FeSO4 + H2↑
② CuO + H2 ![]() Cu + H2O
Cu + H2O
③ MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑ + 2H2O
MnCl2 + Cl2↑ + 2H2O
试回答下列问题:
(1)反应①中_________作氧化剂(填化学式),___________是氧化产物(填化学式);若有2mol Fe完全反应,转移的电子数为________ mol。
(2)用双线桥法表示反应②电子转移的方向和数目:________
(3)反应③中HCl体现了_________________性和_______________性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4=3Br2+Na2SO4+3H2O,与该反应在氧化还原反应原理上最相似的是
A.2NaBr+Cl2=2CaCl+Br2
B.AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl
C.2H2S+SO2=2H2O+3S↓
D.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数的值。下列说法正确的是( )
A.1 mol羟基(-OH)中含7NA个电子
B.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA
C.50 mL 18.4 mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
D.6.2g白磷(分子式为P4)中所含P—P键的数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、一定温度下,某容器中加入足量的碳酸钙发生反应:CaCO3(s)CaO(s)+CO2(g) △H>0;一段时间后达到平衡。
(1)该反应的化学平衡常数表达式为K=______; 为了提高CO2的生成率,可采取的措施______
A.减压B.升温C.增加碳酸钙的量D.转移出CO2
(2)对于该反应,下列说法正确的是______
A.CaCO3(s)加热分解生成CaO(s)和CO2(g),△S>0
B.将容器缩小为原来的一半,平衡不移动
C.将容器扩大为原来的两倍,平衡发生移动,再次平衡后,气体密度不变
D.增大压强,平衡逆向移动,K值减小
Ⅱ、在恒温恒压密闭容器中通入CO和H2O各1mol发生反应CO(g)+H2O(g)CO2(g)+H2(g),当反应达到平衡后,维持温度与压强不变,t1 时再通入各1 mol的CO 和H2O 的混合气体,请在下图中画出正反应和逆反应速率在t1后随时间t变化的曲线图。
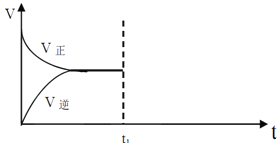 ____________
____________
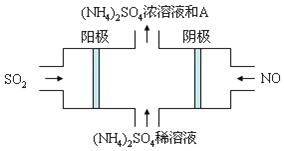
Ⅲ、雾霾的组成成分复杂,包括数百种大气化学颗粒物与气体。图电解装置可将雾霾中的SO2、NO转化为(NH4)2SO4,阴极的电极反应式是______,物质A是______(填名称)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下:
(1)0.5 mol HCl占有的体积是__________L。
(2)33.6 L H2的摩尔质量是__________。
(3)在9.5 g某二价金属的氯化物固体中含有0.2 mol Cl-,将此固体加水溶解稀释为100毫升,则此氯化物的摩尔质量为_________此氯化物溶液的物质的量浓度为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com