
【题目】葡萄糖是一种单糖的理由是( )
A. 它不能发生分解反应B. 不能再水解成更简单的糖
C. 分子中只含1个醛基D. 葡萄糖分子中含碳原子数最少
科目:高中化学 来源: 题型:
【题目】下列事实中,能说明氯的非金属性比硫强的是( )
A.次氯酸(HClO)的酸性比硫酸强
B.次氯酸的氧化性比稀硫酸强
C.氯化氢比硫化氢的热稳定性好
D.最外层电子数氯原子的比硫原子的多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用含有少量氯化钙的氯化钠固体,配制100 mL a mol/L的氯化钠溶液,设计了下面的操作方案。根据方案操作步骤回答下列问题:
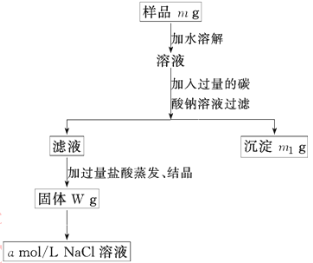
(1)称量粗盐样品m g,在托盘天平左盘上放_____,右盘上放_____。
(2)过滤时,漏斗下端管口应_____,漏斗里液面应_______。
(3)蒸发操作时应将液体放在___中加热,等加热至____时即停止加热。
(4)在样品的溶液中加入过量的Na2CO3溶液,作用是_______,反应的化学方程式是_______。
(5)在滤液中加入盐酸的作用是_______,反应的化学方程式是_____。
(6)配制80 mL a mol/L的NaCl溶液时,应从W g固体中称取NaCl的质量为_____,配制时应在____中进行定容。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是一种红褐色液体或黄色气体,其熔点64.5℃,沸点5.5℃,遇水易水解。它是有机合成中的重要试剂,可由NO与Cl2在常温常压下合成。
(1)实验室制备原料气NO和Cl2的装置如下图所示:
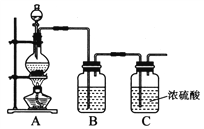
实验室制Cl2时,装置A中烧瓶内发生反应的化学方程式为_______。装置B中盛放的试剂为_______,其作用为___________________。
(2)将上述收集到的Cl2充入D的集气瓶中,按图示装置制备亚硝酰氯。

①NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_______。
②装置D中发生的反应方程式为__________________。
③如果不用装置E会引起什么后果______________________。
④某同学认为装置F不能有效吸收尾气中的某种气体,该气体为_____,为了充分吸收尾气,可将尾气与_______同时通入氢氧化钠溶液中。
(3)工业上可用间接电化学法除去NO,其原理如下图所示,吸收塔中发生的反应为:NO+S2O42+H2O→N2+HSO3

①吸收塔内发生反应的氧化剂与还原剂物质的量之比为_________________。
②阴极的电极反应式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体充入2 L的密闭容器中,一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g)。若经2 s后测得C的浓度为0.6 mol/L,下列几种说法正确的是
2C(g)。若经2 s后测得C的浓度为0.6 mol/L,下列几种说法正确的是
①用物质A表示的反应平均速率为0.3 mol/(L·s)
②用物质B表示的反应的平均速率为0.6 mol/(L·s)
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol/L
A. ①③ B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系中能说明可逆反应N2+3H2 ![]() 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
A. υ正(N2)=υ逆(NH3) B. υ正(N2)=3υ逆(H2)
C. 3υ正(N2)=υ正(H2) D. 2υ正(H2)=3υ逆(NH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X+的核外电子数分别为2、8、8,则X元素在周期表中的位置是( )
A.第三周期第0族B.第四周期第ⅠA族
C.第三周期第ⅠA族D.第三周期第ⅦA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食醋是常用的食品酸味剂,其主要成分是乙酸。下列有关乙酸说法不正确的是( )
A.乙酸易溶于水
B.食醋可由粮食酿造
C.乙酸可与苏打反应
D.乙酸不易挥发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用中和滴定法测定某烧碱的纯度,试根据实验回答:
(1)称取4.1g烧碱样品。将样品配成250mL待测液,需要的主要玻璃仪器除烧杯、玻璃棒外还需__________________ 、______________________。
(2)取10.00mL待测液,用___________________量取。
(3)用0.2010mol·L-1标准盐酸滴定待测烧碱溶液,以酚酞为指示剂,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视_____________,直到看到______________________________即可判断达到滴定终点。
(4)根据下列数据,计算待测烧碱溶液的浓度为:_____________________(结果保留四位有效数字),样品烧碱的质量分数为________________(结果保留四位有效数字)。(假设烧碱中不含有与酸反应的杂质)
滴定次数 | 待测液体积 (mL) | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 10.00 | 0.50 | 20.40 |
第二次 | 10.00 | 4.00 | 24.10 |
(5)滴定过程,下列情况会使测定结果偏高的是_____________________________填序号)。
①酸式滴定管用水洗后便装液体进行滴定;②碱式滴定管水洗后,就用来量取待测液;③锥形瓶用蒸馏水洗涤后,又用待测液润洗;④滴定过快成细流、将碱液溅到锥形瓶壁而又未摇匀洗下;⑤盐酸在滴定时溅出锥形瓶外;⑥滴加盐酸,溶液颜色褪去但不足半分钟又恢复红色;⑦滴定前,酸式滴定管有气泡,滴定后消失;⑧记录起始体积时,仰视读数,终点时俯视。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com