
(13分)实验室配制480mL0.1mol/LNa2CO3溶液回答下列问题
1)应用托盘天平称取十水合碳酸钠(Na2CO3·10H2O)晶体 g。
2)若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上,1g以下用游码,天平平衡时,则实际称量的十水合碳酸钠质量 (填符号 A、偏高 B、偏低 C、不变)
3)用托盘天平和小烧杯称出碳酸钠晶体的质量,其正确操作顺序的标号为(同一步骤可用多次) B→A→ →F→ →F→E
A、调整零点 B、将游码移至刻度尺的零刻度处
C、将碳酸钠晶体放入小烧杯中称量 D、称量空的小烧杯
E、将砝码放回砝码盒内 F、记录称量结果
4)配制Na2CO3溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、 。
5)若实验遇下列情况,所配溶液的浓度偏低的有 (用符号回答)
A、加水定容时越过刻度线
B、忘记将洗涤液转入容量瓶
C、容量瓶内壁附有水珠而未干燥处理
D、溶解后没有冷却便进行定容
E、定容时仰视容量瓶刻度线
6)请你帮助把标签上的内容写一下(如右图)。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
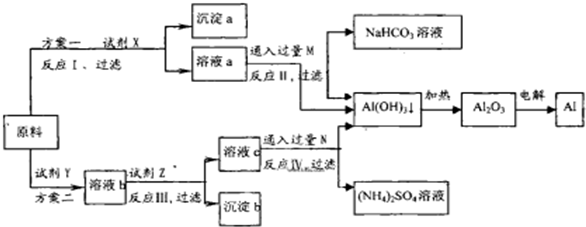
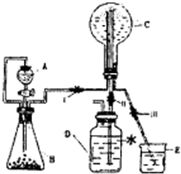
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com