
【题目】某酸性废液中含有Fe2+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对废液进行处理(所加试剂均稍过量),以回收金属,保护环境。

请回答:
(1)沉淀a中含有的单质是_________;
(2)沉淀b的化学式是__________;
(3)沉淀c的化学式是__________;
(4)溶液A与H2O2溶液在酸性条件下反应的离子方程式是_______________。
【答案】 Cu、Fe Fe(OH)3 BaCO3 2Fe2++H2O2+2H+===2Fe3++2H2O
【解析】酸性废液中含有Fe2+、Cu2+、Ba2+三种金属离子,加入铁屑,可置换出铜,沉淀a为Fe、Cu,溶液A含有Fe2+、Ba2+,然后在溶液A中加入过氧化氢、氢氧化钠生成的红褐色沉淀为Fe(OH)3↓,溶液B含有Na+、Ba2+,加入碳酸钠溶液,可生成沉淀c为BaCO3,溶液C含有的阳离子主要为Na+。
(1)由以上分析可知沉淀a中含有的单质是Fe、Cu,故答案为:Fe、Cu;(2)由以上分析可知红褐色沉淀为Fe(OH)3↓,故答案为:Fe(OH)3;(3)由分析可知沉淀c为BaCO3,故答案为:BaCO3;(4)氧化时加入H2O2溶液与二价铁离子发生氧化还原反应,反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O,故答案为:2Fe2++2H++H2O2=2Fe3++2H2O。


科目:高中化学 来源: 题型:
【题目】关于N2(g)+3H2(g)![]() 2NH3(g) △H1KJ/mol,满足如下图像:
2NH3(g) △H1KJ/mol,满足如下图像:

(1)根据图判断△H1 0,T3 T4。(填“>”“<”“=”)
(2)若温度为T1且容器为2L的密闭容器下中,发生合成氨的反应,起始时通入2mol的N2和6mol的H2,10分钟达到平衡状态,此时NH3的体积分数为60%。则0到10min内用H2表示化学反应速率为_________mol/(L·min),N2的转化率为___________,反应开始和平衡状态体系的压强之比等于___________。
(3)若第(2)小问中反应体系达到平衡后,再通入1molN2和3mol的H2,则H2的转化率为___________(填“增大”“减小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见物质的转化是化学学习的重要内容之一。下列各组物质的转化关系中不全部是通过一步反应完成的是
A. Na→NaOH→Na2CO3→NaCl B. Al→Al2O3→Al(OH)3→AlCl3
C. Fe→Fe(NO3)3→Fe(OH)3→Fe2O3 D. S→ SO2→ SO3→ H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定质量的均匀固体混合物Cu、CuO和Cu2O,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少3.20 g,另一份中加入500 mL稀硝酸(其还原产物为NO),固体恰好完全溶解,且同时收集到标准状况下NO气体4.48 L,则所用硝酸的物质的量浓度为( )
A.2.4 mol/L B.1.4 mol/L C.1.2 mol/L D.0.7 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁是由H+、Na+、Al3+、Ba2+、OH—、Cl—、HCO3— 离子中的两种组成,可以发生如图转化,下列说法正确的是( )

A.甲为AlCl3,乙为NaHCO3
B.溶液丙中还可以大量共存的离子有:Fe2+、NO3—、SO42—
C.在甲中滴加丁开始反应的离子方程式HCO3—+ Ba2++OH—= BaCO3↓+ H2O
D.白色沉淀A可能溶解在溶液D中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和条件被略去。A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应;B、C、E是常见气体,G的焰色反应呈黄色;I的溶液呈黄色。

请回答下列问题:
(1)写出下列物质的化学式A__________、 F__________;
(2)说出黄绿色气体C的一种用途_________________________________;
(3)实验室检验H中所含的金属阳离子的方法是,先加____________________无明显现象,再加氯水,溶液变为_________色;
(4)写出Y和D溶液反应的离子方程式_________________________________________;
(5)写出C与H溶液反应的化学方程式__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人类较早使用的金属之一,铁及其化合物之间的相互转化作用可用下式表示:
![]()
I.回答下列有关问题:
(1)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒大小范围是______nm。
(2)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,生成FeCl2和CuCl2,制造印刷电路板。写出FeCl3溶液腐蚀铜的化学反应方程式:___________。检验反应后溶液中还存在Fe3+的试剂是__________。
(3)在下列化学方程式中:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O还原剂是______,生成1molNa2FeO4转移电子数目为__________。
II.现有五种溶液,分别含下列离子:①Ag+,②Mg2+,③Fe2+,④Al3+,⑤Fe3+。
(1)写出符合下列条件的离子符号:既能被氧化又能被还原的离子是______,加铁粉后溶液增重的是______;
(2)向Fe2+的溶液中滴加NaOH溶液,现象是___________________。
(3)欲除去FeCl2中FeCl3选用合适的试剂和分离方法,并写出相应离子方程式:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度和压强下,有如下反应:2SO2(g)+O2(g)![]() 2SO3(g),将1.6molSO2和0.8mol O2放入一体积可变的密闭容器中,测得容器的起始容积为100L经一段时间后,反应达到平衡,测得混合气体的体积为80L,请回答下列问题:
2SO3(g),将1.6molSO2和0.8mol O2放入一体积可变的密闭容器中,测得容器的起始容积为100L经一段时间后,反应达到平衡,测得混合气体的体积为80L,请回答下列问题:
(1)达平衡时SO2的转化率为______________;
(2)若起始时加入amolSO2、bmol O2,且a:b=2:1,在同样温度和压强下,反应达到平衡时,测得混合气体的容积为120L。则a、b的值分别为:a=__________,b=__________。
(3)若容器为体积不变的密闭容器,其容积为100L,起始时加入xmolSO2、ymol O2和zmol SO3,反应达平衡时,温度和压强与(2)完全相同,容器内各气体的体积分数也与(2)达平衡时的情况完全相同,则x、y应该满足的关系式为___________,x、z应该满足的关系式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、实验室中常用MnO2氧化浓盐酸的方法制取氯气,实验装置如图所示:
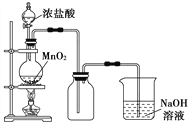
(1)圆底烧瓶中发生反应的化学反应方程式是__________________。
(2)如果将过量二氧化锰与20 mL 12 mol·L-1的盐酸混合加热(忽略盐酸的挥发),充分反应后生成的氯气明显_________(填大于、等于、小于)0.06 mol。其主要原因有_____________________________;
(3)写出尾气处理的离子方程式是_______________________。
II、用Na2CO3·10H2O晶体,配制0.2 mol·L-1的Na2CO3溶液480 mL。
(1)应称取Na2CO3·10H2O晶体的质量:____________。定容时,向容量瓶中加水,至1~2cm时,改用_________加水至刻度,加盖摇匀;
(2)下列操作对所配溶液的浓度可能产生影响
①Na2CO3·10H2O晶体失去了部分结晶水 ②用“左码右物”的称量方法称量晶体(使用游码) ③碳酸钠晶体不纯,其中混有氯化钠 ④容量瓶未经干燥使用。 其中引起所配溶液浓度偏高的有______________(填序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com