
【题目】阿司匹林(乙酰水杨酸,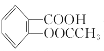 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
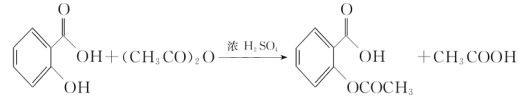
制备基本操作流程如下:
![]()
主要试剂和产品的物理常数如下表所示:
名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
水杨酸 | 138 | 158(熔点) | 微溶 |
醋酸酐 | 102 | 139.4(沸点) | 易水解 |
乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是_____.
(2)合成阿司匹林时,最合适的加热方法是_____.
(3)提纯粗产品流程如下,加热回流装置如图:
![]()
①使用温度计的目的是控制加热的温度,防止_____.
②冷凝水的流进方向是_____(填“a”或“b”);
③趁热过滤的原因是_____.
④下列说法正确的是_____(填选项字母).
a.此种提纯方法中乙酸乙酯的作用是做溶剂
b.此种提纯粗产品的方法叫重结晶
c.根据以上提纯过程可以得出阿司匹林在乙酸乙酯中的溶解度低温时大
d.可以用紫色石蕊溶液判断产品中是否含有未反应完的水杨酸

(4)在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为_____(用百分数表示,小数点后一位).
【答案】醋酸酐和水易发生反应 水浴加热 乙酰水杨酸受热易分解 a 防止乙酰水杨酸结晶析出 abc 84.3%
【解析】
醋酸酐和水杨酸混合,然后向混合溶液中加入浓硫酸,摇匀后加热至85℃,然后冷却、过滤、水洗得到粗产品;
(1)醋酸酐和水易发生反应生成乙酸,生成的乙酸抑制水杨酸和乙酸酐反应,所以需要干燥仪器,
故答案为:醋酸酐和水易发生反应;
(2)合成阿司匹林时要控制温度在85℃~90℃,该温度低于水的沸点,所以合适的加热方法是水浴加热;
(3)①乙酰水杨酸受热易分解,分解温度为128℃~135℃,使用温度计的目的是控制加热的温度,防止乙酰水杨酸受热易分解;
②采取逆流原理通入冷凝水,充满冷凝管,充分冷凝回流,冷凝水从a口进,从b口出,
故答案为:a;
③趁热过滤,防止乙酰水杨酸结晶析出,减少损失,
故答案为:防止乙酰水杨酸结晶析出;
④乙酸乙酯起溶剂作用,趁热过滤除去水杨酸,再冷却结晶析出乙酰水杨酸,说明低温时乙酰水杨酸在乙酸乙酯中的溶解度较小,利用水杨酸、乙酰水杨酸在乙酸乙酯中溶解度不同就行分离提纯,这种分离提纯方法为重结晶,由于水杨酸与乙酰水杨酸均含有羧基,且在水中微弱,不能用紫色石蕊溶液判断产品中是否含有未反应完的水杨酸,
故选:abc;
(4)水杨酸的相对分子质量为138,n(水杨酸)=![]() =0.0145mol,n(乙酸酐)=
=0.0145mol,n(乙酸酐)=![]() =0.0529mol,由于乙酸酐的物质的量大于水杨酸,所以得到的乙酰水杨酸应该按照水杨酸来计算,故理论上得到乙酰水杨酸的质量为0.0145mol×180g/mol=2.61g,产率=
=0.0529mol,由于乙酸酐的物质的量大于水杨酸,所以得到的乙酰水杨酸应该按照水杨酸来计算,故理论上得到乙酰水杨酸的质量为0.0145mol×180g/mol=2.61g,产率=![]() ×100%=
×100%=![]() ×100%=84.3%。
×100%=84.3%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】白花丹酸具有镇咳祛痰的作用,其合成路线流程图如下:
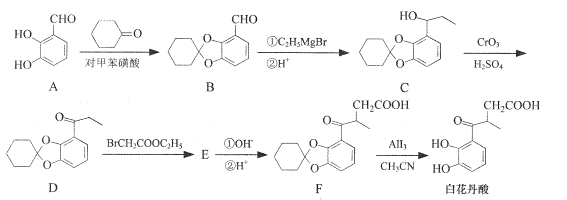
(1)A中的含氧官能团名称为__和_____。
(2)C-D的反应类型为 ___。
(3)白花丹酸分子中混有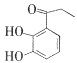 ,写出同时满足下列条件的该有机物的一种同分异构体的结构简式:____。
,写出同时满足下列条件的该有机物的一种同分异构体的结构简式:____。
①分子中有四种不同化学环境的氢;②与FeCl3溶液能发生显色反应,且1 mol该物质最多能与3 mol NaOH反应.
(4)E的结构简式为 ___。
(5)已知:![]() 根据已有知识并结合相关信息写出以
根据已有知识并结合相关信息写出以![]() 和CH3CH2OH为原料制备
和CH3CH2OH为原料制备![]() 的合成路线流程图(合成路线流程图示例见本题题干)____。
的合成路线流程图(合成路线流程图示例见本题题干)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式表达不正确的是 ( )
A. 向FeCl3溶液滴加HI溶液:2Fe3++2I-== 2Fe2++I2
B. CuSO4溶液吸收H2S 气体:Cu2++H2S == CuS↓+2H+
C. 用氢氧化钠溶液吸收工业废气中的NO2:2NO2+2OH- == NO![]() +NO
+NO![]() +H2O
+H2O
D. 向NH4Al(SO4)2溶液中滴加少量Ba(OH)2溶液:2NH4++Ba2++SO42-+2OH—= BaSO4↓+2NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某盐是一种重要的化工原料,在印染、制革、木材和农业等领域有重要用途,其溶液可能含有NH![]() 、Al3+、SO
、Al3+、SO![]() 、Fe2+、Cl-等若干种离子,某同学设计并完成了如下实验:
、Fe2+、Cl-等若干种离子,某同学设计并完成了如下实验:
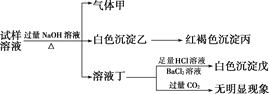
根据以上的实验操作与现象,该同学得出的结论不正确的是( )
A. 试样溶液中肯定有NH![]() 、SO
、SO![]() 和Fe2+
和Fe2+
B. 试样溶液中一定没有Al3+
C. 若气体甲在标准状况下体积为0.448 L,沉淀丙和沉淀戊分别为1.07 g和4.66 g,则可判断试样溶液中还有Cl-
D. 该盐在工业上可以用作净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,3﹣丁二烯和2﹣丁炔分别与氢气反应的热化学方程式如下:CH2=CH﹣CH=CH2 (g)+2H2 (g)→ CH3CH2CH2CH3 (g) H=-236.6kJ/mol CH3﹣C≡C﹣CH3 (g)+2H2 (g)→ CH3CH2CH2CH3 (g) H=-272.7kJ/mol。由此不能判断 ( )
A. 1,3﹣丁二烯和2﹣丁炔稳定性的相对大小
B. 1,3﹣丁二烯和2﹣丁炔分子储存能量的相对高低
C. 1,3﹣丁二烯和2﹣丁炔相互转化的热效应
D. 一个碳碳叁键的键能与两个碳碳双键的键能之和的大小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的四种方法:
方法a | 用炭粉在高温条件下还原CuO |
方法b | 用葡萄糖还原新制的Cu(OH)2制备Cu2O |
方法c | 电解法,反应为2Cu+H2O |
方法d | 用肼(N2H4)还原新制的Cu(OH)2 |
(1)已知:①2Cu(s)+![]() O2(g)=Cu2O(s);△H=﹣169kJmol﹣1
O2(g)=Cu2O(s);△H=﹣169kJmol﹣1
②C(s)+![]() O2(g)=CO(g);△H=﹣110.5kJmol﹣1
O2(g)=CO(g);△H=﹣110.5kJmol﹣1
③Cu(s)+![]() O2(g)=CuO(s);△H=﹣157kJmol﹣1
O2(g)=CuO(s);△H=﹣157kJmol﹣1
则方法a发生的热化学方程式是:_____。
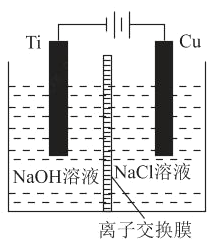
(2)方法c采用离子交换膜控制电解液中OH﹣的浓度而制备纳米Cu2O,装置如图所示:
该离子交换膜为_____离子交换膜(填“阴”或“阳”),该电池的阳极反应式为_____,钛极附近的pH值_____(填“增大”“减小”或“不变”)。
(3)方法d为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.该制法的化学方程式为_____。
(4)在相同的密闭容器中,用以上方法制得的三种Cu2O分别进行催化分解水的实验:
2H2O(g)![]() 2H2(g)+O2(g)△H>0.水蒸气的浓度随时间t变化如下表所示:
2H2(g)+O2(g)△H>0.水蒸气的浓度随时间t变化如下表所示:
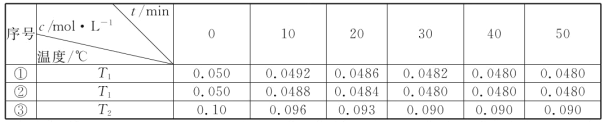
①对比实验的温度:T2_____T1(填“>”“<”或“=”),能否通过对比实验①③到达平衡所需时间长短判断:_____(填“能”或“否”)。
②实验①前20min的平均反应速率 v(O2)=_____
③催化剂的催化效率:实验①_____实验②(填“>”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前世界上海水淡化的主要方法有蒸馏法、电渗析法、反渗透法等。电渗析法是在直流电源作用下通过离子交换膜对海水进行处理(原理如图所示);反渗透法是利用压强差使海水一侧的水分子通过渗透膜进入淡水一侧,从而得到淡水和浓缩的盐溶液(原理如图所示)。下列说法正确的是
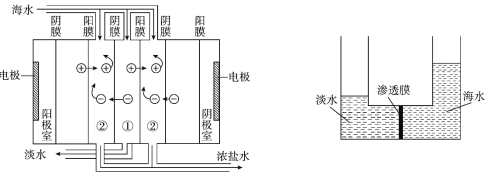
A. 蒸馏法、电渗析法、反渗透法均不发生化学反应
B. 反渗透法所用渗透膜的微孔直径范围是1~100nm
C. 蒸馏法具有设备简单、成本低等优点
D. 浓缩的盐溶液可用于提取或制备食盐、镁、溴等物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有CaCl2、MgCl2、Na2SO4以及泥沙等杂质,以下是制备精盐的实验方案,步骤如下图:
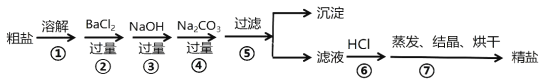
(1)第②步操作的目的是除去粗盐中的______________;( 填化学式,下同)
(2)图中“沉淀”的成分是:____________、_____________、____________、_____________;
(3)第④步操作的目的是除去________________、_________________;写出相应的离子反应方程式:_______________________;_________________________;
(4)第⑥步操作的目的是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HCl的相对分子质量为_________,HCl的摩尔质量为__________。49 g H2SO4的物质的量为 ____________;它与 _______gH2O含相同氧原子;与________L(标准状况)的CO2 相同分子数;与_____________个CO含相同氧原子数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com