
| ||
| m |
| �� |
| n |
| V |
| ||
| 117g��89.6L |
| (1000��26%)g��22.4L |
| 2800g |
| 1.05g/cm3 |
| ||
| 2.67L |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��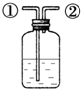 ���ű���ʳ��ˮ���ռ�������ƿ��װ����ʳ��ˮ�������Ӣٿڽ����ڿڳ� |
B��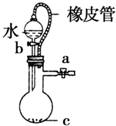 ��װ������Ƥ�ܵ���������ʹˮ˳������ |
C�� ��ȥ���еļ��� |
D��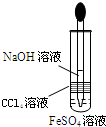 �Ʊ�Fe��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��S��S03 |
| B��Al203��Al�� OH��3 |
| C��Si02��H2SiO3 |
| D��Na2CO3��NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��239Pu��235Uԭ�Ӻ��ڶ�4������ |
| B���˷�Ӧ����ʹ�õ���ˮ��ˮ��Ϊͬλ�� |
| C��ʯ�͡���Ȼ���Ȼ�ʯȼ�����ڿ�������Դ |
| D������ʹ�ú��ܿ���Ч��������������ŷ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������������Һ�У�H+��Fe2+��SO42-��NO3- |
| B��ʹ���ȱ�����Һ�У�Ca2+��NH4+��CH3COO-��Cl- |
| C��0.1 mol?L-1��BaCl2��Һ�У�K+��Na+��OH-��NO3- |
| D����ˮ�������c��H+��=10-12 mol?L-1����Һ�У�Mg2+��K+��Br-��HCO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
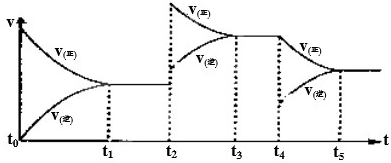
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶�/�� | 500 | 700 | 850 | 1 000 |
| ƽ�ⳣ�� | 2.5 | 1.7 | 1.0 | 0.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 A��B��C��D��EΪǰ������Ԫ�أ�ԭ��������������̬Aԭ�ӵĺ������ռ��4��ԭ�ӹ����B��Cͬ���壬����ƽ�����е���B3Ũ�ȼ��ٻ����˻�Ƥ�������ӣ�D��ǰ������Ԫ���е�һ��������С��Ԫ�أ�E�ĺϽ��ǵ����������ĺϽ�
A��B��C��D��EΪǰ������Ԫ�أ�ԭ��������������̬Aԭ�ӵĺ������ռ��4��ԭ�ӹ����B��Cͬ���壬����ƽ�����е���B3Ũ�ȼ��ٻ����˻�Ƥ�������ӣ�D��ǰ������Ԫ���е�һ��������С��Ԫ�أ�E�ĺϽ��ǵ����������ĺϽ��鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com