
【题目】在一定容积的密闭容器中进行反应:N2(g)+3H2(g)![]() 2NH3(g)。已知反应过程中某一时刻N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.2mol/L。则N2、H2、NH3的起始浓度不可能存在的数据是( )
2NH3(g)。已知反应过程中某一时刻N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.2mol/L。则N2、H2、NH3的起始浓度不可能存在的数据是( )
A.N2为0.2mol/L,H2为0.6mol/L
B.N2为0.15mol/L
C.N2、H2均为0.18mol/L
D.NH3为0.4mol/L
【答案】C
【解析】
反应N2(g)+3H2(g)2NH3(g)为可逆反应,转化率不可能为100%,根据化学计量数及极值法:N2的物质的量浓度范围是0![]() 0.2mol·L-1,H2的物质的量浓度范围是0
0.2mol·L-1,H2的物质的量浓度范围是0![]() 0.6mol·L-1,NH3的物质的量浓度范围是0
0.6mol·L-1,NH3的物质的量浓度范围是0![]() 0.4mol·L-1,据此解答。
0.4mol·L-1,据此解答。
A. N2的起始浓度可能为0.2 mol/L,H2的起始浓度可能为0.6 mol/L,A正确;
B. N2的物质的量浓度范围为0![]() 0.2mol·L-1,N2为0.15mol/L,在该范围内,B正确;
0.2mol·L-1,N2为0.15mol/L,在该范围内,B正确;
C. N2和H2的物质的量浓度之比始终满足1:3,二者化学计量数为1:3,所以不可能均为0.18mol/L,C错误;
D. NH3的物质的量浓度范围是0![]() 0.4mol·L-1,NH3起始浓度可能为0.4 mol/L,D正确;
0.4mol·L-1,NH3起始浓度可能为0.4 mol/L,D正确;
故答案为:C。


 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在体积为2L的恒容密闭容器中,某一反应中![]() 、
、![]() 、
、![]() 三种气体的物质的量随时间变化的曲线如图所示,下列叙述正确的是( )
三种气体的物质的量随时间变化的曲线如图所示,下列叙述正确的是( )
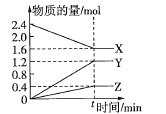
A.反应的化学方程式为![]()
B.t时刻,正、逆反应都不再继续进行,反应达到化学平衡
C.若![]() ,则0~tmin内
,则0~tmin内![]() 的化学反应速率为
的化学反应速率为![]()
D.温度、体积不变,在tmin时充入![]()
![]() 使压强增大,正、逆反应速率都增大
使压强增大,正、逆反应速率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个绝热的固定容积的密闭容器中,发生可逆反应mA(g)+nB(g)![]() pC(g)+qD(s),当m、n、p、q为任意整数时,一定可以作为反应达到平衡的标志是( )
pC(g)+qD(s),当m、n、p、q为任意整数时,一定可以作为反应达到平衡的标志是( )
①体系的压强不再改变 ②体系的温度不再改变 ③体系的密度不再变化 ④各组分质量分数不再改变
A.①②③B.①②③④C.②③④D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入1molCO2和3molH2。在500℃下发生发应,CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如下图1所示:
CH3OH(g)+H2O(g)。实验测得CO2和CH3OH(g)的物质的量(n)随时间变化如下图1所示:
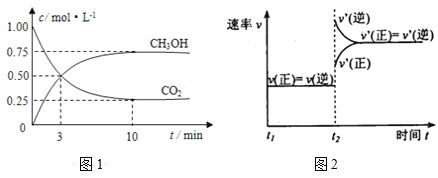
(1)从反应开始到平衡,氢气的平均反应速率v(H2)=________。
(2)500℃该反应的平衡常数为_____(结果保留一位小数),图2是改变温度时化学反应速率随时间变化的示意图,若提高温度到800℃进行,达平衡时,K值_____(填“增大”“减小”或“不变”)。
(3)下列措施中不能使CO2的转化率增大的是_______。
A 在原容器中再充入1mol H2 B 在原容器中再充入1molCO2
C 缩小容器的容积 D 使用更有效的催化剂 E 将水蒸气从体系中分离出
(4)500℃条件下,测得某时刻,CO2(g)、H2(g)、CH3OH(g)和H2O(g)的浓度均为0.5mol/L,则此时v(正)____ v(逆)(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在某密闭容器中发生反应:2HI(g)![]() H2(g)+I2(s) ΔH>0,若0~15s内c(HI)由0.1mol·L-1降到0.07mol·L-1,则下列说法正确的是( )
H2(g)+I2(s) ΔH>0,若0~15s内c(HI)由0.1mol·L-1降到0.07mol·L-1,则下列说法正确的是( )
A.0~15s内用I2的平均反应速率为v(I2)=0.001mol·L-1·s-1
B.c(HI)由0.07mol·L-1降到0.05mol·L-1所需的反应时间为小于10s
C.升高温度正反应速率加快,逆反应速率减慢
D.减小反应体系的体积,化学反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.2mol两种气态烃组成的混合气完全燃烧后得到6.72L二氧化碳(标准状况下)和7.2g水,下列关于该混合烃说法正确的是( )
A.一定有乙烯B.一定有甲烷
C.一定是甲烷和乙烯的混合气体D.可能有乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学常见物质A、B、C、D、E、X,存在下图转化关系 ![]() 部分生成物和反应条件略去
部分生成物和反应条件略去![]() 。下列推断不正确的是
。下列推断不正确的是![]()
![]()
![]()
A.若D是一种强碱,则A、C均可与X反应生成D
B.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
C.若D为NaCl,且A可与C反应生成B,则E可能是![]()
D.若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )
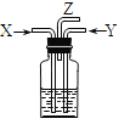
A.洗气瓶中产生的沉淀是碳酸钡
B.洗气瓶中产生的沉淀是硫酸钡
C.在Z导管出来的气体中没有二氧化碳
D.在Z导管口排出无色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中常含有一定量的Cr2O72—和CrO42—,它们会对人类及生态系统产生很大的危害,必须进行处理。下面是一种处理方法的工业流程:

其中第①步存在平衡:2CrO42-(黄色)+2H+![]() Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
下列说法正确的是( )
A. 反应②中还原1mol Cr2O72—,需要6 mol的Fe2+
B. 改变反应①的平衡体系中c(H+)浓度,溶液颜色无明显变化
C. 若2v (Cr2O72-) =v (CrO42-),说明反应①达平衡状态
D. FeSO4溶液呈酸性的原因是Fe2++ 2H2O ![]() Fe(OH) 2↓+ 2H+
Fe(OH) 2↓+ 2H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com