
【题目】(1)有①168 O 、 17 8O 、 188O ;②H2、D2、T2;③石墨、金刚石;④11H 、21H、 31H;四组微粒或物质。互为同位素的是_____(填编号)。
(2)下列物质中:①N2;②MgCl2;③NH4Cl;④CH4;⑤CO2;⑥Ne;⑦H2S;⑧KOH;⑨Na2O2; ⑩K2O;只存在共价键的是_____;属于离子化合物,但含有共价键的 是_____。
(3) 用电子式表示下列物质:
MgCl2 _____; N2 _____;
NH4+_____; Na2O2 _____。
【答案】①、④ ①、④、⑤、⑦ ③、⑧、⑨ ![]()
![]()
![]()
【解析】
(1)质子数相同,中子数不同的原子互为同位素;
(2)像氯化氢那样,以共用电子对(或共价键)结合在一起的化合物,叫做共价化合物;离子化合物 由阳离子和阴离子构成的化合物;
(3)根据构成物质的化学键进行判断并书写电子式。
(1)①168 O 、 17 8O 、 188O质子数相同,中子数不同,故互为同位素;
②H2、D2、T2是由氢的同位素原子构成的氢分子,既不是同位素,也不是同素异形体;
③石墨、金刚石都是由碳元素形成的不同单质,互为同素异形体;
④11H 、21H、 31H质子数相同,中子数不同,故互为同位素;
互为同位素的是:①④;
(2)①CO2中只含共价键,为共价化合物;
②MgCl2中只含离子键,为离子化合物;
③NH4Cl中含离子键和N-H极性共价键,为离子化合物;
④CH4中只含共价键,为共价化合物;
⑤CO2中只含共价键,为共价化合物;
⑥Ne中不含化学键,为单质;
⑦H2S中只含极性共价键,为共价化合物;
⑧KOH中含离子键和极性共价键,为离子化合物;
⑨Na2O2中含离子键和O-O非极性共价键,为离子化合物;
⑩K2O中只含离子键;
只存在共价键的是①④⑤⑦;
属于离子化合物的是②③⑧⑨⑩,且含有共价键为:③⑧⑨;
(3)MgCl2是镁离子与2个氯离子通过离子键结合,电子式为:![]() ;
;
氮气中两个氮原子通过三对共用电子对结合,电子式为:![]() ;
;
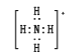
氨根离子为阳离子,氮原子与氢原子间通过共价键,电子式为: ;
;
过氧化钠为离子化合物,2个钠离子与过氧根离子通过离子键结合,两个氧原子通过共用电子对结合,电子式为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】向2L密闭容器中通入amol气体A和bmol气体B,在一定条件下发生反应:xA(g)+yB(g) ![]() pC(g)+qD(g)已知:平均反应速率v(C)=
pC(g)+qD(g)已知:平均反应速率v(C)= ![]() v(A);反应2min时,A的浓度减少了
v(A);反应2min时,A的浓度减少了![]() ,B的物质的量减少了
,B的物质的量减少了![]() mol,有
mol,有![]() molD生成。回答下列问题:
molD生成。回答下列问题:
(1)反应2min内,v(A)=______________;v(B)=______________;
(2)化学方程式中,x=_______、y=_______、p=_______、q=_______;
(3)下列叙述能说明该反应已达平衡状态的是:__________________;
A、 xV(A)正=qV(D)逆 B、气体总的质量保持不变 C、C的总质量保持不变 D、混合气体总的物质的量不再变化 E、混合气体总的密度不再变化 F、混合气体平均分子量不再变化
(4)反应平衡时,D为2amol,则B的转化率为_______________;
(5)其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较,反应速率__________(是“增大”“减小”或“不变”),理由是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3He可以作为核聚变材料,以下关于3He的说法正确的是
A.比4He少一个质子B.比4He多一个中子
C.是4He的同素异形体D.是4He的同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.用氢氧化钠溶液清洗沾在皮肤上的苯酚B.用浓硫酸吸收氨气中的水分
C.用稀硝酸洗去残留在试管内壁上的银D.用酒精萃取碘水中的碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中发生反应:xA(g) +B(g)![]() 2C(g) △H<0,A、 C的物质的量随时间变化的关系如图。下列有关说法正确的是
2C(g) △H<0,A、 C的物质的量随时间变化的关系如图。下列有关说法正确的是
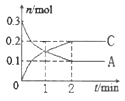
A. x=1
B. 反应进行到1min时,反应体系达到化学平衡状态
C. 2min后,A的正反应速率一定等于C的逆反应速率
D. 2min后,容器中A与B的物质的量之比一定为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)![]() 2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如下图所示:
2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如下图所示:

下列说法中正确的是
A. 30~40 min间该反应使用了催化剂
B. 反应方程式中的x=1,正反应为吸热反应
C. 30 min时降低温度, 40 min时升高温度
D. 8 min前A的平均反应速率为0.08 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向容积为2 L的密闭容器中充入1 mol CO2和3 mol H2,发生如下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),5 min后反应达到平衡时c(CH3OH)为0.2 mol·L-1。CO2(g)的平衡物质的量浓度c(CO2)与温度关系如下图所示。下列说法错误的是
CH3OH(g)+H2O(g),5 min后反应达到平衡时c(CH3OH)为0.2 mol·L-1。CO2(g)的平衡物质的量浓度c(CO2)与温度关系如下图所示。下列说法错误的是

A. 0~5 min,CO2的平均反应速率为0.04 mol·L-1·min-1
B. 在T2 ℃时,若反应处于状态D,则v正<v逆
C. 反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)的ΔH<0
CH3OH(g)+H2O(g)的ΔH<0
D. 若T1 ℃、T2 ℃时的平衡常数分别为K1、K2,则K1>K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色透明的强酸性溶液中,能大量共存的离子组是( )
A. K+、Na+、Cu2+、SO42- B. Na+、Al3+、Cl-、NO3-
C. Na+、K+、HCO3-、Cl- D. K+、 SO42-、 Cl-、Ba2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com