
【题目】下表列出了前20号元素中某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中,第一电离能最小的是(填编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足8e-稳定结构的物质可能是(写分子式)。元素⑨和⑩形成的化合物的化学式为;元素①的原子价电子排布式是。
(3)①、⑥、⑦、⑩四种元素的气态氢化物的稳定性,由强到弱的顺序是(填化学式)。
(4)③和⑨两元素比较,非金属性较弱的是(填名称),可以验证你的结论的是下列中的(填序号)。
A.气态氢化物的挥发性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表③和⑨两元素)
F.两单质在自然界中的存在形式
【答案】
(1)②
(2)PCl3、CCl4;Si3N4;3s23p4
(3)HCl>H2S>PH3>SiH4
(4)氮元素;C
【解析】由题意可知,10种元素是前20号元素,根据表中数据,可推出①S,②K,③O,④Al,⑤C,⑥P,⑦Cl,⑧Na,⑨N,⑩Si。 (1)一般来说,在同一周期中,自左至右,元素的第一电离能逐渐增大;同一主族中,从上向下,元素的第一电离能逐渐减小。故在10种元素中,第一电离能最小的是②K。(2)C、P、Cl中的某两种元素形成的化合物中,PCl3或CCl4分子中的每一个原子都满足8e-稳定结构;元素⑨和⑩形成的化合物是Si3N4;S元素的原子价电子排布式是3s23p4。(3)元素的非金属性越强,形成的气态氢化物越稳定,非金属性强弱为Cl>S>P>Si,故其氢化物稳定性为HCl>H2S>PH3>SiH4。(4)氧元素和氮元素相比,非金属性较弱的是氮元素,可通过C项验证。


科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律分析下面的推断,其中不正确的是
A. Na的原子失去电子能力比Mg强
B. HBr比HCl稳定
C. Ca(OH)2 的碱性比 Mg(OH)2 的碱性强
D. H2SO4 比H3PO4 酸性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。
(1)膦(PH3)是一种无色有剧毒的气体,其还原能力比氨(NH3)强,是一种强还原剂.某反应体系中存在下列物质:Cu、H2SO4、CuSO4、PH3、H3PO4、H2O.回答下列问题:
①上述反应体系中化学反应方程式为;
②膦(PH3)能和水发生微弱的化学反应,其水溶液呈弱碱性,该反应可用离子方程式表示为 .
(2)生活污水中含大量细小的悬浮物,可加某些物质使之聚集成较大的颗粒而沉淀.请你举一种常见的能使生活污水中悬浮物聚沉的物质,其化学式为 .
(3)用CH4催化还原NOX可以消除氮氧化物的污染.例如
CH4(g)+4NO2(g) 4NO(g)+CO2 (g)+2H2O(g)△H1=﹣574kJmol﹣1
CH4(g)+4NO(g)2N2(g)+CO2(g)+2H2O(g)△H2
若1mol CH4还原NO2至N2 , 整个过程中放出的热量为867kJ,则△H2= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数,他们利用盐酸、氢氧化钠溶液设计了三种不同的实验方案:
方案一:铝镁合金 ![]() 测定生成气体的体积
测定生成气体的体积
方案二:铝镁合金 ![]() 测定生成气体的体积
测定生成气体的体积
方案三:铝镁合金 ![]() 溶液
溶液 ![]()
![]() 称量灼烧产物的质量.
称量灼烧产物的质量.
(1)写出方案一中发生反应的离子方程式 .
(2)实验小组根据方案=设计了两个实验装置,如下圈(图中的铁架台已省略). 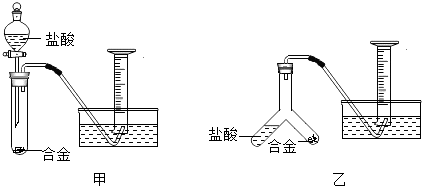
你认为选择(选填甲或乙)装置进行实验更合理,误差更小.
(3)用方案三进行实验时,除了称量灼烧产物质量外,还需称量的是 .
(4)拓展研究:在向铝镁合金溶于盐酸后的溶液中加入过量NaOH溶液时,生成沉淀的质量与加入NaOH溶液体积的关系可用数轴关系表示: 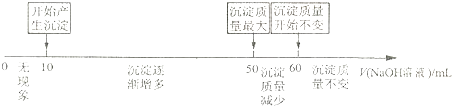
请你判断,根据如图数轴申的数据能否求出合金中镁的质量分数?(选填“能”或“不能”)
下列①②两题选一题作答.
①若不能求出合金中镁的质量分数,请说明理由.
②若能求出合金中镁的质量分数,则镁的质量分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸性废液中含有Fe2+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对废液进行处理(所加试剂均稍过量),以回收金属,保护环境。
请回答:
(1)沉淀a中含有的单质是;
(2)沉淀b的化学式是;
(3)沉淀c的化学式是;
(4)溶液A与H2O2溶液在酸性条件下反应的离子方程式是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于氯化钠晶体,下列描述正确的是( )
A.它是六方紧密堆积的一个例子
B.58.5g氯化钠晶体中约含6.02×1023个NaCl分子
C.与氯化铯晶体结构相同
D.每个Na+与6个Cl-作为近邻
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方法能达到实验目的是( )
A.用分液漏斗从食醋中分离出乙酸
B.用焰色反应鉴别Na2SO4和Na2CO3
C.用NaOH溶液除去Cl2中含有的少量HCl
D.用KSCN溶液检验FeCl3溶液 中是否含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.在恒温条件下,将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示):。
(2)0~10min化学反应速度V(X)=。
(3)比较Y在0~10min和10~20min时平均反应速率的大小:v(0~10) v(10~20)(填“<”、“>”或“=”),原因是。
(4)a、b、c、d四个点中,表示化学反应处于平衡状态的点是 , 理由是。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com