
【题目】设NA代表阿伏加德罗常数,下列物质所含分子数最少的是
A. 6 mol CO2 B. 6g氢气 C. 标准状况下,224L氨气 D. 含氧分子数为4NA的氧气
 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】(1)NaHSO4是一种酸式盐。2mol/L的NaHSO4溶液与1mol/L的Ba(OH)2溶液等体积混合,反应的离子方程式为__________________________。
(2)写出Na与FeCl3溶液的反应的离子反应方程式:_________________________________
(3)乙同学检测到该溶液中含有大量的Cl﹣、Br﹣、I﹣,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl﹣、Br﹣、I﹣的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
Cl2的体积(标准状况) | 11.2L | 22.4L | 28.0L |
n(Cl﹣) | 2.5mol | 3.5mol | 4.0mol |
n(Br﹣) | 3.0mol | 2.5mol | 2.0mol |
n(I﹣) | x mol | 0 | 0 |
原溶液中Cl﹣、Br﹣、I﹣的物质的量浓度之比为______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物E是一种合成高血压药物的中间体,其合成路线流程图如下:
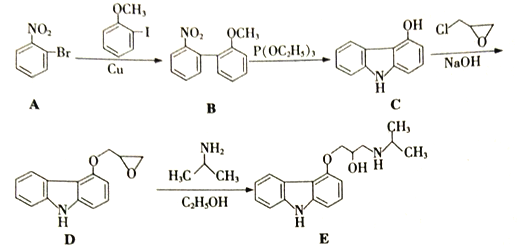
(1) 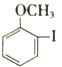 中所含官能团名称为_____和______。
中所含官能团名称为_____和______。
(2)苯环上的硝基对新引入基团的位置会产生一定的影响,如:
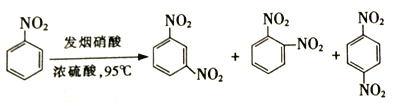 (产物中,间二硝基苯占93%)苯经两步反应制得A,第一步反应的条件为_________。
(产物中,间二硝基苯占93%)苯经两步反应制得A,第一步反应的条件为_________。
(3)写出同时满足下列条件的B的一种同分异构体X的结构简式: _________。
①含有两个苯环,分子中有6种不同化学环境的氢;
②既能与盐酸反应,又能与NaHCO3溶液反应。
(4)合成E时,还可能生成一种与E互为同分异构体的副产物Y,Y的结构简式为______。
(5)常温下,苯酚在Br2的CCl4溶液中发生取代反应,得到一溴代物。请写出以苯酚、CCl4为原料制备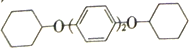 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。______________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个密闭容器甲、乙中,依次充入氧原子数目相同的O2、O3两种气体,若它们的温度和密度均相同。下列说法正确的是
A. 气体体积:甲>乙 B. 气体的压强:甲>乙
C. 气体的分子数:甲<乙 D. 气体的质量:甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列粒子:N2、CO2、NH3、N2O、NO2、NO2-、NO和CO。
(1)互为等电子体的粒子有________________。
(2)过量Mg可以在N2O中燃烧,写出反应的化学方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室要配制80 mlL1.00 mol/LNaCl溶液,实验室现有含有少量碳酸钠的氯化钠固体。
Ⅰ.为了除去氯化钠样品中的杂质,某兴趣小组最初设计了如下方案进行实验:
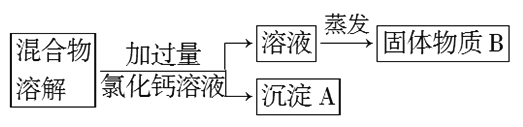
(1)沉淀A的化学式是_______________。
(2)在实验过程中,又发现了新的问题:此方案很容易引入新的杂质。则固体物质B的成分为_________________(用化学式表示)。
(3)继续探究后又提出了新的方案:将混合物溶解,先滴加足量_________________(填试剂名称),再蒸发结晶,有关反应的离子方程式为_______________________________。
Ⅱ.配制溶液:
(1)配制过程中需要使用的玻璃仪器除烧杯和玻璃棒外还有_________________。
(2)从所配溶液中取出10mL,与足量AgNO3溶液反应,经过滤、洗涤、干燥后得到白色沉淀1.50 g。则所配溶液的浓度________1.00 mol/L (填“>”、“<”或“=”),造成此误差的操作可能是_______________。
A.使用容量瓶前未干燥
B.用托盘天平称量氯化钠固体时将砝码错放在左盘
C.定容时俯视容量瓶的刻度线
D.定容后经震荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制Cl2反应4HCl(浓)+MnO2 ![]() MnCl2+ Cl2↑+2H2O,下列说法不正确的是
MnCl2+ Cl2↑+2H2O,下列说法不正确的是
A. 还原剂是HCl,氧化剂是MnO2
B. 每有2molHCl被氧化,转移电子的物质的量为2mol
C. 每消耗1mol MnO2,起还原剂作用的HCl消耗4mol
D. 转移电子的物质的量为1mol时,生成标准状况下Cl2的体积为11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)3.4g NH3中含有________mol H。
(2)标准状况下,等体积的CO和CO2的质量比为________。
(3)100 mL Al2(SO4)3溶液中c (Al3+)=0.20 mol·Lˉ1,则c(SO42-)=_______。
(4)物质的量浓度相同的NaCl、MgCl2、AlCl3溶液中分别加入足量的AgNO3溶液中,生成沉淀的质量相等,三种溶液的体积比为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com