
【题目】如图装置可用于收集SO2并验证其某些化学性质,下列说法正确的是
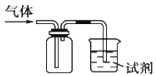
选项 | 试剂 | 现象 | 结论 |
A | 酸性高锰酸钾溶液 | 溶液褪色 | SO2有漂白性 |
B | 品红溶液 | 溶液褪色 | SO2有氧化性 |
C | 滴有酚酞的NaOH溶液 | 溶液褪色 | SO2有还原性 |
D | H2S水溶液 | 溶液变浑浊 | SO2有氧化性 |
A.AB.BC.CD.D
科目:高中化学 来源: 题型:
【题目】利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。
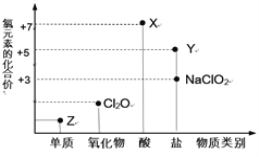
回答下列问题:
(1)X的电离方程式为_________。
(2)氯的某种氧化物(ClmOn)中氯、氧元素质量比为71:48,则m:n= _________。
(3) NaClO有较强的氧化性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式_____________。
(4)NaClO2具有很强的氧化性,常用作消毒剂,其消毒效率是Z的 ___________倍(还原产物都为Cl-,消毒效率以单位物质的量得到的电子数表示)。
(5)Cl2O可用潮湿的Z与Na2CO3反应制取,同时生成NaHCO3,反应中Z既体现氧化性,又体现还原性,该反应的化学方程式为_____________。
(6)自来水中的![]() 对人类健康产生危害。为了降低自来水中
对人类健康产生危害。为了降低自来水中![]() 的浓度,某研究人员提出在碱性条件下用Al粉还原
的浓度,某研究人员提出在碱性条件下用Al粉还原![]() ,产物是N2。发生的反应可表示如下,请完成方程式的配平:___Al+ ____
,产物是N2。发生的反应可表示如下,请完成方程式的配平:___Al+ ____![]() + _____=___
+ _____=___![]() + _____ N2↑ + _______H2O
+ _____ N2↑ + _______H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释工业生产或应用的化学用语中,不正确的是( )
A. FeCl3溶液刻蚀铜电路板:2Fe3+ + Cu==2Fe2++ Cu2+
B. 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O== Al(OH)3↓ + 3NH4 +
C. 将少量二氧化碳通入次氯酸钠溶液中:CO2+H2O+2ClO-== CO32-+2HClO
D. Na2CO3溶液处理水垢:CaSO4(s)+CO32(aq)![]() CaCO3(s)+SO42(aq)
CaCO3(s)+SO42(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),过程如下:
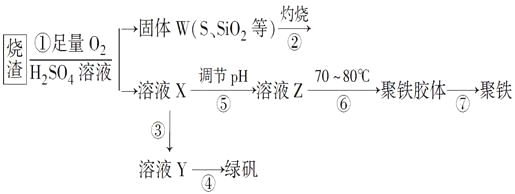
(1)将过程②中的产生的气体通入下列溶液中,溶液会褪色的是________。
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.溴水
(2)过程①中,FeS和O2、H2SO4反应的离子方程式为:________。
(3)过程③中,需加入的物质是________。
(4)过程④中,蒸发结晶需要使用酒精灯、三角架、泥三角,还需要的仪器有___________。
(5)过程⑤调节pH可选用下列试剂中的________(填选项序号)。
A.稀硫酸 B.CaCO3 C.NaOH溶液
(6)过程⑥中,将溶液Z加热到70~80℃,目的是___________。
(7)实验室为测量所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取2.800 g样品;②将样品溶于足量的盐酸后,加入过量的氯化钡溶液;③过滤、洗涤、干燥、称量,得固体质量为3.495 g。若该聚铁主要成分为[Fe(OH)(SO4)]n,则该聚铁样品中铁元素的质量分数为________。(假设杂质中不含铁元素和硫元素)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中加入过量Na2O2后仍能大量共存的是
A.NH![]() 、Ba2+、Cl-、NO
、Ba2+、Cl-、NO![]() B.K+、SiO
B.K+、SiO![]() 、AlO
、AlO![]() 、SO
、SO![]()
C.Fe2+、Mg2+、SCN-、Cl-D.Na+、SO![]() 、I-、HCO
、I-、HCO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期过渡元素单质及其化合物在生活、生产中有广泛应用。回答下列问题:
(1)基态Cu原子电子排布式为:__________。
(2)过渡金属单质及化合物是有机合成反应的重要催化剂。
例如:
①苯甲醇中碳原子的杂化类型是___________。
②苯甲醇的沸点比苯甲醛_______ 。(填“高”或“低”)
③苯甲醛分子中三种非金属元素C、O、H的电负性由大到小的顺序是____________ 。
(3)多数过渡金属的配离子在水中有颜色,其显色与配合物分裂能有关。定义1个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量为d轨道的分裂能,用![]() 表示,中心离子电荷数越大,中心与配体距离越近,则作用越强,
表示,中心离子电荷数越大,中心与配体距离越近,则作用越强,![]() 越大。分裂能(
越大。分裂能(![]() )Co(H2O)62+_______Co(H2O)63+(填“ > ”“〈”或“ =”)。
)Co(H2O)62+_______Co(H2O)63+(填“ > ”“〈”或“ =”)。
(4)钨与碳组成一种特殊材料,其晶体的晶胞如图1所示,它的熔点为2870℃、硬度类似金刚石,预测它的晶体类型是_________。
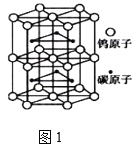
(5)Fe的一种晶体如图2所示,设阿伏加德罗常数的值为NA,铁原子的半径是r cm,该晶体的密度是ρ g/cm3,则铁的相对原子质量为___(只列出计算式)
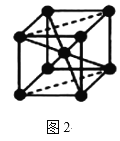
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在密闭容器中SO2、O2、SO3三种气态物质建立化学平衡后,改变条件对反应2SO2(g)+O2(g)2SO3(g) ΔH<0的正、逆反应速率的影响如图所示:
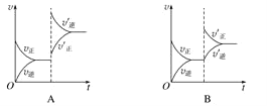
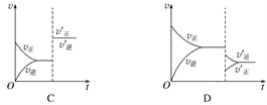
(1)加催化剂对反应速率影响的图象是__________(填字母,下同),平衡__________移动。
(2)升高温度对反应速率影响的图象是__________,平衡向__________方向移动。
(3)增大反应容器体积对反应速率影响的图象是__________,平衡向__________方向移动。
(4)增大O2的浓度对反应速率影响的图象是__________,平衡向__________方向移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z在周期表中的位置如图所示,则下列说法正确的是

A. Z一定是活泼的金属
B. Y的最高价氧化物的水化物是一种强酸
C. Z的最高价氧化物的水化物是强酸
D. 1 molY单质跟足量水反应时,有1 mol电子发生转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的方程式中不合理的是(已知:饱和NaClO溶液的pH约为11)
A. 该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-="==" Cl-+ ClO-+ H2O
B. 该消毒液的pH约为12:ClO-+ H2O![]() HClO+ OH-
HClO+ OH-
C. 该消毒液与洁厕灵(主要成分为HCl)混用,产生Cl2:2H++ Cl-+ ClO-= Cl2↑+H2O
D. 该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ ClO-= HClO+CH3COO—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com