
【题目】现有下列各化合物:
A.CH3CH2CH2CHO与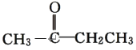
B.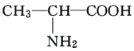 与
与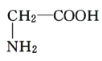
C. ![]() 与
与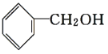
D.CH3CH≡CH与CH2=CH—CH=CH2
E. 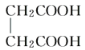 与
与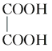
F.戊烯与环戊烷
(1)上述各组化合物中属于同系物的是________,属于同分异构体的是________(填字母)。
(2)上述A中两化合物的含氧官能团是__________和 __________(写名称)。
(3)根据官能团的特点可将C中两种化合物划分为________类和________类。
【答案】BE AF 醛基 羰基 酚 醇
【解析】
同系物是结构相似,分子组成上相差1个或若干个亚甲基原子团的一系列物质的互称;同分异构体是分子式相同,结构不同的化合物的互称。据此判断。
A.CH3CH2CH2CHO与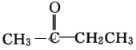 由结构简式可知两者的分子式相同,但结构不同,互为同分异构体。
由结构简式可知两者的分子式相同,但结构不同,互为同分异构体。
B.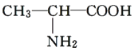 与
与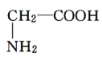 ,两者结构相似,组成上相差1个亚甲基,属于同系物关系。
,两者结构相似,组成上相差1个亚甲基,属于同系物关系。
C. ![]() 与
与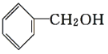 ,前者羟基连在苯环上,属于酚类,后者羟基连在烃基侧链上属于醇类。
,前者羟基连在苯环上,属于酚类,后者羟基连在烃基侧链上属于醇类。
D.CH3CH≡CH与CH2=CH—CH=CH2两者分子式不同,所含官能团也不同,前者是炔烃,后者是二烯烃,没有互称关系。
E. 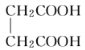 与
与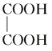 ,两者所含官能团的种类和个数相同,分子组成上相差2个亚甲基,属于同系物关系。
,两者所含官能团的种类和个数相同,分子组成上相差2个亚甲基,属于同系物关系。
F.戊烯与环戊烷,两者分子式均为C5H10,前者是链状烯烃,后者是环状烷烃,结构不同,互为同分异构体。
(1)上述各组化合物中属于同系物的是BE;属于同分异构体的是AF,故答案为:BE;AF。
(2)上述A中两化合物的含氧官能团是醛基和羰基,故答案为:醛基;羰基。
(3)根据官能团的特点C中两种化合物划分为酚类和醇类,故答案为:酚;醇。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ:二氧化碳的回收利用是环保领域研究的热点课题。
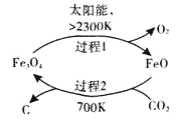
(1)以CO2为原料制取炭黑的流程如图所其总反应的化学方程式为________,
(2)CO2经过催化氢化合成低碳烯烃。其合成乙烯的反应为2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g) ΔH几种物质的能量(在标准状况下,规定单质的能量为 0,测得其他物质在生成时所放出或吸收的热量)如下表所示:
CH2=CH2(g)+4H2O(g) ΔH几种物质的能量(在标准状况下,规定单质的能量为 0,测得其他物质在生成时所放出或吸收的热量)如下表所示:
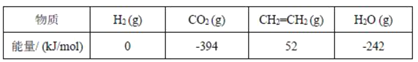
则ΔH=____。
Ⅱ:已知:①2C(s)+O2(g)=2CO(g) ΔH=-220kJ·mol-1;②氢气燃烧的能量变化示意图:
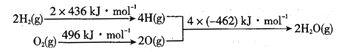
请写出碳和水蒸气反应,生成 CO和H2的热化学方程式:_______
Ⅲ:向100mL0.1mol·L-1 稀 NaOH溶液中加入稀盐酸,“中和热”或“反应放出热量”与所加入的盐酸体积的关系图正确的是(________)
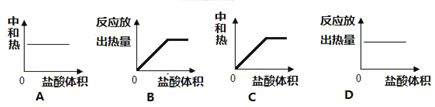
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】As2O3(砒霜)是两性氧化物(分子结构如图所示),溶于盐酸生成AsCl3,AsCl3用LiAlH4还原生成AlH3。下列说法正确的是( )
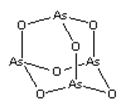
A.As2O3 分子中As原子的杂化方式为sp2
B.LiAlH4为共价化合物
C.AsCl3空间构型为平面正三角形
D.AlH3分子键角大于109.5°
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO![]() 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是
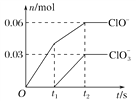
A. 反应中转移电子的物质的量是0.21 mol
B. ClO![]() 的生成可能是由于温度升高引起的
的生成可能是由于温度升高引起的
C. 标准状况下有3.36 L氯气参加反应
D. 苛性钾溶液中KOH的物质的量为0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对工业废气进行脱硝有多种方法。
(1)用活性炭还原法处理氮氧化物的反应为C(s)+2NO(g)![]() N2(g)+CO2(g)。一定条件下按下表所示条件向体积固定的容器中充入物质发生该反应。
N2(g)+CO2(g)。一定条件下按下表所示条件向体积固定的容器中充入物质发生该反应。
容器 | 温度 | 体积 | C(s) | NO(g) | N2(g) | CO2(g) |
甲 | 600℃ | V L | 1mol | 2mol | 0 | 0 |
乙 | 600℃ | V L | 0 | 0 | 2mol | 2mol |
①下列能说明甲容器中反应达到平衡状态的是_______。
a.容器的压强保持不变 b.v(NO)正=2v(CO2)逆
c.混合气体的密度保持不变 d.NO、N2、CO2的物质的量之比为2∶1∶1
②关于平衡时的甲、乙两容器,下列说法一定正确的是_______。
a.p(甲)=p(乙) b.c(NO)甲=c(CO2)乙
c.2c(CO2)甲=c(N2)乙 d.体积分数φ(CO2)甲=φ(N2)乙
(2)氮氧化物与悬浮在大气中的海盐粒子相互作用生成亚硝酰氯(ClNO),涉及反应如下:4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K1 ;2NO2(g)+NaCl(s)
2NaNO3(s)+2NO(g)+Cl2(g) K1 ;2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K2;2NO(g)+Cl2(g)
NaNO3(s)+ClNO(g) K2;2NO(g)+Cl2(g)![]() 2ClNO(g) K3;则K1、K2 、K3之间的关系为K3=_______
2ClNO(g) K3;则K1、K2 、K3之间的关系为K3=_______
(3)利用O3进行如下脱硝反应:2NO2(g)+O3(g)![]() N2O5(g)+O2(g) ΔH<0。其他条件一定时,NO2(g)的平衡转化率随温度和压强的变化情况如下图甲所示。X表示_______(填“压强”或“温度”),L1_______L2(填“<”或“>”)。
N2O5(g)+O2(g) ΔH<0。其他条件一定时,NO2(g)的平衡转化率随温度和压强的变化情况如下图甲所示。X表示_______(填“压强”或“温度”),L1_______L2(填“<”或“>”)。
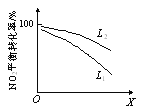
(4)用稀硝酸吸收NOx进行脱硝,得到HNO3和HNO2(弱酸)的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiCoO2(钴酸锂)是锂离子电池的正极材料。以某海水为原料制备钴酸锂的一种流程如下:
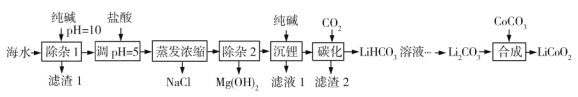
已知如下信息:
①该海水中含浓度较大的LiCl,含少量MgCl2、CaCl2、MnCl2等。
②碳酸锂的溶解度与温度关系如图所示:

③常温下,几种难溶物质的溶度积数据如下:
物质 | Li2CO3 | MgCO3 | CaCO3 | MnCO3 | Mg(OH)2 |
Ksp | 2.5×102 | 6.8×106 | 2.8×109 | 2.3×1011 | 6.0×1010 |
请回答下列问题:
(1)LiCoO2中钴的化合价为________。滤渣1主要成分有MgCO3、Mg(OH)2、CaCO3和__________(填化学式)。
(2)调节pH=5的目的是__________。
(3)“沉锂”包括过滤、洗涤等,宜用_________(填“热水”或“冷水”)洗涤Li2CO3。加入纯碱的量与锂回收率的关系如表所示:
序号 |
| 沉淀质量/g | 碳酸锂含量/% | 锂回收率/% |
① | 0.9∶1 | 10.09 | 92.36 | 77.67 |
② | 1.0∶1 | 10.97 | 90.19 | 82.46 |
③ | 1.1∶1 | 11.45 | 89.37 | 85.27 |
④ | 1.2∶1 | 12.14 | 84.82 | 85.45 |
从生产成本考虑,宜选择_______(填序号)方案投料。
(4)“除杂2”中调pH=13时c(Mg2+)=_________mol·L-1。
(5)“合成”中采用高温条件,放出一种能使澄清石灰水变浑浊的气体。写出“合成”发生反应的化学方程式________。
(6)在“合成”中制备1 mol LiCoO2转移电子的物质的量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应A2(?)+2B2(g) ![]() 2AB2(g) ΔH,在其他条件不变,改变某一条件时得到如下图象,下列对应图象叙述不正确的是
2AB2(g) ΔH,在其他条件不变,改变某一条件时得到如下图象,下列对应图象叙述不正确的是
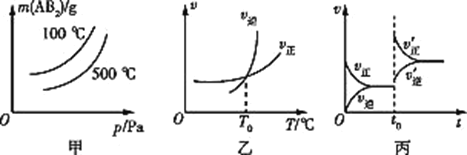
A.由图甲可知,A2为气体
B.由图甲可知,ΔH<0
C.由图乙可知,T=T0 ℃时,该可逆反应达到平衡状态
D.由图丙可知,t=t0时,改变的条件可能是增加了B2的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在①、②、③容积不等的恒容密闭容器中,均充入0.1molCO和0.2molH2,在催化剂的作用下发生反应:CO(g)+2H2(g)![]() CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示。下列说法正确的是
CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示。下列说法正确的是
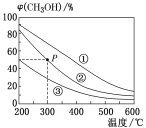
A.该反应的正反应为吸热反应
B.三个容器的容积:①>②>③
C.在P点,CO的转化率为75%
D.在P点,向容器②中再充入CO、H2及CH3OH各0.025mol,此时υ正(CO)<υ逆(CO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com