
【题目】As2O3(砒霜)是两性氧化物(分子结构如图所示),溶于盐酸生成AsCl3,AsCl3用LiAlH4还原生成AlH3。下列说法正确的是( )
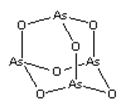
A.As2O3 分子中As原子的杂化方式为sp2
B.LiAlH4为共价化合物
C.AsCl3空间构型为平面正三角形
D.AlH3分子键角大于109.5°
【答案】D
【解析】
A.As2O3分子中形成了3个As-O共价键,As原子上还有一对孤电子对,As原子是杂化轨道数目为4,所以As原子的杂化方式为sp3杂化,A错误;
B.LiAlH4为离子化合物,阳离子是Li+,阴离子为AlH4-,B错误;
C.AsCl3中有3个σ键,孤电子对数为![]() =1,As原子为sp3杂化,含有一个孤电子对,所以空间构型为三角锥形,C错误;
=1,As原子为sp3杂化,含有一个孤电子对,所以空间构型为三角锥形,C错误;
D.AsH3分子中As原子价层电子对个数为3+![]() =4,且含有1个孤电子对,所以该分子为三角锥形,孤电子对对成键电子对之间的排斥力大于成键电子对之间的斥力,而AlH3中无孤电子对,所以键角大于109.5°,D正确;
=4,且含有1个孤电子对,所以该分子为三角锥形,孤电子对对成键电子对之间的排斥力大于成键电子对之间的斥力,而AlH3中无孤电子对,所以键角大于109.5°,D正确;
故合理选项是D。


科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是
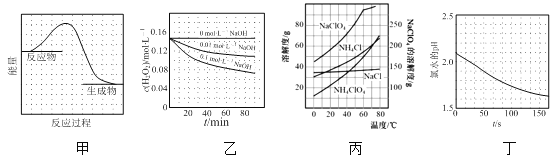
A.图甲表示某反应过程中的能量变化曲线,可推知该反应是吸热反应
B.图乙表示70℃时不同碱性条件下H2O2的浓度随时间变化的曲线,可推知溶液碱性越强,H2O2分解速率越慢
C.图丙表示部分物质的溶解度随温度变化的曲线,可推知20℃时向含a mol NaClO4的饱和溶液中加入a mol NH4Cl固体会有NH4ClO4固体析出
D.图丁表示光照下氯水的pH随时间的变化曲线,可推知光照后溶液中Cl2浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。
(1)按系统命名法给下列有机物命名:
①(CH3)2CHCH(Cl)CH3:___。
②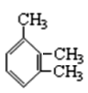 :___。
:___。
(2)羟基的电子式是:___。
(3)2-甲基-1-丁烯的键线式:___。
(4)相对分子质量最小的有机物空间构型是___。
(5)3-甲基戊烷的一氯代产物有___种(考虑立体异构)。
(6)高分子化合物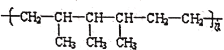 的单体分别是___。
的单体分别是___。
(7)写出下列有机反应的方程式:
①2-溴丙烷的水解反应:___。
②3-甲基-2-丁醇的催化氧化反应:___。
③实验室制乙烯:___。
④对苯二甲酸和乙二醇的缩聚反应:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
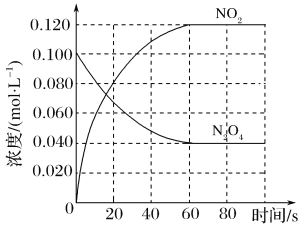
该反应ΔH______0(填“>”、“<”或“=”),在0~60 s时段,反应速率v(N2O4)为________mol·L-1·s-1。平衡常数K=________________(请书写单位)。在温度不变的情况下向平衡体系中再充入N2O4 0.01mol·L-1和NO20.03mol·L-1此时v(正)___________v(逆)(填“>”、“<”或“=”)。有利于提高反应N2O4(g) ![]() 2NO2(g)平衡转化率的条件是________(填标号)。
2NO2(g)平衡转化率的条件是________(填标号)。
A.高温低压 B.低温高压
C.高温高压 D.低温低压
(2)在一定温度下,向a L密闭容器中加入1 molN2O4(g)发生如下反应:N2O4(g) ![]() 2NO2(g),不能说明该反应一定达平衡的是__________。
2NO2(g),不能说明该反应一定达平衡的是__________。
A.容器内压强不随时间变化
B.容器内各物质的浓度不随时间变化
C.容器内O2、NO、NO2的浓度之比为1:2:2
D.单位时间内生成1 mol N2O4(g),同时生成2 mol NO2
E.混合气体的密度不随时间变化
F.混合气体的颜色不随时间变化
(3)在体积都为1 L,pH都等于2的盐酸和醋酸溶液中,投入0.65 g锌粒,则如图所示符合客观事实的是__________
A. 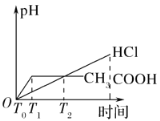 B.
B. 
C. 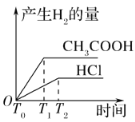 D.
D. 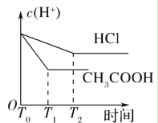
(4)25 ℃时,一元弱酸HA溶液Kal=4.3×10-4 ,一元弱酸HB溶液Ka2=5.6×10-4则酸性HA____________HB(填“>”、“<”或“=”)。
(5)常温下0.001mol·L-1的H2SO4溶液与0.004mol·L-1的NaOH溶液1:1体积比混合,混合后溶液的pH=_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液,经测定含有Al3+、Br-、SO42-,且各离子物质的量浓度相等(不考虑水电离出来的H+和OH-),则对该溶液的说法合理的是( )
A.可能含有![]() B.可能含有
B.可能含有![]() C.一定含有
C.一定含有![]() D.至少含有四种离子
D.至少含有四种离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应的快慢和限度对人类生产生活有重要的影响。800℃时,A、B、C三种气体在恒容密闭容器中反应时的浓度变化如图所示,回答下列问题:

(1)该反应的生成物是________。
(2)2min内,C的反应速率为________。
(3)该反应的化学方程式为________。
(4)在其他条件下,测得A的反应速率为![]() ,此时的反应速率与800℃时相比_____。
,此时的反应速率与800℃时相比_____。
A.比800℃时慢 B.比800℃时快 C.和800℃时速率一样
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
A.如图表示某放热反应分别在有、无催化剂的反应过程
B.如图表示2NO2(g)![]() N2O4(g) ΔH<0的v逆 随时间变化曲线,t1时刻改变的条件是降低温度
N2O4(g) ΔH<0的v逆 随时间变化曲线,t1时刻改变的条件是降低温度
C.如图表示反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0的平衡常数K随压强的变化
2NH3(g) ΔH<0的平衡常数K随压强的变化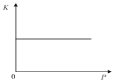
D.如图表示电解精炼铜过程中阳极质量随时间的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列各化合物:
A.CH3CH2CH2CHO与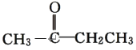
B.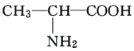 与
与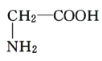
C. ![]() 与
与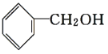
D.CH3CH≡CH与CH2=CH—CH=CH2
E. 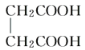 与
与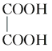
F.戊烯与环戊烷
(1)上述各组化合物中属于同系物的是________,属于同分异构体的是________(填字母)。
(2)上述A中两化合物的含氧官能团是__________和 __________(写名称)。
(3)根据官能团的特点可将C中两种化合物划分为________类和________类。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对反应A+B=AB来说,常温下按以下情况进行反应:
①20 mL溶液中含A、B各0.01 mol
②50 mL溶液中含A、B各0.05 mol
③0.1 mol·L-1的A、B溶液各10 mL
④0.5 mol·L-1的A、B溶液各50 mL
四者反应速率的大小关系是
A.②>①>④>③B.④>③>②>①
C.①>②>④>③D.①>②>③>④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com