
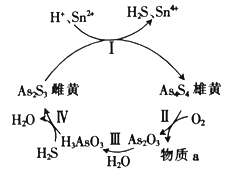
【题目】As和P属于同主族元素,它们都能形成多种含氧酸。中国自古就有“信口雌黄”“雄黄入药”之说。雌黄(As2S3)和雄黄(As4S4)早期都曾用作绘画颜料,又都因有抗病毒疗效而用来入药。在一定条件下,雌黄和雄黄的转化关系如图所示。
(1)亚磷酸(H3PO3)是一种精细化工产品。亚磷酸(H3PO3)与足量NaOH溶液反应生成Na2HPO3。
①则亚磷酸为___(填“一”“二”或“三”)元酸。
②查阅资料知25℃时,亚磷酸(H3PO3)的Ka1=5×10-2,Ka2=2.5×10-7,Na2HPO3可使碘水褪色,25℃时,Na2HPO3水解反应的Kh=____,若向Na2HPO3溶液中加入少量的I2,则溶液中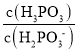 将__(填“增大”、“减小”或“不变”)
将__(填“增大”、“减小”或“不变”)
(2)反应II中,若0.5molAs4S4参加反应,转移14 mol电子,则物质a为__(填化学式)
(3)反应Ⅲ中的产物亚砷酸H3AsO3可以用于治疗白血病,其在溶液中存在多种微粒形态。常温下,用NaOH溶液滴定H3AsO3时,各种微粒的物质的量分数随pH的变化如图所示。
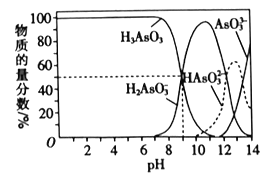
以酚酞为指示剂,将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为红色时停止滴加。该过程中主要反应的离子方程式为___。
【答案】二 4×10-8 增大 SO2 OH-+H3AsO3=H2AsO3-+H2O
【解析】
(1) ①亚磷酸(H3PO3)与足量NaOH溶液反应生成NaHPO3,说明亚磷酸(H3PO3)只能电离两个氢离子与氢氧化钠反应,故为二元酸;答案:二。
②25℃时,Na2HPO3水解反应为HPO32-+H2O= H2PO3-+OH-,所以水解常数为Kh=c(H2PO3-)c(OH-)/c(HPO32-)= c(H2PO3-)c(OH-)c(H+)/c(HPO32-) c(H+)=KW/ Ka2=10-14/2.5×10-7= 4×10-8。因为Na2HPO3可使碘水褪色,所以若向Na2HPO3溶液中加入少量的I2,c(H2PO3-)减小,HPO32-+H2O= H2PO3-+OH-平衡正向移动,进而促进第二步的水解H2PO3-+H2O= H3PO3+OH-,所以溶液中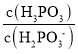 将增大;所以答案:4×10-8;增大。
将增大;所以答案:4×10-8;增大。
(2)由题知As4S4与氧气反应生成AS2O3和物质a,0.5molAs4S4参加反应,转移14 mol 电子,其中As元素转移电子数为2mol,故S转移电子数为12mol,故S从-2价变成+4价,故物质a为SO2。答案:SO2。
(3)①根据图知,碱性条件下H3AsO3的浓度减小、H2AsO3浓度增大,说明碱和H3AsO3生成H2AsO3,该反应为酸碱的中和反应,同时还生成水,离子方程式为OH-+H3AsO3=H2AsO3-+H2O
故答案为:OH-+H3AsO3=H2AsO3-+H2O


科目:高中化学 来源: 题型:
【题目】反应mA(s)+nB(g) ![]() eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是
eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图,下列叙述正确的是

A. 到平衡后,加入催化剂则C%增大
B. 化学方程式中n<e+f
C. 达到平衡后,若升温,平衡左移
D. 达到平衡后,增加A的量有利于平衡向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组进行了有关Cu、硝酸、硫酸化学性质的实验,实验过程如下图所示。下列有关说法正确的是
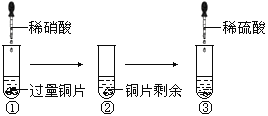
A. 实验①中溶液呈蓝色,试管口有红棕色气体产生,说明稀硝酸被Cu还原为NO2
B. 实验③中滴加稀硫酸,铜片继续溶解,说明稀硫酸的氧化性比稀硝酸强
C. 实验③发生反应的化学方程式为:3Cu+Cu(NO3)2+4H2SO4=4CuSO4+2NO↑+4H2O
D. 由上述实验可得出结论:Cu在常温下既可以和稀硝酸反应,也可以和稀硫酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种生产聚苯乙烯的流程如下,下列叙述不正确的是( )
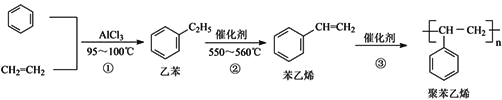
A. 乙烯可由石油裂解得到,苯可由煤的干熘得到,两者均发生了化学变化
B. 乙苯和氢气加成后的产物的一氯代物有5种
C. 鉴别乙苯与聚苯乙烯不可用Br2的四氯化碳溶液
D. 乙烯和聚苯乙烯均可以和H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2与CH4的反应使之转化为CO 和H2,对减缓燃料危机,减少温室效应具有重要的意义。
(1)已知该转化反应为CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ΔH,则加快该反应的化学反应速率,应采用的有效措施有___________________________(填写两种)。
2CO(g)+2H2(g) ΔH,则加快该反应的化学反应速率,应采用的有效措施有___________________________(填写两种)。
(2)在密闭容器中通入物质的量浓度均为0.1 mol·L-1的CH4与CO2,在一定条件下发生反应CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ΔH,测得CH4的平衡转化率与温度、压强的关系如下图所示。
2CO(g)+2H2(g) ΔH,测得CH4的平衡转化率与温度、压强的关系如下图所示。

①由图可知,该反应的ΔH_____0 (填写“大于”或者“小于”),P1、P2、P3、P4由大到小的顺序为_________________________。
②工业生产时一般会选用P4和1250℃进行合成,请解释其原因______________________________。
③在压强为P4、1100℃的条件下,该反应5min时达到平衡点X,则用CO表示该反应的速率为_________________mol·L-1·min-1。
④该温度下,反应的平衡常数K的数学表达式为K=_______,经计算K的数值为K=_____________(保留3位有效数字),若要使K减小可采取的措施是_________________。
(3)CO和H2在工业上还可以通过反应C(s)+H2O(g) ![]() CO(g)+H2 (g)来制取。
CO(g)+H2 (g)来制取。
① 在恒温恒容下,如果从反应物出发建立平衡,可认定已达平衡状态的是_______________
A. H2、CO和H2O的物质的量之比为1:1:1 B.体系压强不再变化
C. 气体平均相对分子质量不变 D.混合气体的密度保持不变
② 在某密闭容器中同时投入四种物质,2min时达到平衡,测得容器中有1mol H2O(g)、1mol CO(g)、2.2molH2(g)和一定量的C(s),如果此时对体系加压,平衡向_______(填“正”或“逆”)反应方向移动,达到新的平衡后,气体的平均摩尔质量为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)键线式![]() 的名称是_____________________。
的名称是_____________________。
(2)C5H12的某种同分异构体只有一种一氯代物,写出它的结构简式_____________。
(3)某芳香烃结构为![]() ,其一氯代物有_________种。
,其一氯代物有_________种。
(4)写出由2-溴丙烷和必要的无机试剂制取1,2-丙二醇的化学反应方程式(有几步就写几个方程式):____________________。
(5)有机物A只含有C、H、O三种元素,常用作有机合成的中间体。16.8g该有机物燃烧生成44.0 g CO2和14.4 g H2O;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O—H键和位于分子链端的C≡C键,核磁共振氢谱上有三个峰,峰面积之比为6:1:1。
①A的分子式为___________,A的结构简式为_____________。
②有机物B是A的同分异构体,1 mol B 可与1 mol Br2加成,该有机物中所有碳原子在同一个平面上,没有顺反异构现象,B的结构简式是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)13.8g氮的氧化物(NOx)中含N原子数为0.3mol,则NOx的摩尔质量为___,x的数值为___,该质量的NOx在标准状况下的体积为___L。
(2)某待测液中可能含有Ag+、Fe3+、K+、Ba2+、NH4+等离子,进行如下实验:① 加入过量的稀盐酸,有白色沉淀生成;② 过滤,得无色透明溶液,在滤液中加入过量的稀硫酸,又有白色沉淀生成;③ 过滤,取少量滤液,加入NaOH溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:待测液中一定含有___离子;—定不含有__离子;还有____离子不能确定是否存在,要检验这些离子的实验方法是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们将有机物中连有四个不同原子(或原子团)的碳原子称为手性碳原子,如图所示烷烃X中含有一个手性碳原子(用*标记)。含有手性碳原子的物质通常具有光学活性。回答下列问题:

(1)烷烃X的名称是_____________;其一氯代物共有__________种(不考虑立体异构,下同)。
(2)具有光学活性且相对分子质量最小的烷烃的分子式是__________,其有__________种符合条件的结构。
(3)某芳香烃A可经过如下反应得到一种热塑性塑料SAN(两种单体1:1共聚产物)。

写出SAN的结构简式:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑,下列说法正确的是( )
MnCl2+2H2O+Cl2↑,下列说法正确的是( )
A.MnO2是还原剂
B.HCl 是氧化剂
C.若生成7.1gCl2,则转移0.1 mol电子
D.若生成7.1gCl2,被氧化的盐酸的物质的量是0.2mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com