
【题目】将等体积、等物质的量浓度的醋酸与氢氧化钠溶液混合后,溶液呈(填“酸性”、“中性”或“碱性”.下同.)溶液中C(Na+)C(CH3COO)(填“大于”、“小于”或“等于”.下同.)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】150℃时,NH4HCO3分解为NH3、H2O,CO2三种物质,此时该混合气的密度是相同条件下的氢气密度的()
A. 13.2倍B. 26.3倍C. 15.25倍D. 12倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示(B中冷却装置未画出),将氯气和空气(不参与反应)以体积比约1:3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O制备次氯酸溶液.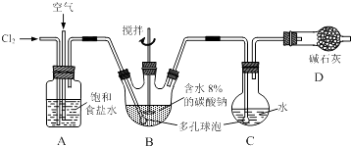
已知:Cl2O极易溶于水并与水反应生成HClO;Cl2O的沸点为3.8℃,42℃以上分解为Cl2和O2 .
(1)①实验中控制氯气与空气体积比的方法是 .
②为使反应充分进行,实验中采取的措施有 .
(2)①装置B中产生Cl2O的化学方程式为: .
②若B无冷却装置,则进入C中的Cl2O会大量减少.其原因是 .
(3)装置C中采用棕色圆底烧瓶是因为 .
(4)已知次氯酸可被H2O2、FeCl2等物质还原成Cl﹣ . 测定C中次氯酸溶液的物质的量浓度的实验方案为:用取20.00mL次氯酸溶液, . (可选用的试剂:H2O2溶液、FeCl2溶液、AgNO3溶液.除常用仪器外须使用的仪器有:电子天平,真空干燥箱)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应热的叙述中正确的是( )
①已知2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJmol﹣1 , 则氢气的燃烧热为△H=﹣241.8kJmol﹣1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)═Z(g)+W(s)△H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
④已知:
共价键 | C﹣C | C═C | C﹣H | H﹣H |
键能/(kJmol﹣1) | 348 | 610 | 413 | 436 |
上表数据可以计算出 ![]() (g)+3H2(g)→
(g)+3H2(g)→ ![]() (g)的反应热;
(g)的反应热;
⑤由盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1molCO2固体时,放出的热量相等;
⑥25℃,101kPa时,1mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热.
A.①②③④
B.③④⑤
C.④⑤
D.⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)2Z(g);△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
A.0~2 min的平均速率v(Z)=2.0×10﹣3 molL﹣1min﹣1
B.其他条件不变,降低温度,反应达到新平衡前 v(正)<v(逆)
C.该温度下此反应的平衡常数K=144
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜与稀硫酸不发生反应,但如果在铜与稀硫酸的混合溶液中加入某种盐,就能使铜溶解,且有气体产生,则该盐是:( )
A. Na2CO3 B. KNO3 C. CuCl2 D. BaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质的说法中正确的是( )
A. 石墨能导电,所以石墨是电解质
B. 碳酸钙在水中的溶解度很小,但溶解的部分全部电离,所以碳酸钙为电解质
C. 二氧化碳的水溶液都能导电,所以它们都是电解质
D. 水难电离,纯水几乎不导电,所以水是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的分类组合正确的是( )
分类组合 | 酸 | 碱 | 盐 | 非金属氧化物 | 金属氧化物 |
A. | C2H5OH | Ca(OH)2 | K2CO3 | CO2 | CaO |
B. | HNO3 | NaHCO3 | Na2SO4 | CuO | MgO |
C. | NH3 | Ba(OH)2 | MgCl2 | P2O5 | CaO |
D. | CH3COOH | NaOH | CaCO3 | SO2 | Mn2O7 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5 , 反应PCl5(g)PCl3(g)+Cl2(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是( )
A.反应在前50s的平均速率为v(PCl3)=0.0032molL﹣1s﹣1
B.保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11molL﹣1 , 则反应的△H<0
C.相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20mol Cl2 , 达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0mol PCl3、2.0mol Cl2 , 达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com