
【题目】下列有关反应热的叙述中正确的是( )
①已知2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJmol﹣1 , 则氢气的燃烧热为△H=﹣241.8kJmol﹣1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)═Z(g)+W(s)△H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
④已知:
共价键 | C﹣C | C═C | C﹣H | H﹣H |
键能/(kJmol﹣1) | 348 | 610 | 413 | 436 |
上表数据可以计算出 ![]() (g)+3H2(g)→
(g)+3H2(g)→ ![]() (g)的反应热;
(g)的反应热;
⑤由盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1molCO2固体时,放出的热量相等;
⑥25℃,101kPa时,1mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热.
A.①②③④
B.③④⑤
C.④⑤
D.⑥
【答案】D
【解析】解:①燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,氢气燃烧生成液态水,由热化学方程式可知,氢气的燃烧热<﹣241.8kJmol﹣1 , 故错误;
②单质A转化为单质B是一个吸热过程,则B的能量比A的高,能量越高越不稳定,故错误;
③一定条件下,反应热与平衡移动无关,与化学计量数与物质的状态有关,故错误;
④反应热=反应物总键能﹣生成物总键能,由于苯环中不存在碳碳双键,不能计算反应热,故错误;
⑤金刚石与石墨的结构不同,能量不相同,在相同条件下,金刚石或石墨燃烧生成1molCO2固体时,放出的热量不相等,故错误;
⑥碳的燃烧热指:25℃,101kPa时,1mol碳完全燃烧生成CO2所放出的热量,故正确,
故选D.


科目:高中化学 来源: 题型:
【题目】下列电离方程式不正确的是( )
A.醋酸溶于水:CH3COOH═CH3COO﹣+H+
B.Na2SO4溶于水:Na2SO4═2Na++SO42﹣
C.碳酸氢钠溶于水:NaHCO3═HCO3﹣+Na+
D.次氯酸溶于水:HClOH++ClO﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为防止有机物挥发,可加一层水保存,即水封。下列有机物中,既能用水封法保存,又能发生水解和消去反应的是
A.乙醇B.溴乙烷C.乙酸乙酯D.四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X位于第四周期,其基态原子有4个未成对电子.Y原子最外层电子数是其内层电子总数的3倍,元素Z基态原子的3p轨道上有4个电子.
(1)Y与Z可形成多种化合物. ①元素Y与Z中电负性较大的是(用元素符号描述).
②离子ZY32﹣的空间构型为(用文字描述).
③写出一种与ZY2互为等电子体的氧化物分子的化学式 .
(2)Y的氢化物(H2Y)在乙醇中的溶解度大于H2Z,其原因是 .
(3)含X2+的溶液与KCN、氨水反应可得到化合物K3[X(CN)5(NH3)]. ①基态X2+的电子排布式是
②1mol配合物K3[X(CN)5(NH3)]中含σ键的数目为 .
(4)下图为X与Z所形成的一种化合物的基本结构单元,推测该化合物的化学式: . 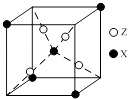
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HIO4主要以H5IO6形式存在,H5IO6是白色晶体,易溶于水,具有很强的氧化性,在强酸溶液中能氧化Mn2+。
(1)请完成并配平下列离子反应。
__________Mn2++________H5IO6![]() __________
__________![]() +________
+________![]() +________H++________
+________H++________
(2)根据以上离子方程式判断H5IO6是________电离物质(填“易”或“难”)。
(3)上述反应,被氧化的元素是________(填元素符号),当1 mol Mn2+参加反应时,转移电子的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在测定硫酸铜晶体结晶水含量的实验中,会导致测定结果偏低的是( )
A.加热后固体发黑
B.坩埚沾有受热不分解的杂质
C.加热时有少量晶体溅出
D.晶体中混有受热不分解的杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等体积、等物质的量浓度的醋酸与氢氧化钠溶液混合后,溶液呈(填“酸性”、“中性”或“碱性”.下同.)溶液中C(Na+)C(CH3COO)(填“大于”、“小于”或“等于”.下同.)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下,Ksp(AgCl)=1.56×10﹣10 , Ksp(Ag2CrO4)=1×10﹣12 . 下列关于该温度下的叙述正确的是( )
A.向氯化银的悬浊液中加入氯化钠溶液,Ksp(AgCl) 减小
B.饱和AgCl溶液与饱和Ag2CrO4溶液相比,前者的c(Ag+)大
C.若向0.0008 molL﹣1的K2CrO4溶液中加入等体积0.002 molL﹣1的AgNO3溶液,则CrO42﹣完全沉淀(提示:沉淀完全c(CrO42﹣)≤10﹣5 molL﹣1)
D.若将0.001 molL﹣1 AgNO3溶液滴入浓度均为0.001 molL﹣1的KCl和K2CrO4混合溶液中,则先产生AgCl沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于溶液和胶体的叙述正确的是( )
A. 溶液呈电中性,而胶体是带电的,因而胶体可以产生电泳现象
B. 通电时,溶液溶质粒子移向两极,而胶体分散质移向同一极
C. 纳米碳的直径在1nm-100nm之间,因此其属于胶体
D. 三角洲的形成、夜晚霓虹灯、明矾净水及土壤保肥等均与胶体的性质有关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com