
| A�� | ����C��s��+H2O��g��?CO��g��+H2��g����Ӧ����һ�������´ﵽƽ�⣬���ӻ����C��s������ƽ�ⲻ�ƶ� | |
| B�� | ����2SO2��g��+O2��g��?2SO3��g����Ӧ�����ܶȱ��ֲ��䣬�ں��º��ݻ���º�ѹ�����£���������Ϊ�ﵽ��ѧƽ��״̬�ı�־ | |
| C�� | ����C��s��+CO2��g��?2CO��g����Ӧ�����ܶȱ��ֲ��䣬�ں��º��ݻ���º�ѹ�����£�������Ϊ�ﵽ��ѧƽ��״̬�ı�־ | |
| D�� | ����I2��g��+H2��g��?2HI��g����Ӧ���������������ѹǿ�������̴ﵽƽ������ʱ�䣬��HI�İٷֺ������ֲ��� |
���� A��CΪ��̬���ı���������Ӱ�컯ѧƽ�⣻
B�����º��������£��ܶ�ʼ�ղ��䣬�����º�ѹ�������ܶ�Ϊ������
C��CΪ���壬��Ӧǰ����������������仯������º��ݺͺ��º�ѹ�������ܶȶ��DZ�����
D���÷�ӦΪ�����������Ŀ��淴Ӧ��ѹǿ�ʹ���Ӱ�췴Ӧ���ʣ���Ӱ�컯ѧƽ�⣮
��� �⣺A������C��s��+H2O��g��?CO��g��+H2��g����Ӧ������CΪ���壬��һ�������´ﵽƽ�⣬���ӻ����C��s����������ѧƽ�ⲻ�ƶ�����A��ȷ��
B�����ڷ�Ӧǰ��������������䣬�ں��º��ݣ����Ի��������ܶ�ʼ�ղ��䣬���ܶȲ����ж��Ƿ�ﵽ��ƽ��״̬�������º�ѹ�����£����������ܶ������ܶȱ��ֲ��䣬��Ӧ�ﵽƽ��״̬�������º�ѹ���ܶȿ�����Ϊ�ﵽ��ѧƽ��״̬�ı�־����B����
C��C��״̬Ϊ��̬����Ӧǰ��������������ȣ��ں��º��������£����������ܶ��������ﵽƽ��״̬ʱ�������л��������ܶȲ��䣻�����º�ѹ�����£��淴Ӧ���У���ϵ���������������CO2��CO���ʻ��������ܶ���С�����ܶȱ��ֲ��䣬��Ӧ�ﵽƽ�⣬��C��ȷ��
D����ӦI2��g��+H2��g��?2HI��g���У���Ӧǰ�����������ȣ�ѹǿ��Ӱ�컯ѧƽ�⣬��������������ѹǿ���ܼӿ췴Ӧ���ʣ����̴ﵽƽ������ʱ�䣬��HI�İٷֺ������ֲ��䣬��D��ȷ��
��ѡB��
���� ���⿼���˻�ѧƽ���Ӱ�죬��Ŀ�Ѷ��еȣ���ȷ��ѧƽ�⼰��Ӱ������Ϊ���ؼ���BCΪ�״��㣬ע�����ջ�ѧƽ��״̬���������жϷ���������������ѧ�������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
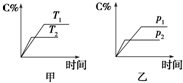 ���淴ӦA������+aB��g��?C��g��+D��g��������aΪ����������Ӧ�����У���������������ʱ��C�İٷֺ�����C%�����¶ȣ�T����ѹǿ��p���Ĺ�ϵ��ͼ��ʾ���Իش��������⣺
���淴ӦA������+aB��g��?C��g��+D��g��������aΪ����������Ӧ�����У���������������ʱ��C�İٷֺ�����C%�����¶ȣ�T����ѹǿ��p���Ĺ�ϵ��ͼ��ʾ���Իش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪�����ڷ�Ӧ��H2��g��+Cl2��s���T2HCl ��g����H=-a kJ/mol�� ��  ��a��b��c�������㣬��Ͽ�1molH-Cl�����������Ϊ-a-b-c | |
| B�� | ��2C��s��+O2��g���T2CO��g����H=-221.0 kJ/mol����̼��ȼ����Ϊ110.5 kJ/mol | |
| C�� | ��Ҫ���ȵķ�Ӧһ�������ȷ�Ӧ���������ܷ����ķ�Ӧһ���Ƿ��ȷ�Ӧ | |
| D�� | ��ͼ�ɱ�ʾˮ�ֽ�����е������仯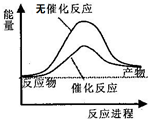 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| t/min | 2 | 4 | 7 | 9 |
| n��H2O��/mol | 0.12 | 0.11 | 0.10 | 0.10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��֪ ��� | ��ʼ״̬���ʵ���/mol | ƽ��ʱNH3�� ���ʵ���/mol | ||
| N2 | H2 | NH3 | ||
| 1 | 4 | 0 | a | |
| �� | 1.5 | 9 | 0 | ��1.5a |
| �� | 0 | 0.5 | 1 | 0.5a |
| �� | m | g��g��4m�� | 0 | am����$\frac{ag}{4}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C��s��+$\frac{1}{2}$O2��g��=CO��g������H1 C��s��+O2��g��=CO2��g������H2 | |
| B�� | $\frac{1}{2}$H2��g��+$\frac{1}{2}$Cl2��g��=HCl��g������H1 H2��g��+Cl2��g��=2HCl��g������H2 | |
| C�� | S��g��+O2��g��=SO2��g������H1 S��s��+O2��g��=SO2��g������H2 | |
| D�� | 2H2��g��+O2��g��=2H2O��g������H1 2H2��g��+O2��g��=2H2O��l������H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| 50g | 20g | 20g | 10g | 5g |
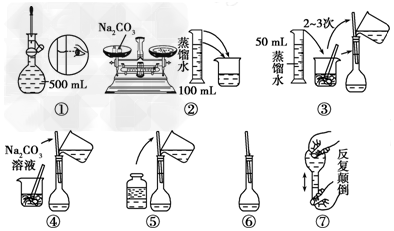
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��ѧʽ | CH3COOH | HCN |
| ����ƽ�ⳣ�� | 1.8��10-5 | 4.9��10-10 |
| A�� | �����pH��ͬ��CH3COOH��Һ��HCN��Һ���ֱ���������Fe��Ӧ��HCN��Һ������H2���� | |
| B�� | �����pH��ͬ��CH3COOH��Һ��HCN��Һ���к�NaOH��Һ������NaOH�����ʵ�����ͬ | |
| C�� | amol•L-1HCN��Һ��ˮϡ�ͺ���ƽ�ⳣ����С������KCN�������ƽ�ⳣ������ | |
| D�� | 25��ʱ���ڵ�Ũ�ȵ�CH3COOH��Һ��HCN��Һ�У�ˮ�ĵ���̶�ǰ�ߴ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com