
【题目】甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。
(1)甲醇脱氢法可制备甲醛(反应体系中各物质均为气态),结合下图回答问题。

①此反应的热化学方程式是______
②反应活化能:过程I___过程II(填“>”“=”或“<”)
③过程II温度—转化率图如下,下列说法合理的是_____

a.甲醇脱氢法制备甲醛过程无副反应发生
b.温度高于 650℃催化剂烧结,活性减弱
c.及时分离产品有利于提高甲醇生成甲醛的转化率
(2)甲醛超标会危害人体健康,需对甲醛进行含量检测及污染处理。
①某甲醛气体传感器的工作原理如图所示,b极的电极反应式为____,当电路中转移4×10-4 mol电子时,传感器内参加反应的甲醛(HCHO)为_____mg。

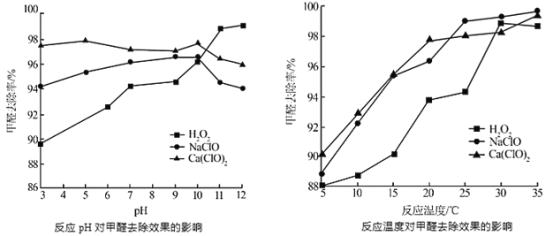
②氧化剂可处理甲醛污染,结合以下图像分析春季(水温约15℃)应急处理甲醛污染的水源应选择的试剂为______
【答案】CH3OH(g)=HCHO(g)+H2(g)⊿H=+84kJ/mol > b、c HCHO-4e-+ H2O= CO2+ 4H+ 3 Ca(ClO)2
【解析】
(1)①由图可知1molCH3OH脱氢生成1molHCHO和1molH2要吸收能量463kJ/mol-379kJ/mol=84kJ/mol,据此写出热化学方程式;
②由图可知反应活化能:过程I>过程II;
③a.由图可知,甲醇转化率大于甲醇生成甲醛的转化率,说明有其它副反应发生;
b.由图可知,温度高于 650℃甲醇生成甲醛的转化率降低,说明催化剂烧结,活性减弱;
c.减小生成物浓度平衡向正反应方向移动,所以及时分离产品有利于提高甲醇生成甲醛的转化率;
(2)①由图可知,甲醛气体传感器为原电池原理,b极为负极,甲醛发生氧化反应生成CO2,以此书写电极反应式;根据电极反应式计算反应的甲醛的量。
②分析图像可知,水温约15℃时选择Ca(ClO)2处理甲醛污染的水源,甲醛去除率较高。
(1)①由图可知1molCH3OH脱氢生成1molHCHO和1molH2要吸收能量463kJ/mol-379kJ/mol=84kJ/mol,所以反应的热化学方程式是CH3OH(g)=HCHO(g)+H2(g)⊿H=+84kJ/mol,
故答案为:CH3OH(g)=HCHO(g)+H2(g)⊿H=+84kJ/mol;
②由图可知反应活化能:过程I>过程II,
故答案为:>;
③a.由图可知,甲醇转化率大于甲醇生成甲醛的转化率,说明有其它反应发生,所以甲醇脱氢法制备甲醛过程有副反应发生,故a错误;
b.由图可知,温度高于 650℃甲醇生成甲醛的转化率降低,说明催化剂烧结,活性减弱,故b正确;
c.减小生成物浓度平衡向正反应方向移动,所以及时分离产品有利于提高甲醇生成甲醛的转化率,故c正确。
故答案为:b、c;
(2)①由图可知,甲醛气体传感器为原电池原理,b极为负极,甲醛发生氧化反应生成CO2,电极反应式为HCHO-4e-+ H2O= CO2+ 4H+;由反应式可知,当电路中转移4×10-4 mol电子时,传感器内参加反应的甲醛(HCHO)为![]() 30g/mol=3
30g/mol=3![]() 10-3g=3mg。
10-3g=3mg。
②分析图像可知,水温约15℃时选择Ca(ClO)2处理甲醛污染的水源,甲醛去除率较高,且甲醛去除率受pH的影响不大;
故答案为:3;Ca(ClO)2。


科目:高中化学 来源: 题型:
【题目】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。下列说法错误的是( )

A. zh3中各原子最外层都达到8e-稳定结构
B. y与g可形成化合物yg2,结构式为g=y=g
C. d和f形成的简单离子半径大小关系为:d2- < f3+
D. f 和h 形成的化合物属于离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.如图为原电池装置示意图。

(1)若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,写出B电极反应式:__________。该电池在工作时,A电极的质量将_______(填“增加”“减小”或“不变”),若该电池反应消耗了0.1 mol H2SO4,则转移电子的数目为________。
(2)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为氢氧燃料电池,写出A电极反应式:_____________________________。该电池在工作一段时间后,溶液的碱性将________(填“增强”“减弱”或“不变”)。
Ⅱ.现用图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为1000 mL,供选择的电极材料有纯铜片和纯锌片。

(3)b电极材料为________,其电极反应式为_________________________。
(4)当量筒中收集到560 mL(标准状况下)气体时,通过导线的电子的物质的量为________mol,此时a电极质量________(填“增加”或“减少”)________g。
(5)如果将a、b两电极的电极材料对调,U形管中将出现的现象是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如下:(所加试剂均过量,气体全部逸出)
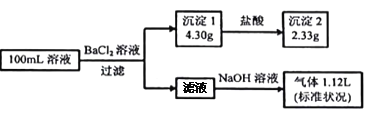
下列说法不正确的是
A. 原溶液一定存在CO32-和SO42-,一定不存在Fe3+
B. 若原溶液中不存在Na+,则c(Cl-)<0.1mol·L-1
C. 原溶液中c(Cl-)≥0.1mol·L-1
D. 原溶液一定存在Cl-,可能存在Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列实验的描述正确的是

A. 图甲所示的实验:根据溶液颜色变化可比较Zn、Cu的金属活动性
B. 图乙所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀
C. 图丙所示的实验:根据温度计读数的变化用浓硫酸和NaOH反应测定中和热
D. 图丁所示的实验:根据两烧瓶中气体颜色的变化判断2NO2(g)N2O4(g)是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,有![]() 盐酸;
盐酸;![]() 硫酸;
硫酸;![]() 醋酸三种酸的稀溶液
醋酸三种酸的稀溶液![]() 用a、b、c、
用a、b、c、![]() 、
、![]() 、
、![]() 号填写
号填写![]()
![]() 当其物质的量浓度相同时,
当其物质的量浓度相同时,![]() 由大到小的顺序是____________,
由大到小的顺序是____________,
![]() 同体积同物质的量浓度的三种酸,中和NaOH能力由大到小的顺序是____________,
同体积同物质的量浓度的三种酸,中和NaOH能力由大到小的顺序是____________,
![]() 当其
当其![]() 相同时,物质的量浓度由大到小的顺序为____________,
相同时,物质的量浓度由大到小的顺序为____________,
![]() 当
当![]() 相同、体积相同时,同时加入形状、质量、密度相同的锌,若产生相同体积的氢气
相同、体积相同时,同时加入形状、质量、密度相同的锌,若产生相同体积的氢气![]() 相同状况
相同状况![]() ,则开始时反应速率的大小关系是____________.
,则开始时反应速率的大小关系是____________.
![]() 将
将![]() 相同的三种酸均加水稀释至原来的10倍,
相同的三种酸均加水稀释至原来的10倍,![]() 由大到小的顺序为_____________.
由大到小的顺序为_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列六种短周期元素(用字母x等表示)。最高正价或最低负价与原子序数关系如图所示。

根据判断出的元素回答问题:
(1)f在周期表中的位置是______。已知x为非金属元素,由x、e、g三种元素组成的离子化合物的电子式:______。
(2)上述元素简单离子半径最大的是(用化学式表示,下同):___;比较g、h的最高价氧化物对应水化物的酸性强弱:_____。
(3)已知1mole的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式:__________。
(4)x和d组成的化合物中,既含有极性共价键又含有非极性共价键的是____(填化学式),此化合物可将碱性工业废水中的CN-氧化,生成碳酸盐和氨气,相应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在一恒容密闭容器中,能表示反应 X(g)+2Y(g)![]() 2Z(g) 一定达到化学平衡状态的是
2Z(g) 一定达到化学平衡状态的是
①容器中气体的密度不再发生变化
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成2n mol Z,同时消耗2n mol Y
A. ①② B. ②③ C. ③④ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,N4分子结构与白磷分子相似,呈正四面体结构。已知断裂1molN—N键吸收193 kJ热量,断裂1molN≡N键吸收941 kJ热量,则1mol N4气体转化为N2时要__________填“吸收”或“放出”)热量________________ kJ。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com