
【题目】将1 mol CH4和适量的氧气在密闭容器中点燃,充分反应后,甲烷和氧气均无剩余,且产物均为气体(101 kPa,120℃),其总质量为72 g,下列有关叙述不正确的是( )
A.产物的平均摩尔质量为24 g/mol
B.反应中消耗的氧气为56 g
C.若将产物通过浓硫酸充分吸收后恢复至(101 kPa,120℃),则压强变为原来的三分之一
D.若将产物通过碱石灰,则可全被吸收,若通过浓硫酸,则不能被完全吸收
【答案】D
【解析】
1mol CH4若完全燃烧产生1mol的CO2和2mol的H2O,其质量是80g,若燃烧产生1mol的CO和2mol的H2O,其质量是64g,现在混合物的质量是72 g,则产物中含有CO、CO2、H2O,根据质量守恒定律可知,其中CO和CO2的物质的量之和为1mol,H2O的物质的量为2mol。
A.根据元素守恒可知产物的物质的量是3mol,质量是72g,故产物的平均摩尔质量=![]() =24 g/mol,A正确;
=24 g/mol,A正确;
B.1 mol CH4质量为16g,生成物为72g,根据质量守恒定律可知反应中消耗的氧气为72g-16g=56g,B正确;
C.若将产物通过浓硫酸充分吸收后恢复至(101 kPa,120℃),则水被吸收,由分析可知,气体的物质的量变成原来的三分之一,压强也变为原来的三分之一,C正确;
D.若将产物通过碱石灰,由分析可知,生成物中的CO与碱石灰不能发生反应,所以其不能被吸收,若通过浓硫酸,浓硫酸只能吸收水,所以也不能被完全吸收,D错误。
答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有甲、乙、丙三种溶液,进行如下操作:则甲、乙、丙三种溶液可能是( )
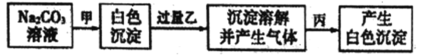
A.BaCl2、H2SO4、MgCl2B.BaCl2、HCl、Na2SO4
C.CaCl2、HNO3、NaClD.CaCl2、HNO3、BaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟离子电池是一种前景广阔的新型电池,其能量密度是目前锂电池的十倍以上且不会因为过热而造成安全风险.如图是氟离子电池工作示意图,其中充电时 F-从乙电极流向甲电极,下列关于该电池的说法正确的是
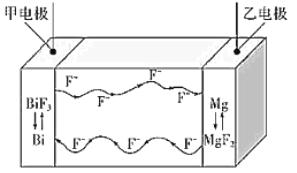
A.放电时,甲电极的电极反应式为 Bi-3e-+3F-=BiF3
B.充电时,导线上每通过1 mol e-,甲电极质量增加 19 g
C.放电时,乙电极电势比甲电极高
D.充电时,外加电源的正极与乙电极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)物质X的产量通常用来衡量一个国家的石油化工水平。以X为主要原料合成重要的有机化合物路线如下图所示,请回答下列问题。

(1)X所含官能团的名称是______________,A物质所含官能团的名称是________。
(2)反应③的化学方程式是_______________,以乙烯为原料可合成有机高分子化合物D,反应①的化学方程式是____________________,该反应属于______反应(填有机反应类型)。
(3)下列物质中,不能通过乙烯加成反应得到的是________(填序号)。
a. CH3CH3 b. CH3CHCl2 c. CH3CH2Br
(4)葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用下图所示装置制备乙酸乙酯:

①试管a中生成乙酸乙酯的化学方程式是______。
②实验开始时,试管b中的导管不伸入液面下的原因是______。
③反应结束后,将试管b中的混合液经过____(填写实验分离操作)可得到纯净的乙酸乙酯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25°C,改变0.01 mol·L一1 CH3COONa溶液的pH.溶液中c(CH3COOH)、c(CH3COO-)、c(H +)、c(OH- )的对数值lgc与溶液pH的变化关系如图所示,下列叙述正确的是
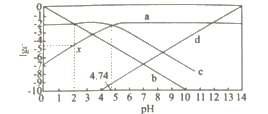
A.图中任意点均满足c(CH3COOH)+c(CH3COO-)=c(Na+)
B.0.01 mol·L-1CH3COOH的pH约等于线a与线c交点处的横坐标值
C.由图中信息可得点x的纵坐标值为4.74
D.25°C时,![]() 的值随 pH的增大而增大
的值随 pH的增大而增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
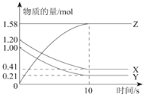
A.反应的化学方程式为: X(g)+Y(g)![]() Z(g)
Z(g)
B.反应开始到10s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y的转化率为79.0%
D.温度、体积不变,10s时充入1 mol He使压强增大,正、逆反应速率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加德罗常数的值,下列说法正确的是
A. 16.25gFeCl3水解形成的Fe(OH)3胶体粒子数为0.1NA
B. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
C. pH=1的H3PO4溶液中,含有0.1NA个H+
D. 10 g的D2O中含有的质子数与中子数分别为5NA和4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向铜片中加入某浓度的硫酸120ml,在加热条件下反应,待铜片全部溶解后,将其溶液稀释到500ml。再加入足量锌粉,使之充分反应,收集到标准状况下氢气2.24L,过滤残留固体,干燥后称量,质量减轻了7.50g。求:
(1)溶解的铜的质量。______
(2)原硫酸的物质的量浓度。(要求写出简要计算过程)_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe3O4中含有Fe(Ⅱ)、Fe(Ⅲ),以Fe3O4/Pd为催化材料,可实现用H2消除酸性废水中的致癌物NO2-,其反应过程如图所示。下列说法正确的是( )
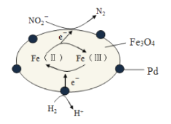
A.Pd作正极
B.Fe(Ⅱ)与Fe(Ⅲ)的相互转化起到了传递电子的作用
C.反应过程中NO2-被Fe(Ⅱ)氧化为N2
D.用该法处理后水体的pH降低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com