
【题目】有一种有机化合物,其结构简式如下,下列有关它的性质叙述中,正确的是( )
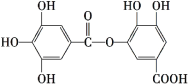
A.酸性条件下 能发生水解反应,水解后能生成两种物质
B.在一定条件下,1 mol该物质最多能与7 mol NaOH完全反应
C.在一定条件下,1 mol该物质可以和8 mol H2发生加成反应
D.有弱酸性,能与NaHCO3溶液反应
科目:高中化学 来源: 题型:
【题目】国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污和生态环境保护与调水作为一个完整的系统来分析的原则。在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患。经检测,某工厂废液中含有大量的![]() 、
、![]() 、
、![]() 、
、![]() 。试分析并回答下列问题:
。试分析并回答下列问题:
(1)该废液中可能大量存在的阴离子是________(填序号)。
A ![]() B
B ![]() C
C ![]() D
D ![]()
(2)为了回收废液中的金属银,某同学设计了如图所示的实验方案。若按照该方案获得金属银108g,在保证不污染环境且![]() 循环利用的情况下,可得出理论上应提供标准状况下的
循环利用的情况下,可得出理论上应提供标准状况下的![]() ________L。
________L。
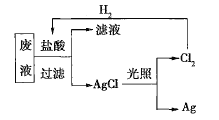
(3)为了实现(2)中氯气的循环利用,有人设想以氢气和氯气为原料利用原电池原理直接制盐酸,假设这种想法可行,下列说法肯定错误的是________(填序号)。
A 两极材料都用石墨,用稀盐酸作电解质溶液
B 通入氢气的电极为原电池的正极
C 电解质溶液中的阳离子向通入氯气的电极移动
D 通入氯气的电极的电极反应式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一固体混合物,可能由![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 混合而成,为检验它的成分,做了如下实验:
混合而成,为检验它的成分,做了如下实验:![]() 已知
已知![]() 不能被稀
不能被稀![]() 氧化,
氧化,![]() 微溶于水
微溶于水![]()
![]() 将固体溶于足量水,搅拌后静置,得到无色透明溶液和白色沉淀;
将固体溶于足量水,搅拌后静置,得到无色透明溶液和白色沉淀;
![]() 取等量固体加入足量的稀硝酸中,有刺激性气味黄绿色气体产生,同时有白色沉淀生成。根据以上实验现象,你认为以下判断正确的是
取等量固体加入足量的稀硝酸中,有刺激性气味黄绿色气体产生,同时有白色沉淀生成。根据以上实验现象,你认为以下判断正确的是![]()
![]()
A.一定含有![]() 、
、![]() 、
、![]()
B.无法判断是否含有![]()
C.一定含有![]() 、
、![]() 、
、![]() ,不能肯定是否含有
,不能肯定是否含有![]()
D.是否含![]() ,只要把实验
,只要把实验![]() 产生的气体通入少量澄清石灰水中,若没有变浑浊,则一定不含
产生的气体通入少量澄清石灰水中,若没有变浑浊,则一定不含![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,CH3COOH的电离平衡常数Ka=1.75×10-5,NH3·H2O的电离平衡常数Kb=1.75×10-5,现在25 ℃时向10 mL浓度均为0.1 mol·L-1的HCl和CH3COOH的混合溶液中逐滴加入0.1 mol·L-1的氨水,溶液的pH变化曲线如图所示。下列有关说法不正确的是( )
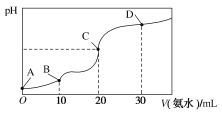
A.A点到B点,溶液的导电性逐渐减小
B.整个过程中,C点处水的电离程度最大
C.pH =7时对应的点应在C点和D点之间,此时溶液中存在:c(NH4+)=c(CH3COO-)+c(CH3COOH)
D.D点处:c(NH4+)>c(Cl-)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体混合物溶于水,所得溶液中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的几种离子,且各种离子的物质的量相同。为了确定其组成,进行如下实验:
中的几种离子,且各种离子的物质的量相同。为了确定其组成,进行如下实验:
(1)取一定量的样品,加足量水充分溶解,得到澄清溶液。
(2)取少量溶液,滴入足量稀硝酸,再滴入足量硝酸钡溶液,有沉淀生成;充分振荡,静置,向上层清液中滴入硝酸银溶液,有沉淀生成。
(3)再取少量![]() 中溶液,加入氢氧化钠溶液,有沉淀生成。
中溶液,加入氢氧化钠溶液,有沉淀生成。
根据上述实验现象,该固体样品的成分可能是
A.该混合物一定是NaCl和![]()
B.该混合物一定是NaCl和![]()
C.该混合物可能是![]() 和
和![]()
D.该混合物可能是![]() 和
和![]() 3
3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25C时,0.1mol/L的3种溶液①盐酸②氨水③CH3COONa溶液。下列说法中,不正确的是
A. 3种溶液中pH最小的是①
B. 3种溶液中水的电离程度最大的是③
C. ①与②等体积混合后溶液显酸性
D. ①与③等体积混合后c(Na+)>c(Cl-)>c(H+)>c(CH3COO-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga_____________As,第一电离能Ga____________As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_____________________。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGag·mol-1和MAs g·mol-1,原子半径分别为rGapm和rAspm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。
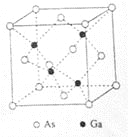
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物结构,性质和应用的说法中,不正确的是![]()
![]()
A.环己烷与溴混合振荡后,在光照条件下可以发生取代反应
B.裂化汽油可以使溴水褪色和酸性![]() 褪色,且原理相同
褪色,且原理相同
C.苯的二氯代物、四氯代物的同分异构体数相等
D.燃烧等物质的量的乙烯、乙醇,消耗氧气的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于2SO2(g)+O2(g) 2SO3(g),ΔH<0,根据下图,下列说法错误的是( )

A.t2时使用了催化剂B.t3时采取减小反应体系压强的措施
C.t5时采取升温的措施D.反应在t6时刻,SO3体积分数最大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com