
【题目】已知化学反应①:Fe(s)+CO2(g)![]() FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)![]() FeO(s)+H2(g),其化学平衡常数为K2,在温度973 K和1173 K的情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其化学平衡常数为K2,在温度973 K和1173 K的情况下,K1、K2的值分别如下:
温度 | K1 | K2 |
973 K | 1.47 | 2.38 |
1 173 K | 2.15 | 1.67 |
(1)通过表格中的数值可以推断:反应①是_______(填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g)![]() CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=______。
CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=______。
(3)根据反应①与②可推导出K1、K2与K3之间的关系式为__________,据此关系式及上表数据,能推断出反应③是________(填“吸热”或“放热”)反应。
(4)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有______ 、_____ (填写字母序号)。
A.缩小反应容器的容积 B.扩大反应容器的容积
C.升高温度 D.使用合适的催化剂
E.设法减小平衡体系中的CO的浓度
(5)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:
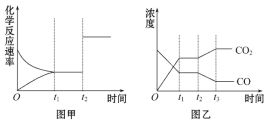
①图甲中t2时刻发生改变的条件是__________。
②图乙中t2时刻发生改变的条件是__________。
【答案】吸热 ![]() K3=K1/K2 吸热 CE 增大压强或使用催化剂 降低温度或设法分离出H2
K3=K1/K2 吸热 CE 增大压强或使用催化剂 降低温度或设法分离出H2
【解析】
(1)根据表中数据可知,升高温度,K1是增大的,说明升高温度平衡向正反应方向进行,所以反应①是吸热反应。
(2)平衡常数是在一定条件下,可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据方程式可知,平衡常数表达式是K3=![]() 。
。
(3)根据盖斯定律可知,①-②即得到反应③,所以K3=K1/K2;升高温度,K1增大,K2增减小,所以K3是增大,因此正反应是吸热反应。
反应③是体积不变的、吸热的可逆反应,所以要使平衡向正反应方向移动,则可以升高温度,或降低生成物的浓度等,但压强和催化剂不能改变平衡状态,答案选CE。
(5)①图甲中t2时刻正逆反应速率都增大,但平衡不移动,所以改变的条件是增大压强或使用催化剂。
②图乙中t2时刻CO2的浓度增大,而CO的浓度降低,即平衡向逆反应方向进行,所以改变的条件是降低温度或从体系中分离出H2。


科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都是短周期元素,原子序数依次增大,A、D同主族,B、C、D、E同周期,B、A可按原子个数比2:l和1:1分别形成两种离子化合物甲和乙,C是地壳中含量最高的金属元素。短周期中,B原子半径最大,E的最高价氧化物对应水化物酸性最强。
(1)E的最高价氧化物对应的水化物的分子式为________________;
(2)D与E可形成分子式为D2E2的物质,该物质为浅黄色油状液体,有特殊气味,是一种重要的工业添加剂。则D2E2的结构式为______________;
(3)B、C、D、E、A简单离子半径由大到小的顺序为_______________(用离子符号表示)
(4)用电子式表示化合物甲的形成过程________;
(5)C元素的单质能与B元素的最高价氧化物的水化物发生反应,写出该反应离子方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求在下列空格中填空。
(1)一定量的乙醇与苯的混合物与足量的金属钠反应,可生成11.2L氢气(在标准状况下),将此混合物燃烧能生成108g水。
①求混合物中苯的质量__________________
(2)某种烃A的蒸气折合成标况下的密度是3.214g/L,已知该烃的碳氢质量比为5∶1,求:
①该烃的相对分子质量:_________,
②如果该烃的一氯取代物有4种,写出该烃的结构简式:___________________________________________
(3)5.8g有机物完全燃烧,只生成CO2和H2O蒸气,其体积比为1:1(同压同温),若把它们通过碱石灰,碱石灰质量增加18.6g,同量的有机物与0.1mol乙酸完全发生酯化反应.又知该有机物对空气的相对密度为2。(注意:羟基不能直接连在双键上)
①有机物的分子式___________________________________________________________
②有机物的结构简式___________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化镁是优良的阻燃剂,同时在医药、建筑等行业的应用也十分广泛。用硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量SiO2、FeCO3等)为原料制备高纯氧化镁的实验流程如下:

已知在水溶液中生成氢氧化物沉淀的pH:
Mg(OH)2 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 9.4 | 7.6 | 1.5 |
完全沉淀时 | 10.4 | 9.7 | 2.8 |
(1)菱镁矿酸溶前需要粉碎,目的是_______________。
(2)加入H2O2氧化时,发生反应的离子方程式为______________________。
(3)加氨水调节溶液的pH范围为________ ,滤渣2 的主要成分是____________(填化学式)。
(4)流程图中在获得滤渣2的“过滤”与“煅烧”之间要经过的操作步骤为_______、过滤等操作,得到MgSO4·xH2O晶体。
(5)已知煅烧12.3gMgSO4·xH2O晶体得到2gMgO,则x值为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO![]() 2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/(10-4mol·L-1) | 10 | 4.5 | 2.5 | 1.5 | 1.0 | 1.0 |
c(CO)/(10-3mol·L-1) | 36.0 | 30.5 | 28.5 | 27.5 | 27.0 | 27.0 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1) 已知该反应ΔS<0,在上述条件下反应能够自发进行,则反应的ΔH________0(填写“>”“<”或“=”)。
(2)前2 s内的平均反应速率v(N2)=________。
(3)在该温度下,反应的平衡常数表达式K=________。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是________。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。已知A的气态氢化物能与其最高价氧化物的水化物反应得到一种离子化合物,B的一种单质具有杀菌消毒的作用,C+和D3+的电子层结构相同,E的主族序数是其周期序数的2倍。
(1)F在元素周期表中的位置是__________________。
(2)上述元素形成的简单离子中,半径最大的是____________(填离子符号)。
(3)由上述元素中的一种或几种组成的物质甲可以发生如下反应:

①若丙具有漂白性,则甲和水反应的离子方程式为__________________________。
②若乙的水溶液是强碱性溶液,物质丙为B的一种单质,则甲中含有的化学键的类型为________,D的单质与乙的水溶液反应的离子方程式为_________________。
③若甲为D和E形成的二元化合物,物质丙是气体,则丙的结构式为___________;物质乙为白色沉淀,其化学式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)+2ICl(g)![]() I2(g)+2HCl(g),该反应分①、②两步进行,其能量曲线如图所示,
I2(g)+2HCl(g),该反应分①、②两步进行,其能量曲线如图所示,
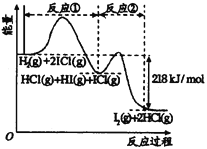
下列有关说法正确的是
A. 反应①为吸热反应
B. 反应①和②均是同种元素间发生的氧化还原反应
C. 反应①比反应②的速率慢,与相应正反应的活化能有关
D. HI(g)+ICl(g) ![]() I2(g)+HCl(g) △H=-218 kJ/mol
I2(g)+HCl(g) △H=-218 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是原子序数依次增大的五种短周期主族元素,其中A的原子序数是B和D原子序数之和的1/4,C元素的最高价氧化物的水化物是一种中强碱,甲和丙是D元素的两种常见氧化物,乙和丁是B元素的两种常见同素异形体,0.005mol/L戊溶液的pH=2,它们之间的转化关系如图所示(部分反应物省略),下列叙述正确的是
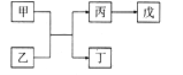
A. C、D两元素形成化合物属共价化合物
B. C和E形成的化合物的水溶液呈碱性
C. 简单离子半径D > B > C
D. E的氧化物水化物的酸性大于D的氧化物水化物的酸性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com