
【题目】磷化铝(AlP)通常可作为一种广谱性熏蒸杀虫剂,吸水后会立即产生高毒性PH3气体(沸点-89.7℃,还原性强)。某化学兴趣小组的同学用下述方法测定粮食中残留磷化物的含量。

在C中加入100g原粮,E中加入20.00mL 1.50×l0-3mol/L KMnO4溶液(H2SO4酸化),往C中加入足量水,充分反应后,用亚硫酸钠标准溶液滴定E中过量的KMnO4溶液。回答下列问题:
(1)仪器D的名称是________________________。
(2)AlP与水反应的化学方程式为__________________________________。
(3)装置A中盛装KMnO4溶液的作用是除去空气中的还原性气体,装置B中盛有焦性没食子酸( )的碱性溶液,其作用是_____________________________。
)的碱性溶液,其作用是_____________________________。
(4)通入空气的作用是____________________________________。
(5)装置E中PH3被氧化成磷酸,则装置E中发生反应的氧化剂和还原剂物质的量之比为______________。(6)收集装置E中的吸收液,加水稀释至250mL,取25.00mL于锥形瓶中,用4.0×10-4mol/L的Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液15.00mL,Na2SO3与KMnO4溶液反应的离子方程式为______________, 则该原粮中磷化物(以PH3计)的含量为_____ mg·kg-1。
【答案】 直形冷凝管(或冷凝管) AlP+3H2O=PH3↑+Al(OH)3 吸收空气中的O2 保证生成的PH3全部被酸性KMnO4溶液吸收 8:5 5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O [(20×10-3×1.50×10-3-15×10-3×4×10-4×2/5×250/25.00)×5/8×34×103]/ 100×10-3=1.275
【解析】(1)根据仪器的特点,仪器D的名称是直形冷凝管;(2)AlP与水反应生成磷化氢和氢氧化铝,反应的化学方程式为AlP+3H2O=PH3↑+Al(OH)3;(3)装置B中盛有焦性没食子酸(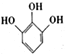 )的碱性溶液,其作用是吸收空气中的O2;(4)通入空气的作用是保证生成的PH3全部被酸性KMnO4溶液吸收;(5)装置E中PH3被氧化成磷酸,则装置E中发生反应5PH3+8MnO4-+24H+==5H3PO4+8Mn2++12H2O,其中MnO4-为氧化剂,PH3为还原剂,故氧化剂和还原剂物质的量之比为8:5;(6)酸性条件下Na2SO3与KMnO4溶液反应生成硫酸钠、硫酸锰和硫酸钾及水,反应的离子方程式为5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O;
)的碱性溶液,其作用是吸收空气中的O2;(4)通入空气的作用是保证生成的PH3全部被酸性KMnO4溶液吸收;(5)装置E中PH3被氧化成磷酸,则装置E中发生反应5PH3+8MnO4-+24H+==5H3PO4+8Mn2++12H2O,其中MnO4-为氧化剂,PH3为还原剂,故氧化剂和还原剂物质的量之比为8:5;(6)酸性条件下Na2SO3与KMnO4溶液反应生成硫酸钠、硫酸锰和硫酸钾及水,反应的离子方程式为5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O;![]() mg·kg-1。
mg·kg-1。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】现有下列三种溶液:①45%的乙醇溶液、②汽油和氯化钾溶液、③氯化钠和单质碘的水溶液,分离上述各组混合液的正确方法依次是( )
A.分液、萃取、蒸馏B.萃取、蒸馏、分液
C.分液、蒸馏、萃取D.蒸馏、分液、萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1120mL的烧瓶里充满NO2和O2的混合气体,然后将其倒扣于水槽中,可以看到液体充满烧瓶(气体体积已折算成标况下的体积),下列说法正确的是
A. NO2与O2的体积分别为896mL和224mL
B. 总反应式:NO2+O2+H2O=HNO3
C. 转移的电子数为0.02mol
D. 有NO气体生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所表示的方法研究金属钠与水反应的性质,其中A是用带孔的铝箔包着的小块的金属钠.

(1)从大块钠上取下的小块钠要用滤纸擦一擦,这样做的目的是_______________。
(2)包裹钠块的铝箔要预先扎上足够多的小孔,若孔数不够,可能出现的不良后果是__________.假如在实验刚开始就将镊子松开拿出水面,A表现出的现象是 _______________________,出现这种现象的原因是______________。
(3)据预测,钠与水反应生成氢气和氢氧化钠.
证明生成氢氧化钠的实验方法和相应的现象是______________________;
(4)已知反应结束后铝箔和钠均消失,请写出相关反应的离子方程式:______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知298K时,Ksp(NiS)=1.0×10-21,Ksp(NiCO3)=1.0×10-7 ;p(Ni)=-lg c(Ni2+),p(B)=-lg c(S2-)或-lg c(CO32-)。在含物质的量浓度相同的Na2S和Na2CO3的混合溶液中滴加Ni(NO3)2溶液产生两种沉淀,溶液中阳离子、阴离子浓度关系如图所示。下列说法错误的是

A. 常温下NiCO3的溶解度大于NiS的溶解度
B. 向d点对应的溶液中加入对应阴离子的钠盐,d点向b点移动
C. 对于曲线I,在b点加热,b点向c点移动
D. P为3.5且对应的阴离子是CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下所示:
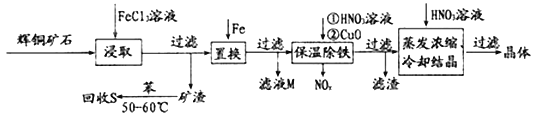
(1)“浸取”时,为了提高浸取速率可采取的措施有___________________________(任写一点)。写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:_____________________________________。
(2)“保温除铁”过程中,加入CuO的目的是_________________________________________;“蒸发浓缩、冷却结晶”过程中,加入HNO3调节溶液的pH,其理由是____________________。
(3)气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为________________________________。向“滤液M”中加入(或通入)_____ (填字母),可得到另一种可循环利用的物质。
a.铁 b.氯气 c.高锰酸钾
(4)“回收S”过程中温度控制在50 ~60℃之间,不宜过高或过低的原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体可能含有 Ba2+、NH4 + 、Cu2+、Na +、Cl -、CO32-、SO42-中的几种离子,取等质量的两份该固体,进行如下实验:
(1)一份固体溶于水得到无色透明溶液。加入足量的 BaCl2 溶液,得到沉淀 6.63g;在沉淀中加入过量 的稀盐酸,仍有 4.66g 沉淀。
(2)另一份固体与过量的 NaOH 固体混合后充分加热,产生气体 1.344L(标准状况)。已知NH4 + OH-=NH3↑H2O ,则下列说法正确的是( )
A. 该固体中一定只含有 NH4 + 、CO32-、SO42-
B. 该固体中一定没有Cu2+、Na +、Ba2+、Cl-
C. 该固体中一定含有NH4 + 、Na +、Cl -、CO32-、SO42-
D. 若该固体中含有 Na+,则一定含有 Cl-,且二者等量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】农药波尔多液可用于水果灭虫,是由石灰水和硫酸铜溶液混合而成的悬浊液。它不能用铁制容器盛放,是因为铁与该农药中的硫酸铜起反应。在该反应中,对铁的叙述错误的是( )
A. 铁发生还原反应B. 铁发生氧化反应
C. 铁是还原剂D. 铁失去电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适量铁粉放入三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等.则已反应的Fe3+和未反应的Fe3+的物质的量之比是( )
A.2:3
B.3:2
C.1:2
D.1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com