
【题目】某废液阳离子只可能含有:Na+、NH4+、Ba2+、Cu2+、Fe2+、Fe3+、Al3+中的某几种,实验设计了下述方案进行处理,以回收金属,保护环境
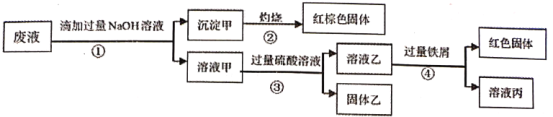
已知:步骤①中,滴加NaOH溶液过程中产生的沉淀会部分溶解,下列说法正确的是:
A.根据步骤①中的现象,说明废液中一定含有Al3+
B.步骤②,由红棕色固体可知,废液中一定存在Fe3+
C.取溶液丙进行焰色反应,焰色为黄色,说明原溶液中一定含Na+
D.该废液一定含有NH4+、Ba2+、Cu2+
【答案】D
【解析】
沉淀甲灼烧后为红棕色固体,该红棕色固体为Fe2O3,则沉淀甲可能为Fe(OH)2或Fe(OH)3,说明废液中可能含有Fe2+或Fe3+;溶液甲中加入过量硫酸溶液,产生固体乙,则固体乙为BaSO4,说明废液中一定含有Ba2+;溶液乙中加入过量铁屑,产生红色固体,该红色固体为Cu,说明废液中一定含有Cu2+,以此解答该题。
A.由步骤④可知,废液中一定含有Cu2+,而沉淀甲中没有Cu(OH)2,说明加入NaOH溶液后,Cu元素以离子形式存在于溶液甲中,则废液中一定含有NH4+,Cu元素以[Cu(NH3)4]2+形式存在于溶液甲中,因此步骤①沉淀部分溶解,不能说明废液中一定含有Al3+,故A错误;
B.由分析可知,废液中可能含有Fe2+或Fe3+,故B错误;
C.由于步骤①中加入过量NaOH溶液,因此溶液丙中一定含有Na+,焰色反应显黄色,不能说明废液中含有Na+,故C错误;
D.由分析可知,废液中一定含有Ba2+和Cu2+,由选项A的分析可知,废液中一定含有NH4+,故D正确;
故答案选D。


科目:高中化学 来源: 题型:
【题目】700℃时,H2(g)+CO2(g)![]() H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时,v(H2O)为0.025 mol/(L·min),下列判断不正确的是()
H2O(g)+CO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示。其中甲经2min达平衡时,v(H2O)为0.025 mol/(L·min),下列判断不正确的是()
起始浓度 | 甲 | 乙 | 丙 |
C(H2)/mol/L | 0.1 | 0.2 | 0.2 |
C(CO2)/mol/L | 0.1 | 0.1 | 0.2 |
A. 平衡时,乙中CO2的转化率大于50%
B. 当反应平衡时,丙中c(CO2)是甲中的2倍
C. 温度升至800℃,上述反应平衡常数为25/16,则正反应为吸热反应
D. 其他条件不变,若起始时向容器乙中充入0.10mol/L H2和0.20 mol/L CO2,到达平衡时c (CO)与乙不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中大多数元素是金属元素,金属及其化合物在生活生产中有着重要应用,根据试题信息,完成下列计算:
(1)某常见二价金属12.6g与足量稀硫酸反应,生成氢气5.04L(S.T.P),该元素原子的摩尔质量为__g/mol.
(2)39.32g某金属混合物,由12.32g镁和0.25mol另一种比镁不活泼的金属元素A组成,该混合物与一定量盐酸反应,产生氢气4.928L(S.T.P),则参加反应的HCl为__mol,金属A的相对原子质量为__.
(3)由NaCl、NaHCO3、Na2CO310H2O组成的混合物157.8g,充分加热后,产生的气体(气体温度150℃)依次通过无水CaCl2和碱石灰,两种吸收剂分别增重59.4g和13.2g,则混合物中NaHCO3的质量分数为___,若等质量的该混合物与足量盐酸反应,产生二氧化碳(S.T.P)__L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化为吸热反应的是
A.H2O(l)=H2O(g);ΔH=+44.0 kJ/mol
B.在高温条件下碳与水蒸气的反应
C.形成化学键时共放出能量862 kJ的化学反应
D.能量变化如图所示的化学反应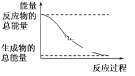
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或试剂的选择都合理的是
A.减压过滤时,常用倾析法先转移上部清液,溶液量不超过漏斗容量的2/3,慢慢开大水龙头,待溶液快流尽时再转移下部沉淀
B.用酸性高锰酸钾溶液检验FeCl2和FeCl3混合液中的Fe2+
C.用NaOH溶液除去溶在乙酸乙酯中的乙酸
D.向CoCl2溶液中逐滴加入浓盐酸并振荡,溶液的颜色会从蓝色逐渐变成粉红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对乙酰氨基苯酚X是常用的非甾类消炎解热镇痛药。可用如下路线来合成:
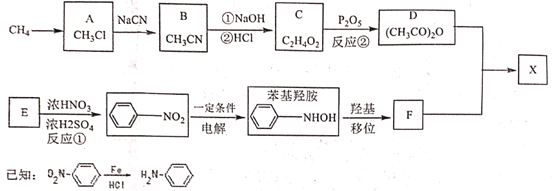
请回答下列问题:
(1)下列说法正确的是:_____________
A 反应①②皆为取代反应 B 有机物D能与水反应生成C
C F既能与强酸反应又能与强碱反应 D X分子中含有酚羟基和肽键两种官能团
(2)X与足量氢氧化钠反应的化学方程式:_____________。
(3)分析F分子结构特点和X合成原理后,认为制得X中有某种副产物,请写出该副产物的结构简式:___
(4)写出同时满足下列条件的X的所有同分异构体的结构简式:__________
①分子中含有-NH2;
②与氯化铁溶液发生显色反应;
③苯环上的取代基不超过3个且苯环上只有两种不同环境的H
(5)请设计以甲苯为原料合成![]() 的路线(用流程图表示,无机物任选)__________
的路线(用流程图表示,无机物任选)__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四期某些过渡元素在工业生产中有着极其重要的作用。
(1)铬是最硬的金属单质,被称为“不锈钢的添加剂”。
写出Cr在周期表中的位置___________;其原子核外电子排布的最高能层符号___________.
(2)在1 mol CrO5(其中Cr为+6价)中,含有过氧键的数目为___________。
(3)钒(23V)是我国的丰产元素,被称之为“工业的味精”,广泛用于催化及钢铁工业。回答下列问题:
写出钒原子价电子排布图___________;V2O5常用作SO2转化为SO3的催化剂。SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为___________;

(4)Ni是一种优良的有机反应催化剂,Ni能与CO形成正四面体形的配合物Ni(CO)4,其中配原子是___________。
(5)钛称之为21世纪金属,具有一定的生物功能。钙钛矿(CaTiO3)晶体是工业获取钛的重要原料。 CaTiO3晶胞如下图,边长为a=0.266m,晶胞中Ti、Ca、O分别处于顶角、体心、面心位置。Ti与O间的最短距离为___________nm,与Ti紧邻的O个数为___________。

(6)在CaTiO3晶胞结构的另一种表示中,Ca处于各顶角位置,则T处于___________位置,O处于___________位置。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20gA全部溶于0.15L 6.0molL-1盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12L(标况)气体。同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检查时,溶液D不变色。
请填空:
(1)①中引发铝热反应的实验操作是_________________________________________,产物中的单质是___________。
(2)②中所发生的各反应的化学方程式是_______________________________________。
(3)③中所发生的各反应的离子方程式是 _________________________。
(4)若溶液D的体积仍视为0.15L,则该溶液中c(Mg2+)为 _______________。c(Fe2+)为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的△H前者大于后者的是( )
①C(s)+O(g)=CO(g)△H1;C(s)+![]() O2(g)=CO(g)△H2
O2(g)=CO(g)△H2
②S(s)+O2(g)=SO2(g)△H3;S(g)+O2(g)=SO2(g)△H4
③H2(g)+![]() O2(g)=H2O(l)△H5;2H2(g)+O2(g)=2H2O(l)△H6
O2(g)=H2O(l)△H5;2H2(g)+O2(g)=2H2O(l)△H6
④CaCO3(s)=CaO(s)+CO2(g)△H7;CaO(s)+H2O(l)=Ca(OH)2(s)△H8
A.①B.④C.②③④D.①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com