
| A、常温常压下,2.24L H2O2气体中含有的分子数为0.1×6.02×1023 |
| B、46 g NO2和N2O4混合气体中含有原子数为3NA |
| C、100 mL 0.2 mol/L的Fe2(SO4)3溶液中,含有的Fe3+数为0.1×0.2×6.02×1023 |
| D、25℃时,纯水中含有的H+数为1×10-7×6.02×1023 |
| 46g |
| 46g/mol |


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:
| A、原子序数A>B |
| B、电子总数A>B |
| C、离子半径A->B2+ |
| D、原子半径A>B |
查看答案和解析>>
科目:高中化学 来源: 题型:
235 92 |
235 92 |
| A、表示铀元素的一种原子 |
| B、表示铀元素的一种核素 |
| C、质量数是235,原子序数是92,核内有147个质子 |
| D、质量数是235,原子序数是92,核内有147个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
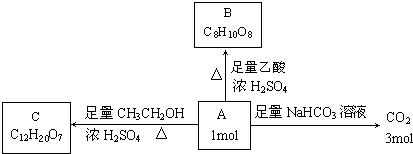
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将浓度为0.1mol?L-1HF溶液加水不断稀释过程中,c(H+)和c(OH-)都会减小 |
| B、常温下,为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的PH,若PH>7,则H2A是弱酸;若PH<7,则H2A是强酸 |
| C、将SO2通入一定量的KOH溶液,所得溶液呈中性,该溶液中一定含KHSO2 |
| D、用0.2000mol?L-1NaOH标准溶液滴定浓度均为0.1mol?L-1的HCl与CH3COOH的混合液,至中性时,溶液中的酸恰好被完全中和 |
查看答案和解析>>
科目:高中化学 来源: 题型:
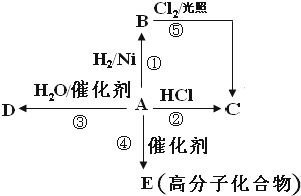
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com