
【题目】下列说法正确的是
A. 有能量变化的过程均为化学变化
B. 氢氧化钡晶体与氯化铵晶体的反应为放热反应
C. 反应物的总能量高于生成物的总能量时发生放热反应
D. 旧化学键断裂所放出的能量低于新化学键形成所吸收的能量时发生吸热反应
科目:高中化学 来源: 题型:
【题目】从物质A开始有如下图所示的转化关系(其中部分产物已略去)。已知H能使溴的CCl4溶液褪色;1mol F(分子式C4H6O2)与足量新制的Cu(OH)2在加热条件下充分反应可生成2molCu2O。分析图表并回答问题:
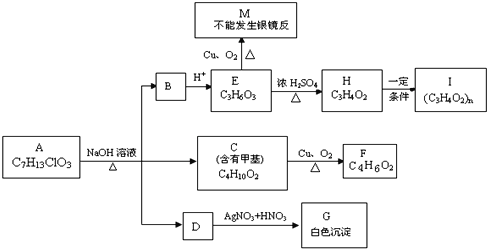
(1)A可能的结构简式:_______________________________________________;
(2)写出反应类型: E→H_________________、H→I__________________;
(3)写出C→F的化学方程式:__________________________。
(4)请设计出由丙烯合成CH3-CH(OH)-COOH的反应流程图_______(有机物用结构简式表示,必须注明反应条件)。提示:合成过程中无机试剂任选。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的说法正确的是
A. 能生成碱的金属元素都在ⅠA族
B. 稀有气体元素原子的最外层电子数均为8
C. 第二周期ⅣA族元素的原子核电荷数和中子数一定为6
D. 原子序数为14的元素位于元素周期表的第3周期ⅣA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl―→2KCl+5Cl2↑+2MnCl2+8H2O

对实验现象的“解释或结论”正确的是 ( )
选项 | 实验现象 | 解释或结论 |
A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
C | d处立即褪色 | 氯气与水生成了漂白性物质 |
D | e处变红色 | 还原性:Fe2+>Cl- |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微型化学实验可以有效实现化学实验绿色化的要求。如下图所示在一块衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol/L的KI(含淀粉溶液)、NaOH的酚酞(C20H14O4)试液、FeCl2(含KSCN)溶液各一滴,在圆心处放置一粒芝麻大小的KMnO4的晶体,向KMnO4的晶体上滴加一滴浓盐酸,再立即用表面皿盖好根据上述描述涉及到的元素,回答下列问题:
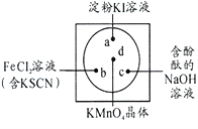
(1)a中反应的化学反应方程式为________________________________________证明KI中含有钾元素的方法是:____________________________。
(2)c中反应的离子反应方程式为_______________________________________b中的现象是________________________________________________。
(3)短周期原子半径最大的原子共有______种不同能量的电子。它与同周期原子半径最小元素形成晶体,该晶体中每个阳离子周围距离最近有_______个阴离子。
(4)把少许 KMnO4撒入盛水烧杯中溶解,包含物理过程(即__________过程和化学过程(即_____________过程。所以,溶液中的有色离子应该是__________________(写名称)
(5)NH3与H2O分别能与H+结合成NH4+与H3O+。与NH4+具有相同空间构型的微粒是_______;
a.H3O+b.CH4c.P4d.NH3
(6)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)1000kg,若用KI与 Cl2反应制KIO3,至少需要消耗Cl2___________________L(标准状况,保留2位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库。下图是从海水中提取食盐和溴的主要流程。

(1)粗盐除含 NaCl 外,还含有少量 MgCl2、 CaCl2、 Na2SO4以及泥沙等杂质。以下是粗盐提纯的
操作流程。

提供的试剂:
Na2CO3溶液、 K2CO3溶液、 NaOH 溶液、 BaCl2溶液、 Ba(NO3)2溶液、饱和 NaCl 溶液。
①除去溶液 I 中的 MgCl2、 CaCl2、 Na2SO4,从提供的试剂中选出 a 所代表的试剂,按滴加顺序依次为: 过量的NaOH 溶液、_______、_______;
②如何证明操作①中 NaOH 溶液已经过量?_______。
③蒸发过程所用的主要仪器有:铁架台、酒精灯、_______;
(2)某同学在实验室中用四氯化碳萃取较高浓度的溴水中的溴,经振荡并在铁架台上静置分层后,
①分离出四氯化碳层的操作是:_______。
②分离溴的四氯化碳溶液的操作方法是:_______。
(3)工业上将较高浓度的溴水经进一步处理得到工业溴。某研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料, Br2的沸点为 59℃,微溶于水,有毒性和强腐蚀性。水的沸点为 100℃。他们参观生产过程后,设计了如下装置简图:

①图中仪器 B 的名称:_______。
②用热水浴加热的优点是:_______。
③实验装置气密性良好,要达到提纯溴的目的,收集溴时温度计应控制的温度为:_______℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列空白。
(1)“辛烷值”用来表示汽油的质量,汽油中异辛烷的爆震程度最小,将其辛烷值标定为100,下图是异辛烷的球棍模型,则异辛烷的系统命名为_________________。
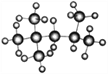
(2)写出下列反应的化学方程式和反应类型
①2—溴丙烷与NaOH溶液:________________________。
②苯酚和饱和溴水:____________________________。
(3)有机物A可以通过不同的反应得到B和C:
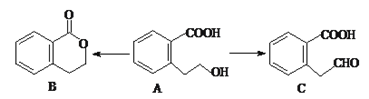
①A的分子式为___________________,C的含氧官能团名称为___________________。
②A制取B的有机反应类型为________________。
③A制取C的化学方程式为:_____________________________________________。
④A发生消去反应后产物的结构简式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:Fe3+→Fe2+;MnO![]() →Mn2+;Cl2→2Cl-;HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,则得到I2最多的是( )
→Mn2+;Cl2→2Cl-;HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,则得到I2最多的是( )
A. Fe3+ B. MnO![]() C. Cl2 D. HNO2
C. Cl2 D. HNO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com