
【题目】1799年,意大利物理学家伏特把一块锌板和一块锡板浸在盐水里,发现连接两块金属板的导线中有电流通过。下列说法正确的是( )
A.锌板是正极
B.锡板被氧化
C.盐水是电解质溶液
D.电子由锡板沿导线流向锌板
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
【题目】下列有关比较正确的是( )
A.N、O、F最高价依次升高
B.Al3+、S2-、F-微粒半径依次增大
C.单质的熔点:Cl2>Br2>I2
D.碱性:CsOH>KOH>NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
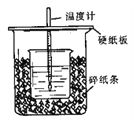
(1)从实验装置上看,图中尚缺少的一种玻璃用品是________________。
(2)烧杯间填满碎纸条的作用是________________。
(3)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量________________(填“相等、不相等”),所求中和热___________(填“相等、不相等”)。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验, 测得的中和热的数值会________________。(填“偏大”、“偏小”、“无影响”)。
Ⅱ、(1)下图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:__________________________。

(2)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。已知:C(s,石墨)+O2(g)=CO2(g) △H1=-393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H3=-2599kJ·mol-1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的焓变:△H=___________。
(3)1.3gC2H2完全燃烧生成液态水和CO2,放出62kJ热量,写出C2H2燃烧的热化学方程式:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于2 mol氨气,下列说法正确的是
A. 质量为17 g
B. 含有6.02×![]() 个NH3分子
个NH3分子
C. 标准状况下的体积为44.8 L
D. 溶于1 L水后,溶液中NH4+的浓度为2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“除氢气外,烃、肼、甲醇、氨、煤气等液体或气体,均可作燃料电池的燃料”。已知肼燃烧时发生下列反应,N2H4+O2![]() N2+2H2O。以Pt为电极,以硫酸为电解质溶液组成肼燃料电池,下列关于肼燃料电池的说法中不正确是 )
N2+2H2O。以Pt为电极,以硫酸为电解质溶液组成肼燃料电池,下列关于肼燃料电池的说法中不正确是 )
A. 肼是燃料电池的负极反应物,O2是正极反应物
B. 肼燃料电池的正极反应为 O2 + 2H2O + 4e-= 4OH-
C. 肼燃料电池的负极反应为:N2H4 —4e—=N2↑+4H+
D. 电池工作过程中H+向正极移动,但H+物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)是一种重要的化工试剂,实验室合成硫酰氯的实验装置如下图所示:

已知:① SO2(g) + Cl2(g)![]() SO2Cl2(l) △H = -97.3 kJ/mol;
SO2Cl2(l) △H = -97.3 kJ/mol;
② 硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置甲为储气装置,用于提供氯气,则仪器A中盛放的试剂为______________。装置丙中活性炭的作用是______________。
(2)在上图方框内画出所缺装置,并注明相关试剂的名称。
(3)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为_____________,分离产物的方法是(填字母)_________。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有________(填序号)。
① 先通冷凝水,再通气 ② 控制气流速率,宜慢不宜快
③ 若三颈烧瓶发烫,可适当降温 ④ 加热三颈烧瓶
(5)在无活性炭存在的条件下SO2与Cl2也可发生反应,现将SO2、Cl2按照一定比例通入水中,请设计 一个简单实验验证二者是否恰好完全反应: (简要描述实验步骤、现象和结论)。
仪器自选,供选择试剂:滴加酚酞的氢氧化钠溶液、碘化钾溶液、淀粉溶液、品红溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA 表示阿伏加德罗常数的值。下列说法正确的是
A. 在沸水中滴入含0.1molFeC13的饱和溶液,制得胶粒数为0.1 NA
B. 含0.4mol HNO3的稀硝酸与足量Fe反应,转移电子数为1.2 NA
C. 120 gNaHSO4和MgSO4的晶体混合物中阳离子数为NA
D. 标准状况下,44.8LSO2与足量O2反应生成的SO3分子数为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉煤气为炼铁过程中产生的副产品,主要成分为N2、CO、CO2、H2O等,其中可燃成分CO含量约占25%左右,CO2、N2的含量分别占15%、55%。回答下列问题:
(1)上述提及的气体分子中,电子数相等的两种气体是________(写化学式)。
(2)高炉煤气中CO具有较高的利用价值,可以与H2合成甲烷,已知有关反应的热化学方程式如下:
① H2(g)+![]() O2(g)=H2O(l) △H=-285.8kJ/mol
O2(g)=H2O(l) △H=-285.8kJ/mol
② CO(g)+![]() O2(g)=CO2(g) △H=-283.0kJ/mol
O2(g)=CO2(g) △H=-283.0kJ/mol
③CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ/mol
则CO(g)+2H2(g)=CH4(g)+ ![]() O2(g) △H=_________kJ/mol。
O2(g) △H=_________kJ/mol。
(3)高炉煤气中N2的含量较高,利用CO前需要对CO 进行富集,实现CO和N2的分离。
① 工业上常采用醋酸亚铜氨溶液来吸收CO,该反应的热化学方程式为
CH3COOCu(NH3)2(aq)+CO(g)=CH3COOCu(NH3)2·CO(aq) △H<0。吸收CO后的溶液经过适当处理可恢复为醋酸亚铜氨溶液,从而实现CO与吸收液的分离,分离过程可采取的措施有______________(写出一种即可)。
②到目前为止,CO吸附剂的开发大多数以亚铜为活性组分负载在各种载体上,然后采用变压吸附(PSA)方式在含N2体系中脱出CO。下图是变压吸附回收高炉煤气中CO的流程图:
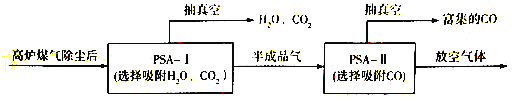
PSA-I吸附CO2时间对PSA-II中CO回收率的影响见下图,由此可见,为了保证载体亚铜吸附剂对CO的吸附和提纯要求,应采取的措施是________, “放空气体”的主要成分为_______。
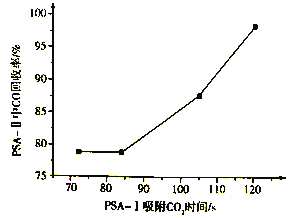
(4)高炉炼铁过程中发生的主要反应为Fe2O3(s)+ 3 CO(g)===2Fe (s)+3CO2(g)。该反应在不同温度下的平衡常数如下表所示:
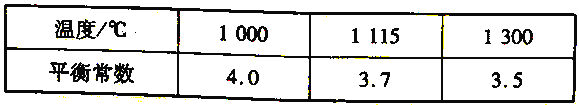
① 该反应的△H______0(填“> " " < ”或“= " )。
② 欲提高上述反应中CO 的转化率,可采取的措施是______。
a.适当降低反应体系的温度 b.及时移出体系中的CO2 c.加入合适的催化剂
d.减小容器的容积 e.增大Fe2O3的量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com