
����Ŀ���±��г��ˢ١���10��Ԫ�������ڱ��е�λ�á�
�� ���� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
4 | �� | �� |
��1������Ԫ���У���������ǿ���ǣ���Ԫ�ط��ţ���ͬ��________���ۢܢ�����Ԫ�ص�ԭ�Ӱ뾶�ɴ�С��˳����____________��
��2������Ԫ�ص�����������Ӧ��ˮ������������ǿ����________���ѧʽ��
��3��Ԫ�آ��⻯��ĵ���ʽΪ____________�����⻯����Ԫ�آ�����������Ӧ��ˮ���ﷴӦ�Ļ�ѧ����ʽΪ____________��
��4���ȽϢ͢��⻯����ȶ�����ǿ������˳����____________���ѧʽ����
���𰸡�K Mg��Al��C HClO4 ![]() NH3+HNO3=NH4NO3 NH3��PH3
NH3+HNO3=NH4NO3 NH3��PH3
��������
�������ڱ���λ�ã���Ԫ�طֱ�Ϊ��Na��K��Mg��Al��C��N��P��Cl��Br��Ne��
(1)��Ԫ�����ڱ��У�Խ�������£�Ԫ�ؽ�����Խǿ��Խ���ҡ����ϣ�Ԫ�صķǽ���Խǿ������õĽ���Ԫ���ǽ�������ǿ����K��Mg��Al��Si������Ԫ�ص�ԭ�Ӱ뾶��ԭ�������ĵ�������С��C��Siͬһ���Ԫ�ش��ϵ��£�����Ӳ������࣬ԭ�Ӱ뾶���ۢܢ�����Ԫ�ص�ԭ�Ӱ뾶�ɴ�С��˳����Mg��Al��Si��C���ʴ�Ϊ��K��Mg��Al��C��
(2)�ǽ�����Խǿ����Ӧˮ��������Խǿ��Ҳ����Խ��Ԫ�����ڱ����Ͻǵ�Ԫ������������Ӧ��ˮ��������Խǿ,���ڷ�Ԫ�������ۣ���������Ԫ�ص�����������Ӧ��ˮ������������ǿ����HClO4���ʴ�Ϊ��HClO4��
(3)Ԫ�آ��⻯����NH3��N�����5�����ӣ���3�����γ�3�����ۼ�������һ���µ��Ӷԣ�����ʽΪ![]() �����⻯����Ԫ�آ�����������Ӧ��ˮ����HNO3��Ӧ�Ļ�ѧ����ʽΪNH3+HNO3=NH4NO3���ʴ�Ϊ��
�����⻯����Ԫ�آ�����������Ӧ��ˮ����HNO3��Ӧ�Ļ�ѧ����ʽΪNH3+HNO3=NH4NO3���ʴ�Ϊ��![]() ��NH3+HNO3=NH4NO3��
��NH3+HNO3=NH4NO3��
(4)�ǽ�����Խǿ���⻯����ȶ���Խǿ��N��P��ͬһ�����Ԫ�أ����ϵ����⻯����ȶ��Լ������͢��⻯����ȶ�����ǿ������˳����NH3��PH3���ʴ�Ϊ��NH3��PH3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ǻ���������ҩ��ϳɵ���Ҫ�м��壬�����ɱ��Ӻ���ȩ�ᷴӦ�Ƶã�
![]() +
+![]() ��
��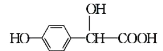
(��ȩ��) (�ǻ�������)
�����й�˵����ȷ����
A. �÷�Ӧ��ȡ����Ӧ
B. ![]() ���ǻ������ụΪͬϵ��
���ǻ������ụΪͬϵ��
C. 1���ǻ�����������������17��ԭ�ӹ�ƽ��
D. 1 mol�ǻ��������������ֱܷ��1 mol NaHCO3��2 mol NaOH��3 mol Na��4 mol H2������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݷ�Ӧ��2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)��Ƶ�ԭ�����ͼ��ʾ��
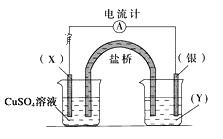
��ش��������⣺
(1)�缫X�IJ�����__���������ҺY��__��
(2)���缫Ϊ��ص�__���������ĵ缫��ӦΪ__��
(3)X�缫�Ϸ����ĵ缫��ӦΪ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ��װ�ü���;������ȫ��ȷ����
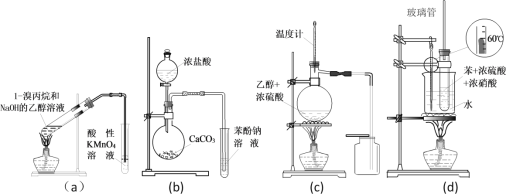
A. aװ�ü�����ȥ��Ӧ���б�ϩ����
B. bװ�ü������ԣ����̼�����
C. cװ������ʵ������ȡ���ռ���ϩ
D. dװ������ʵ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1������8�ֻ�ѧ���ţ�![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]()
�ٱ�ʾ���صķ��Ź�________�֡�
����������ȣ������ܻ���ͬλ�ص���________��________��
��2��Ϊ��֤��Ԫ�صķǽ����Ա���Ԫ�صķǽ�����ǿ��ij��ѧʵ��С���������ͼʵ�飬��ش�
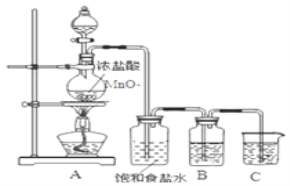
��װ��B��ʢ�ŵ��Լ���____________(��ѡ��)��ʵ������Ϊ____________��
A��Na2S��Һ B��Na2SO3��Һ C��Na2SO4��Һ
����֤����Ԫ�ر���Ԫ�طǽ�����ǿ������Ϊ____________��(�����)
A������Ϊǿ�ᣬ������Ϊ���� B��������������Ա�ϡ����ǿ
C��S2-��Cl-��ԭ��ǿ D��HCl��H2S�ȶ�
��3����2L���ܱ������з���4molN2O5���������·�Ӧ��2N2O5(g)![]() 4NO2(g)+O2(g)����Ӧ��5minʱ�����N2O5ת����20%����v(NO2)Ϊ_________��5minʱ��N2O5�ڻ�������е����������____________��
4NO2(g)+O2(g)����Ӧ��5minʱ�����N2O5ת����20%����v(NO2)Ϊ_________��5minʱ��N2O5�ڻ�������е����������____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ե��з�̪��Һ��������Һ����������ɫ�������
A. ������Һ���� B. CH3COONa��Һ����
C. ��ˮ�м�������NH4Cl���� D. С�մ���Һ�м�������NaCl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪NA�ǰ����ӵ�������ֵ������˵����ȷ����
A.11 g�غ������صĻ������е�������ĿΪ0.4NA
B.28 g����ϩ��![]() �����е�������ĿΪ16NA
�����е�������ĿΪ16NA
C.����״����224 mL SO2����ˮ�Ƴ�100 mL��Һ��H2SO3��![]() ��
��![]() ������Ŀ֮��Ϊ0.01NA
������Ŀ֮��Ϊ0.01NA
D.��63 g HNO3��Ũ����������ͭ��ȫ��Ӧ��ת�Ƶ�����ĿΪ0.50NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ӡˢ��·���ڵ�����ҵ��Ӧ�ù㷺,���е�ͭ����·��ͨ����ѧ�Լ���ʴ�������л���Ե�����ϵ�ͭ���γɵġ��ӷ�����ӡˢ��·���Ͽ��Ի���ͭ���仯����ס��ҡ�������ͬѧ�ֱ�����˲�ͬ�Ļ��շ������£����ֲ�����ȥ����
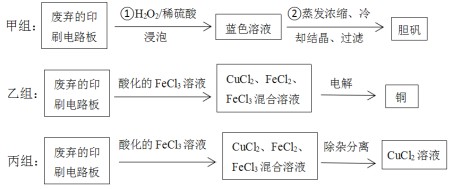
��1�����鲽����з�Ӧ�����ӷ���ʽΪ��______��
��2������ͬѧ����ʵ��ʱ������H2O2�ѱ��ʲ���ʹ�ã�������Ҫ�ڲ�ʹ��H2O2��ǰ����ʵ�ַ�ӦCu+H2SO4=CuSO4+H2����������Ϊ��ʵ�ָ�ת����װ���е������ڣ�����缫���ϣ�����Cu������C��������ʵ�ֵ�װ���в�Ҫ��д����
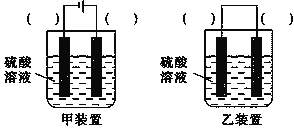
________
��3������ͬѧʹ�õ�FeCl3��Һ��Ҫ�ữ��ԭ���ǣ�________��
��4��ͼΪ������ʱ��װ��ͼ������ͭ�缫Ӧ�����Դ��_____���������������������������������۲쵽�������������ݲ���ʱ����ֹͣ��⣬��ʱҪ���յ�ͭ��ȫ�������������������ĵ缫��ӦΪ������Ӧ�������Ⱥ�˳����д����_____��___��___��
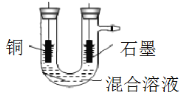
��5������ͬѧ��1L 0.2mol/L��FeCl3��Һ�ܽ�ͭ�����ʱ������������ɫ����0.56L����״���£�ʱֹͣ��⣬��ʱ���������������ڱ�״���µ������_____L��
��6������ͬѧ����FeCl3��ʴͭ���Ļ��Һ��,��Cu2+��Fe3+��Fe2+��Ũ�Ⱦ�Ϊ0.10mol/L��������±����������ݺ�ҩƷ,������ȥCuCl2��Һ��Fe3+��Fe2+��ʵ�鲽�裨д���Լ��Ͳ�������_____________����____���۹�����ȥ������
�������↑ʼ����ʱ��pH | �������������ȫʱ��pH | |
Fe3+ | 1.9 | 3.2 |
Fe2+ | 7.0 | 9.0 |
Cu2+ | 4.7 | 6.7 |
�ṩ��ҩƷ:Cl2��Ũ���ᡢNaOH��Һ��CuO��Cu | ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������±�����Ĵ�����ͨ�����������̽��������±���������ʣ����Դﵽ��һ������������ͨ��Ч����
I����֪��NaBr+H2SO4(Ũ) ![]() NaHSO4+ HBr
NaHSO4+ HBr
CH3CH2OH+HBr ![]() CH3CH2Br+H2O
CH3CH2Br+H2O
������ķе�38.4�棬ʵ�����Ʊ������飨CH3CH2Br����װ�úͲ������£�
�ټ��װ�õ������ԣ���װ��ͼ��ʾ��U�ιܺʹ��ձ��м����ˮ��
����Բ����ƿ�м���10mL95%�Ҵ���28mL78%Ũ���ᣬȻ�������ϸ��13g�廯�ƺͼ������Ƭ��
��С�ļ��ȣ�ʹ���ַ�Ӧ��
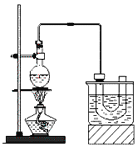
�ش��������⣺
��1��Ϊ�˸��õĿ��Ʒ�Ӧ�¶ȣ�����ͼʾ��С����ȣ����õļ��ȷ�ʽ��_______________��
��2��Ũ�������ǿ�����ԣ���������ԭ������HBrΪBr2������U�ι��д��Ƶ���������ػ�ɫ��Ϊ�˳�ȥ�ֲ�Ʒ�е�����Br2����ѡ�������Լ��еģ�______������ţ�
A��NaOH��Һ B��H2O
C��Na2SO3��Һ D��CCl4
����ʱ�������Ҫ����������______________�����������ƣ���Ҫ��һ���Ƶô����������飬����ˮϴ��Ȼ�������ˮCaCl2���ٽ���_________����������ƣ���
II���������ڲ�ͬ�ܼ�����NaOH�ɷ�����ͬ���͵ķ�Ӧ�����ɲ�ͬ�ķ�Ӧ���ijͬѧ��������������ʣ���ͼʵ��װ��(����̨���ƾ�����)��֤ȡ����Ӧ����ȥ��Ӧ�IJ������һ�����̽����
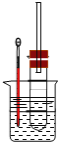
��1�����Թ��м���5 mL 1 mol/L NaOHˮ��Һ��5 mL �����飬���Թ���ͼ�̶����ȡ��Թܿڰ�װһ�����ܵ�������_________��
��2�����Թ��м���5 mL NaOH�Ҵ���Һ��5 mL �����飬���Թ���ͼ�̶����ȡ�
����д���÷�Ӧ�Ļ�ѧ����ʽ_____________________________________________��
��Ϊ֤����������NaOH�Ҵ���Һ�з���������ȥ��Ӧ������Ƶ�ʵ�鷽���У���Ҫ�������___________�������װ����ͼ��ʾ��������ͨ�����Ը��������Һǰ��һ��ʢˮ���Թܣ���������_____________��
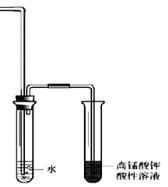
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com