
【题目】下列有关实验装置及用途叙述完全正确的是
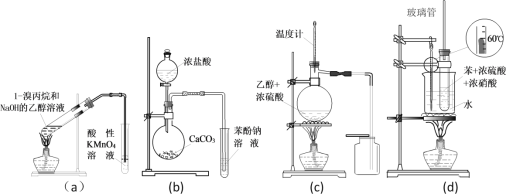
A. a装置检验消去反应后有丙烯生成
B. b装置检验酸性:盐酸>碳酸>苯酚
C. c装置用于实验室制取并收集乙烯
D. d装置用于实验室制硝基苯
【答案】D
【解析】
A.乙醇易挥发,结合乙醇的性质分析判断;
B.盐酸易挥发,根据盐酸与苯酚钠能否反应,结合实验目的分析判断;
C.制备乙烯需要测定反应液的温度170℃,据此判断;
D.苯与浓硝酸发生取代反应生成硝基苯,水浴加热控制温度50~60℃,据此判断。
A.乙醇易挥发,也能被高锰酸钾氧化,则应排除乙醇的干扰,再检验,故A错误;
B.盐酸易挥发,盐酸与苯酚钠反应,则不能比较碳酸、苯酚的酸性,应排除盐酸的干扰,故B错误;
C.制备乙烯测定反应液的温度170℃,则温度计的水银球应在液面下,故C错误;
D.苯与浓硝酸发生取代反应生成硝基苯,水浴加热控制温度50~60℃,则图中装置可制备,故D正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】一种防止血栓形成与发展的药物J的合成路线如图所示(部分反应条件略去):
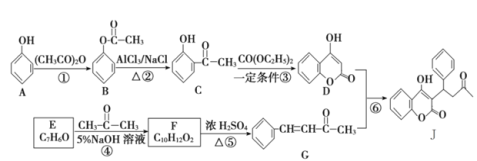
回答下列问题:
(1)A中官能团的名称是_________,反应⑤的反应类型是___________。
(2)J的分子式是__________。F的结构简式是_________。
(3)反应③的化学方程式为____________________________________。
(4)已知C有多种同分异构体。写出同时满足下列条件的C的同分异构体的结构简式__________。(只需写出两个)
①苯环上有两个处于对位上的取代基;
②1mol该有机物与足量金属钠反应生成1g氢气。
(5)请参照J的合成方法,完成下列合成路线:___________________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个化学过程的示意图。
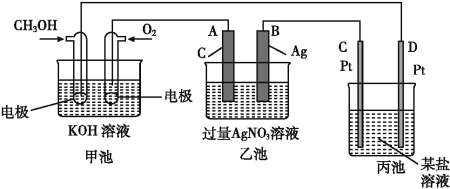
(1)C(Pt)电极的名称是____。
(2)写出通入O2的电极上的电极反应式:_______________。
(3)写出通入CH3OH的电极上的电极反应式:_________。
(4)若丙池是电解饱和食盐水溶液,在____(填“阳极”或“阴极”)附近滴入酚酞溶液变红。
(5)乙池中反应的化学方程式为____。
(6)当乙池中B(Ag)极的质量增加5.40 g时,甲池中理论上消耗O2____mL(标准状况下);若丙池中饱和食盐水溶液的体积为500 mL,电解后,溶液的pH=_____。(25 ℃,假设电解前后溶液的体积无变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两套如图所示装置,分别为装置①和装置②,各盛有2g锌粒(颗粒大小相同)。
实验①:在装置①中加入40mL1mol/L的硫酸
实验②:在装置②中加入40mL4mol/L的硫酸。
比较二者收集10mLH2时所用的时间。
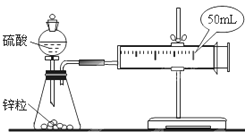
(1)当收集到10mLH2时,哪个实验所耗时间较长?__(填写实验序号)为什么?__。
(2)活塞外移的情况是__。
A.均匀外移 B.先快后慢 C.先慢后快 D.先慢后快,然后又逐渐减慢
你选择的理由是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在体积均为20mL、浓度均为0.1mol·L-1的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)表示为pH水=-lgc(H+)水。pH水与滴加氢氧化钠溶液体积的关系如图所示。
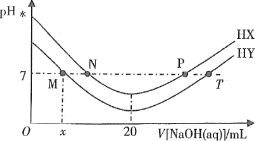
下列推断正确的是
A.HX的电离方程式为HX=H++X-
B.T点时c(Na+)=c(Y-)>c(H+)=c(OH-)
C.常温下用蒸馏水分别稀释N、P点溶液,pH都降低
D.常温下,HY的电离常数![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝及其化合物在生产生活中具有重要的作用。
(1)铝属于活泼金属却能在空气中稳定存在,原因是(用化学用语及相关文字说明)___________
(2)铝电池性能优越,在现代生产、生活中有广泛的应用。铝-空气电池以其环保、安全而受到越来越多的关注,其原理如下图所示。
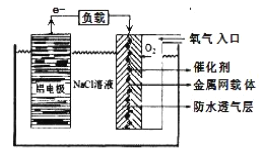
该电池的正极反应方程式为 _____;电池中NaCl溶液的作用是 ______;以该电池为电源,用惰性电极电解Na2SO4溶液,当Al电极质量减少1.8g时,电解池阴极生成的气体在标准状况下的体积为_______L。
(3)AlCl3与NaN3在高温下反应可制得高温结构陶瓷氮化铝(AlN),且生成N2。NaN3晶体中阴、阳离子个数比为______,写出反应化学方程式为___________
(4)同主族的元素应用广泛。2019年1月3日上午,嫦娥四号探测器翩然落月,首次实现人类飞行器在月球背面的软着陆。所搭载的“玉兔二号”月球车,通过砷化镓(GaAs)太阳能电池提供能量进行工作。回答下列问题:
①基态Ga原子价电子排布式____,核外电子占据最高能级的电子云形状为____;基态As原子最高能层上有____个电子。
②镓失去电子的逐级电离能(单位:kJ/mol)的数值依次为577、1985、2962、6192,-1由此可推知镓的主要化合价为_____和+3,砷的第一电离能比镓_____填“大”或“小”)。
③第四周期元素中,与基态As原子核外未成对电子数目相同的元素符号为____。
④砷化镓可由(CH3)3Ga和AsH3在700℃制得,(CH3)3Ga中C原子的杂化方式为 ______,AsH3分子的空间构型为______。
⑤相同压强下,AsH3的沸点_______NH3(填“大于”或“小于”),原因为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了①~⑩10种元素在周期表中的位置。
族 周期 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑤ | ⑥ | ⑩ | |||||
3 | ① | ③ | ④ | ⑦ | ⑧ | |||
4 | ② | ⑨ |
(1)上述元素中,金属性最强的是(填元素符号,下同)________,③④⑤三种元素的原子半径由大到小的顺序是____________。
(2)上述元素的最高价氧化物对应的水化物中酸性最强的是________(填化学式)
(3)元素⑥的氢化物的电子式为____________,该氢化物与元素⑥的最高价氧化物对应的水化物反应的化学方程式为____________。
(4)比较⑥和⑦氢化物的稳定性由强到弱的顺序是____________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的的是( )

A.用图甲装置模拟实验室进行石油的分馏实验
B.用图乙装置制取乙酸乙酯并除去其中的醋酸
C.用图丙装置可以检验溴乙烷与NaOH醇溶液共热产生的乙烯
D.用图丁装置分离苯和苯酚钠的水溶液,先从分液漏斗下口放出有机相
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中,T所处的周期序数与主族序数相等。请回答下列问题:
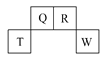
(1)R的原子结构示意图为__。
(2)元素的非金属性(原子的得电子能力):Q___W(填“>”或“<”),Q的最高价氧化物的电子式为___,Q的一种氢化物的相对分子量是氢气相对分子量的36倍,该氢化物可能的结构简式有___。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为___。
(4)原子序数比R多1的元素的一种氢化物能分解出它的另一种氢化物,此分解反应的化学方程式是___。
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成R的含氧酸盐只有一种。则该含氧酸盐的化学式是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com