
【题目】短周期元素W、X、Y、Z的原子序数依次增大,其中Z为金属且Z的原子序数为W的2倍。n、p、q是由这些元素组成的二元化合物,常温下,n为气体。m、r、s分别是Z、W、X的单质,t的水溶液呈碱性焰色反应呈黄色,上述物质间的转化关系如图所示。下列说法正确的是

A. 简单离子半径:Z>Y>X B. 化合物P中只存在离子键
C. 图示转化关系涉及的反应均为氧化还原反应 D. 最简单气态氢化物的稳定性:W>X
【答案】C
【解析】已知W、X、Y、Z是原子序数依次增大的短周期元素;Z为金属且Z的原子序数为W的2倍;n、p、q是由这些元素组成的二元化合物,常温下n为气体;m、r、s分别是Z、W、X的单质,t的水溶液显碱性且焰色反应呈黄色,结合转化关系图可得:W为C、X为O、Y为Na、Z为Mg,m为金属镁、n为CO2、p为Na2O2、q为MgO、r为碳单质、s为O2、t为Na2CO3。A、离子的核外电子层数越多,离子半径越大,核外电子排布相同时,离子半径随原子序数的增大而减小,则简单离子半径:X>Y>Z,A错误;B、p为Na2O2既存在离子键又存在非极性键,B错误;C、图示转化关系涉及的反应为:2Mg+CO2![]() 2MgO+C、
2MgO+C、
2CO2+2Na2O2=2Na2CO3+ O2↑、C+O2![]() CO2,均为氧化还原反应,C正确;D、W的最简单气态氢化物为CH4,X的最简单氢化物为H2O,故最简单气态氢化物的稳定性:W<X,D错误。答案选C。
CO2,均为氧化还原反应,C正确;D、W的最简单气态氢化物为CH4,X的最简单氢化物为H2O,故最简单气态氢化物的稳定性:W<X,D错误。答案选C。


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
【题目】氟及氟产品在工农业生产中应用非常广泛,回答下列问题:
(1)基态氟原子核外电子的运动状态有__种,这些电子的电子云形状有__种;氟原子的外围电子排布式为______.
(2)NaHF2(氟化氢钠)电解可制氟气,NaHF2中所含作用力的类型有_____;与HF2-互为等电子体的分子有___(举一例).
(3)N2F2(二氟氮烯)分子中,氮原子的杂化轨道类型为____.
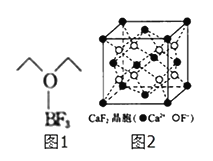
(4)三氟化硼乙醚(如图1)的熔点为-58℃,沸点为126~129℃,它属于__晶体.
(5)氟化钙的晶胞结构如图2所示,晶胞参数α=0.555nm.
①Ca2+、F-的配位数分别为__和__.
②列式表示氟化钙晶体的密度:_________gcm-3(不必计算出结果).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiO(OH)+2H2O![]() Cd(OH)2+2Ni(OH)2。有关该电池的说法正确的是( )
Cd(OH)2+2Ni(OH)2。有关该电池的说法正确的是( )
A. 充电过程是化学能转化为电能的过程 B. 充电时阳极反应:Ni(OH)2-e-+OH-=NiO(OH)+H2O
C. 放电时负极附近溶液的碱性不变 D. 放电时电解质溶液中的OH-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,满足下列条件的溶液一定呈酸性的是
A. 能与金属Al反应放出H2的溶液B. 加酚酞后显无色的溶液
C. pH=6的某溶液D. c(H+)>c(OH—)的任意水溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中的一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质
①是溶液②是胶体
③能产生丁达尔效应④能透过滤纸
⑤不能透过滤纸⑥静置后,会析出黑色沉淀
A.①④⑥ B.②③④ C.②③⑤ D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4–和有机阳离子构成电解质溶液,其放电工作原理如下图所示。下列说法不正确的是
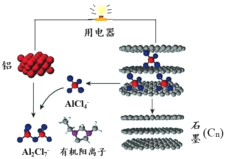
A.放电时,铝为负极、石墨为正极
B.放电时,有机阳离子向铝电极方向移动
C.放电时的负极反应为:Al –3e- + 7AlCl4– = 4Al2Cl7–
D.充电时的阳极反应为:Cn + AlCl4––e- = CnAlCl4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com