
����Ŀ����Դ�������������ش�п����м�����渽��пƤ���������⼰���ۣ��кܶ���;��ij�����ۺ����ö�п����м�Ĺ�������ͼ����ش�

��1��������������Һ���ݷ���м��Ŀ����_________��
��2���������������ʺϳ䵱������A����_______�����ţ���
A�� KMnO4 B�� Cl2 C��H2O2 D�� HNO3
��3���ۺ�������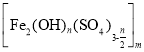 ��ˮ��������Ҫ�����������ۺϸ�����Ҫ������ˮ���������ۺ����������̣���ˮ����ʱ��Ӧ�Ļ�ѧ����ʽΪ__���ۺϸ�����Һ��pH���������һ���ķ�Χ�ڣ�pHƫСFe3+ˮ��̶�����pHƫ����__������ڳ�ѹ��������ѹ�������ŵ���__��
��ˮ��������Ҫ�����������ۺϸ�����Ҫ������ˮ���������ۺ����������̣���ˮ����ʱ��Ӧ�Ļ�ѧ����ʽΪ__���ۺϸ�����Һ��pH���������һ���ķ�Χ�ڣ�pHƫСFe3+ˮ��̶�����pHƫ����__������ڳ�ѹ��������ѹ�������ŵ���__��
��4������Fe3O4�������ڸ���ʯīϩ���ϵ����ܡ��Ƶ���ҺBʱ�����������A��������ԭ����_____��
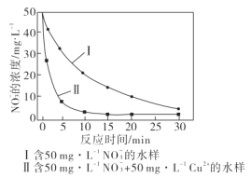
��5������мҲ�����������������ۣ����������ܹ�ȥ������ˮ�е�NO3-����Ӧ�����ӷ���ʽΪ4Fe+NO3-+10H+=4Fe2++NH4++3H2O���о����֣���pHƫ�ͽ��ᵼ��NO3-��ȥ�����½�����ԭ����__����ͬ�����£���������ȥ����ͬˮ����NO3-�������нϴ���죨����ͼ���������ò���Ŀ���ԭ����___��
���𰸡���ȥ��м��������ۡ��ܽ�пƤ C Fe2(SO4)3+nH2O![]() +
+![]() H2SO4 �γ������������� ���������¶ȷ�ֹ����ֽ� ʹ��ҺB�е�Fe2+��Fe3+����һ������ ����������H+��Ӧ����H2 Cu��Cu2+����������ȥ��NO3-�ķ�Ӧ�����γɵ�Fe-Cuԭ���������������ȥ��NO3-�ķ�Ӧ���ʣ�
H2SO4 �γ������������� ���������¶ȷ�ֹ����ֽ� ʹ��ҺB�е�Fe2+��Fe3+����һ������ ����������H+��Ӧ����H2 Cu��Cu2+����������ȥ��NO3-�ķ�Ӧ�����γɵ�Fe-Cuԭ���������������ȥ��NO3-�ķ�Ӧ���ʣ�
��������
��������ͼ������м���顢��ɸ����NaOH���м�������з���м����������ڼ���������ˮ�⣬п�Ļ�ѧ���ʺ������ƣ�Ҳ�ܺ�NaOH��Ӧ����пƤ�ܽ⡣���˺�õ�����Һ����Ҫ�ɷ�Ϊƫп���ƣ�������ҺpHֵ������Zn(OH)2��������һϵ�б仯�����յõ�ZnO��
�������õIJ������а�����м����������ʣ����������������ɵõ�FeSO4��Fe2(SO4)3�Ļ����Һ���������Һ��Ϊ2�ݣ�һ�ݼ�����������������ڷ�Ӧ���н�Fe2+��ȫ����ΪFe3+�����ھۺϸ��м���ˮ�����ᣬȻ����м�ѹ�����õ��ۺ�����������һ���м�������������������Һ�в���Fe2+����ΪFe3+��������ҺpH�������֪����ҺB�к�Fe2+��Fe3+������ҺB�м���NaOH��Ȼ��ͨ��N2�����������£��õ�����Fe3O4���ݴ˷�����
��1������м���渽��пƤ���������⼰���ۣ������ڼ���������ˮ�⣬п������NaOH��Ӧ������NaOH��Һ���ݿɳ�ȥ����м��������ۡ��ܽ�пƤ����Ϊ����ȥ��м��������ۡ��ܽ�пƤ��
��2�������̿�֪��������A������û�������µ����ʣ���ֻ��H2O2��������������������Ϊ��C��
��3������Fe3+��ˮ�⣬�ɵ�ˮ�ⷴӦ����ʽΪ��Fe2(SO4)3+nH2O![]() +
+![]() H2SO4����pHƫ��������Ӧ��Fe3++3OH-=Fe(OH)3��������Fe(OH)3����������ڳ�ѹ��������ѹ����ʱ�ɽ������ʵķе㣬�Ӷ����������¶ȣ��ܷ�ֹ������������ʵķֽ⡣��Ϊ��Fe2(SO4)3+nH2O
H2SO4����pHƫ��������Ӧ��Fe3++3OH-=Fe(OH)3��������Fe(OH)3����������ڳ�ѹ��������ѹ����ʱ�ɽ������ʵķе㣬�Ӷ����������¶ȣ��ܷ�ֹ������������ʵķֽ⡣��Ϊ��Fe2(SO4)3+nH2O![]() +
+![]() H2SO4���γ������������������������¶ȷ�ֹ����ֽ⣻
H2SO4���γ������������������������¶ȷ�ֹ����ֽ⣻
��4��Fe3O4��Fe2+��Fe3+�ı�ԼΪ1:2��������������A����ʹ��ҺB�е�Fe2+��Fe3+����һ����������Ϊ��ʹ��ҺB�е�Fe2+��Fe3+����һ��������
��5��pHƫ�ͣ�����Һ��H+Ũ�Ƚϴ��������ۻ��H+��Ӧ����H2���Ӷ�����NO3-��ȥ�����½����������Ũ��-ʱ��ͼ��֪����Cu2+��ˮ�����䷴Ӧʱ��϶̣���30minʱ��NO3-��Ũ�ȶ�����ȣ����֪Cu��Cu2+������������ã�Ҳ�������γɵ�Fe-Cuԭ���������������ȥ��NO3-�ķ�Ӧ���ʣ���Ϊ������������H+��Ӧ����H2��Cu��Cu2+����������ȥ��NO3-�ķ�Ӧ�����γɵ�Fe-Cuԭ���������������ȥ��NO3-�ķ�Ӧ���ʣ���


 ���Ӣ��������ϵ�д�
���Ӣ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����600 mLij�ֻ������Һ��ֻ���ܺ������������е������֣�K+��NH4+��Cl-��Mg2+��Ba2+��CO32-��SO42-���ֽ�����Һ�ֳ����ȷݣ���������ʵ�飺
��1�����һ���м���AgNO3��Һ���г���������
��2����ڶ����м�����NaOH��Һ�����Ⱥ��ռ�������0.04 mol��
��3����������м�����BaCl2��Һ�ø���ij���6.27g������������ϴ�ӡ������������Ϊ2.33g�� ��������ʵ�����������Ʋ���ȷ����
A. K+��һ������ B. Ba2+��Mg2+��һ��������
C. Cl-��һ������ D. �����Һ��CO32-��Ũ��Ϊ0.2 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��17.4g MnO2��240 mL 10 mol/L(�ܶ�Ϊ1.10g/mL)������(����)��ϼ���(����������ӷ�)��ʹ���ַ�Ӧ��������Һ�м���������AgNO3��Һ������֪��MnO2+4HCl(Ũ)![]() MnCl2+Cl2��+2H2O��
MnCl2+Cl2��+2H2O��
����(1)10 mol/L���������������____________
(2)�����������ڱ�״���µ����______________��
(3)��������������_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ݱ�������300�桢70MPa���ɶ�����̼�������ϳ��Ҵ��ѳ�Ϊ��ʵ��2CO2��g����6H2��g��![]() CH3CH2OH��g����3H2O��g�������������������
CH3CH2OH��g����3H2O��g�������������������
A. ��Ӧ����300 �����п��Ʋ�÷�Ӧ�����ȷ�Ӧ
B. ʹ�ô�������߷�Ӧ����
C. �������CO2��������H2��ת����
D. ��ƽ���������з����CH3CH2OH��H2O�����CO2��H2��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ������ˮ��Һ��ֻ���ܺ������������е������֣�K+��NH4+��Cl����Mg2+��Ba2+��CO32����SO42������ȡ���ݸ�100mL����Һ��������ʵ�飺
����һ�ݼ���AgNO3��Һ�г���������
���ڶ��ݼ�����NaOH��Һ���Ⱥ��ռ�������0.08mol��
�������ݼ�����BaCl2��Һ�ø������12.54g������������ϴ�ӡ������������Ϊ4.66g����������ʵ�飬�ش��������⣺
��1���ɵڶ��ݽ��е�ʵ���֪�������Ӧ����___________���ӣ������ʵ���Ũ��Ϊ________��
��2���ɵ����ݽ��е�ʵ���֪12.54�˳����ijɷ���______________��д������ѧʽ���������ʵ����ֱ�Ϊ______________________��
��3��ԭ��Һ���Ƿ����K+_______��ǡ�����������K+��Ũ�ȵ�ȡֵ��Χ��____________________���������ڴ˿տɲ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ�����ö���������Ũ�����Ʊ�������ʵ��װ�ã�������ͼ��գ�
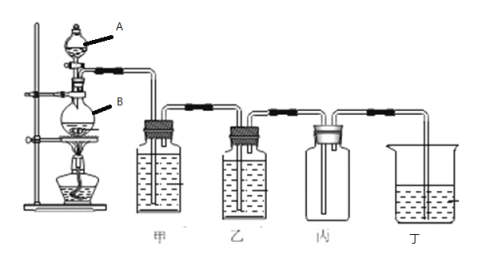
��1������A�����ƽ�_______������B�����ƽ�_______��
��2��д���ö���������Ũ�����Ʊ����������ӷ���ʽ______��
��3������ʢ��______��������_______��
��4������ʢ��______��������_____��
��5������������____��ʵ����ɺ���е�������________��
��6��������ʢ��NaOH��Һ��д��������Ӧ�����ӷ���ʽ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ǹ�ҵ����ȡ�����һ�ַ�����

��ش���������(��Ԫ������Ӧ��Ԫ�ط��ű�ʾ)��
��1�����������������У������û���Ӧ����____(�Ӧ����)��
��2��д����Ӧ�۵Ļ�ѧ����ʽ____��
��3��������W����;�ܹ㣬ͨ��������������ҵ����ֽ��ҵ���ϼ�����������������������Ȼˮ������������ʯӢɰ�ʹ��һ��������ϼ�����1 373��1 623 K��Ӧ�����ɻ�����W���仯ѧ����ʽ��____��
��4��A��B��C���������������ܼ���������Ϊ����Ŀ���һ��������___(�ѧʽ)���ֱ�ͨ��W��Һ���ܵõ���ɫ������������___(�ѧʽ)��
��5����ҵ�Ϻϳɰ���ԭ��H2���Ʒ����Ȱѽ�̿��ˮ������Ӧ����ˮú�������ᴿˮú���õ�������H2���ᴿˮú���õ�������H2�Ļ�ѧ����ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС����Ƶ�����ˮ�ⷴӦ��ͼ��ʾ���г�װ��ʡ�ԣ�������˵��������ǣ� ��
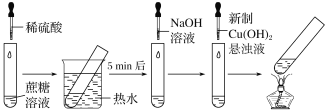
A.ϡ�������ˮԡ���ܼӿ�����ˮ������
B.�μ�NaOH��Һ��Ŀ���ǵ���Һ��pH������
C.���������ں��Թ������ɺ�ɫ����
D.ʵ������֤������ˮ���л�ԭ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ˮ�����г�����ɱ�������� HClO��ɱ��������ClO- ǿ��25��ʱ����-��ˮ��ϵ�д�������ƽ���ϵ��
Cl2(g)![]() Cl2(aq) K1=10-1.2
Cl2(aq) K1=10-1.2
Cl2(aq)+ H2O![]() HClO+H++Cl- K2=10-3.4
HClO+H++Cl- K2=10-3.4
HClO![]() H++ClO- Ka=?
H++ClO- Ka=?
����Cl2(aq)��HClO �� ClO-�ֱ�����������ռ����(��)��pH�仯�Ĺ�ϵ��ͼ��ʾ�����б�����ȷ����
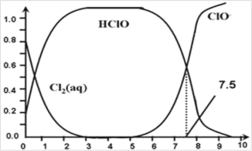
A.Cl2(g)+H2O![]() 2H++ClO-+Cl- K=10-10.9
2H++ClO-+Cl- K=10-10.9
B.���ȴ���ˮ��ϵ�У�c(HClO)+c(ClO-)=c(H+)-c(OH-)
C.���ȴ�������ˮʱ��pH=7.5ʱɱ��Ч����pH=6.5ʱ��
D.�ȴ�������ˮʱ�����ļ���ɱ��Ч�����ڶ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com